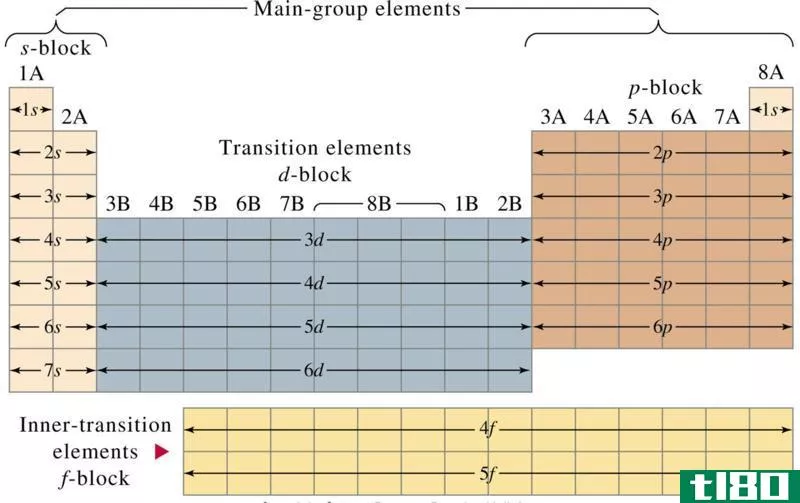
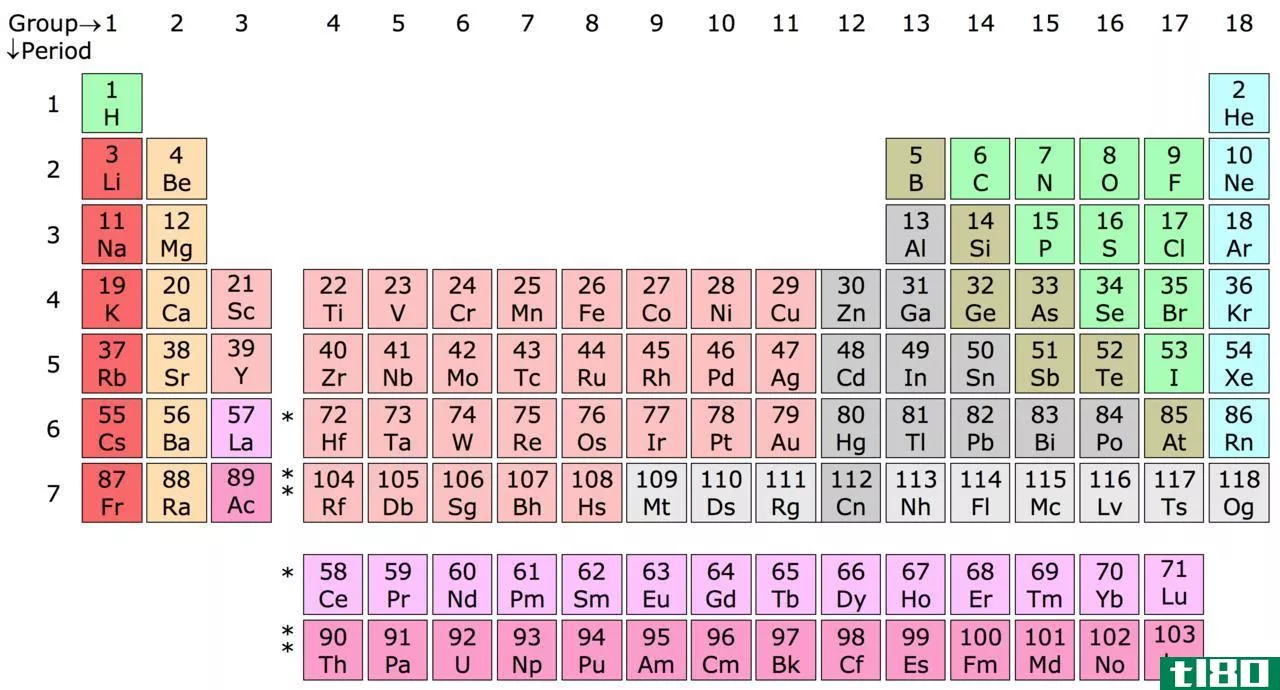
活化络合物vs过渡态|过渡络合物vs活化络合物
当一个或多个反应物转化为产物时,它们可能经历不同的修饰和能量变化。反应物中的化学键正在断裂,新的键正在形成,生成的产物与反应物完全不同。这种化学修饰被称为化学反应。有许多变量控制着反应。反应要发生,就需要能量。反应物分子在整个反应过程中经历各种变化,假设原子构型不同。活化络合物和过渡态是用来识别这些中间络合物的两个术语,大多数情况下这两个术语可以互换使用。
什么是活化复合物?
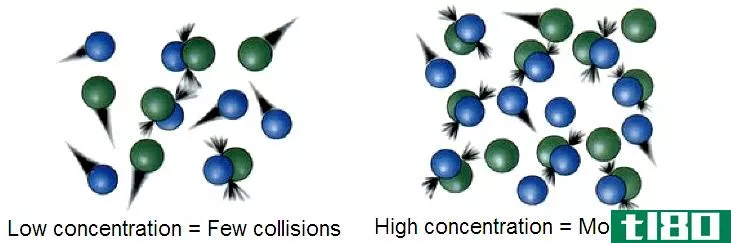
分子在发生反应之前必须被激活。分子通常没有太多的能量与他们,只是偶尔一些分子处于能量状态,以进行反应。当有两个反应物时,反应物必须以适当的方向相互碰撞。虽然反应物只是彼此相遇,但大多数相遇并不会导致反应。这些观察结果提出了对反应有一个能垒的想法。反应混合物中能量较高的反应物可视为活化络合物。并不是所有的活化络合物都会进入产物中,如果没有足够的能量,它们会退回到反应物中。
什么是过渡状态?
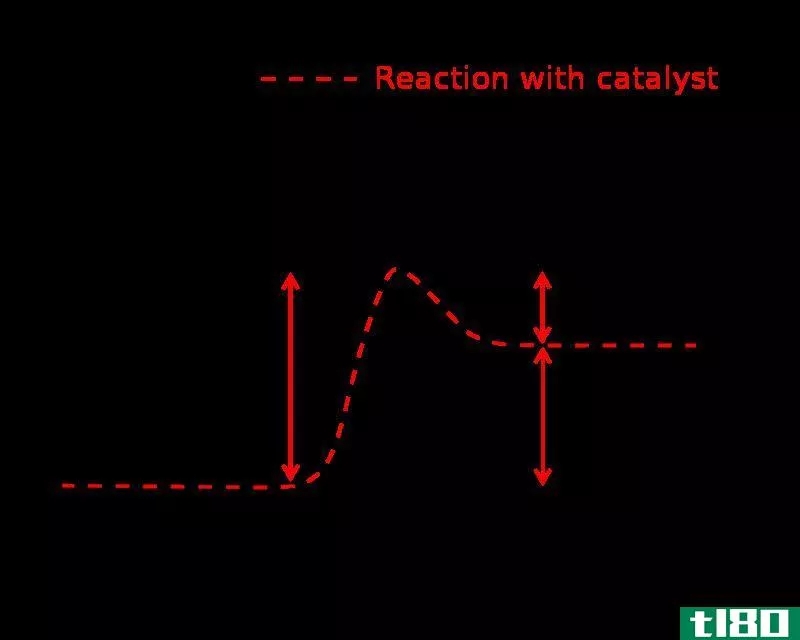
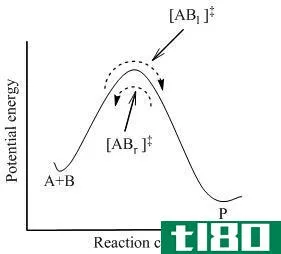
处于一种不利于反应的电子态或分子发生扭曲的电子态。在反应发生之前,分子必须通过这个高能的过渡态。这个能隙被称为活化能。这是发生反应的最高能量屏障。如果一个反应的活化度太高,只有一小部分分子有足够的能量来克服它,因此无法得到预期的产物浓度。反应中所有分子的原子排列都具有活化能,称为过渡络合物。过渡复合体具有部分断裂键和部分生成新键的组分。因此,它有部分正负电荷。过渡状态用双**符号(‡)表示。如果一个反应的过渡态能量可以降低,那么这个反应应该快得多,并且需要很低的能量才能进行。对于放热反应,下面是能量曲线。
 It is essential to know the transition state structures especially when designing the drugs for enzyme inhibition.
It is essential to know the transition state structures especially when designing the drugs for enzyme inhibition.
| 活化络合物和过渡态的区别是什么?•过渡态是反应物生成时能量最高的原子排列。活化络合物是反应途径中的所有其他构型,它们比正常分子具有更高的能量。•很可能存在过渡态络合物进入产物。然而,活化络合物可以回落形成反应物,而不是进入产物。 |