主要区别
酸碱滴定和氧化还原滴定的主要区别在于,酸碱滴定是在酸和碱存在的情况下进行的,而氧化还原滴定是在两种氧化还原物质存在下进行的。
酸碱滴定法(acid-base titration) vs. 氧化还原滴定(redox titration)
酸碱滴定发生在酸和碱的存在下,以形成结果物,但氧化还原滴定发生在两种氧化还原物存在的情况下,即,能够被氧化和还原从而得到结果物。
而酸碱滴定过程中进行的导致水分子形成的反应称为中和反应,是这种滴定发生的主要原因;然而,在氧化还原滴定中只发生氧化和还原反应。其中一种物质减少,另一种氧化,从而完成整个过程。
酸碱滴定中使用的指示剂通常是进行化学反应所涉及的酸或碱,即这种反应不需要特殊的指示剂,如用于测定终点的PH计。相反,氧化还原反应,如氧化还原物种所进行的,需要特殊的氧化还原指示剂来指示反应。
酸碱滴定是比较常见的,它们的反应可以发生在任何酸或碱之间,而与特定物质无关。它也不取决于与反应有关的酸碱的强弱。但是,在氧化还原滴定的情况下,这些类型的滴定是非常具体的,因为它们需要能够被还原或氧化的物质,因此在d块元素中常见。
比较图
什么是酸碱滴定法(acid-base titration)?
在酸碱滴定反应中,用作滴定剂的酸和碱。常用酸的一些例子是H2SO4、HNO3或HCL等。同样地,这些反应中最常用的碱是K2CO3、Na2CO3或NaOH等。酸碱滴定根据每种成分的强度进行分类,有四种类型。如果所用的酸和碱是强的,那么这种类型的滴定被称为强酸强碱滴定法,在其他情况下,类别名称随滴定剂的强弱而变化时也是一样。
用这些酸和碱作为滴定剂进行中和反应的分析物的滴定。在这个中和反应中,水作为副产品产生。将碱放在滴定瓶中,在滴定管中加入酸,这些酸和碱之间以H+离子和OH-离子的形式发生反应。
对添加到溶液中的滴定液量进行体积测量。因此,记录下与已知量溶液完全反应所需的滴定液体积,并在其化学方程式(如化学计量法)中输入数值后,确定未知溶液的浓度。
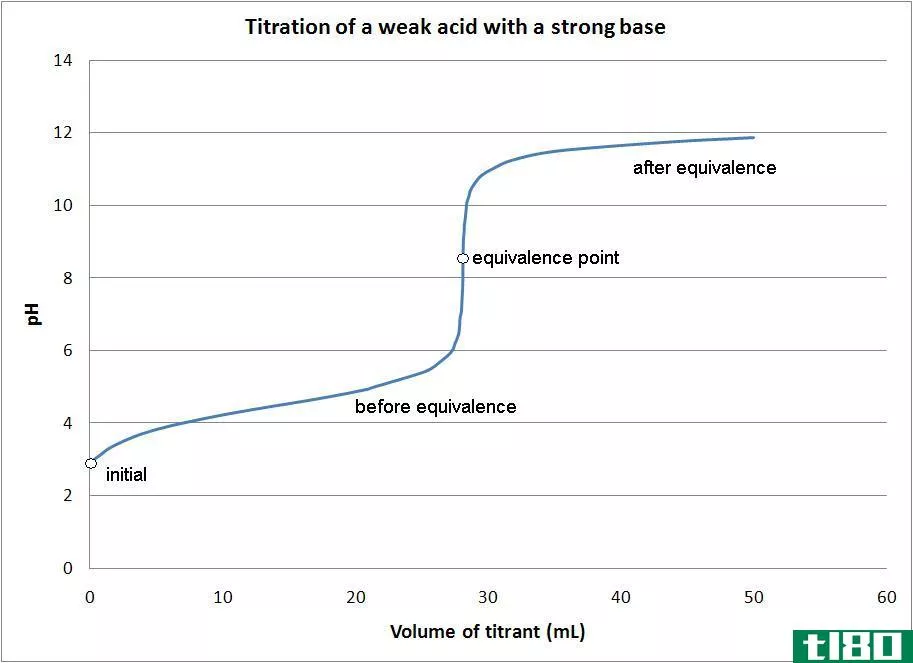
在碱性溶液中加入酸碱指示剂,以确定滴定终点。当溶液的性质从酸性变为碱性时,决定因素颜色的变化表明滴定的终点。当中和反应完成时,任何额外的酸滴都会导致溶液颜色的改变,因为它会改变溶液的性质。
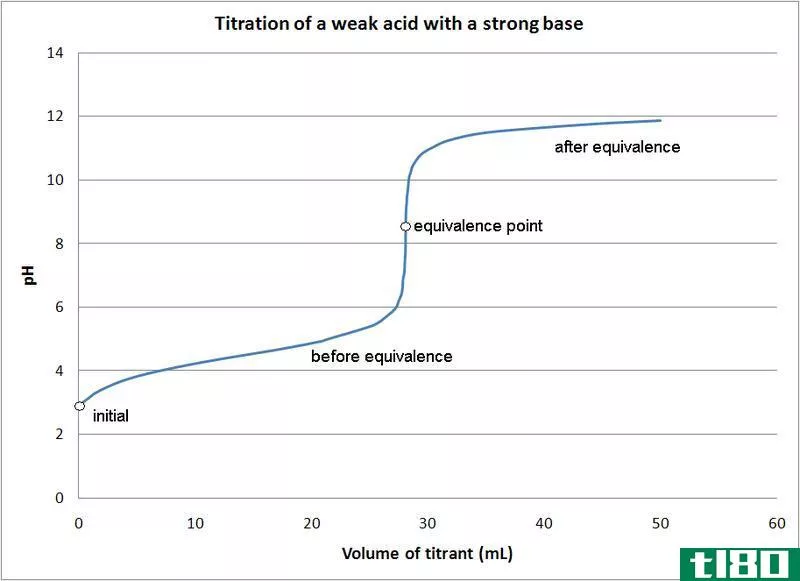
对于强酸和强碱,当量点为7,但如果使用弱酸或弱碱,PH曲线会发生变化。因此,用于酸碱滴定的指示剂通常是进行化学反应的酸或碱。因此,通常,这种反应不需要特殊的指示剂,因为ph值的变化决定了终点。酸碱滴定比较常见,这种滴定可以发生在任何酸或碱和分析物之间,而不考虑特定物质。
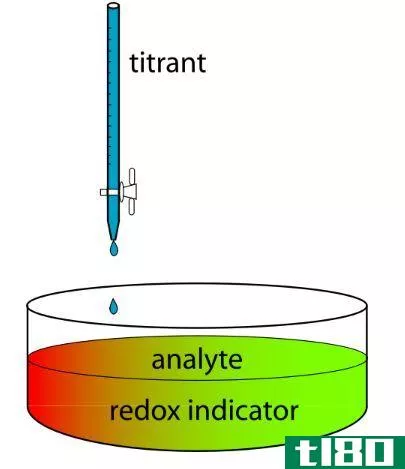
什么是氧化还原滴定(redox titration)?
氧化还原滴定是在两种氧化还原物质存在的情况下进行的,这两种氧化还原物质能够被氧化和还原,因此可以进行分析物的滴定。氧化和还原反应同时发生在同一溶液中。
其中一种氧化还原物质在反应完成时被氧化,另一种则被还原。氧化性物质释放电子,还原性物质获得完成氧化还原反应的电子。当电子的获得和丢失保持不变时,电荷在整个反应中保持不变。
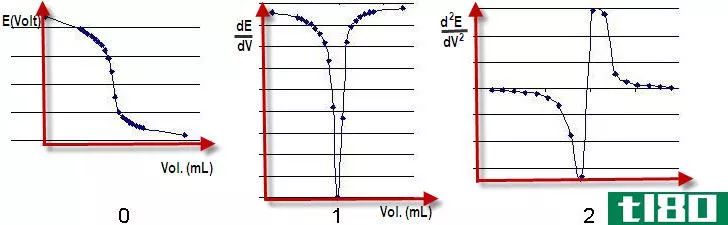
在某些情况下,如MnO4——反应过程中颜色的变化表明终点或反应状态被跟踪。但是像硫代硫酸盐还原碘到碘的情况需要淀粉作为反应终点的指示剂。当用碘溶液作为滴定剂分析葡萄酒中的二氧化硫时,这种淀粉也被用作指示剂。
这里的淀粉代表溶液中碘过量后产生蓝色淀粉碘络合物的终点,因此指示溶液的终点。与酸碱滴定不同,在这些滴定反应中使用特殊的指示剂来确定终点。在氧化还原滴定的情况下,分析物可通过使用规定的物质进行滴定,因为这种滴定非常特殊,并且需要能够被还原或氧化的物质,因此通常在d块元素中出现。与Fe2+/Fe3+的情况一样,Cr3+/Cr6+具有参与氧化还原反应的能力,因为它们具有可变的氧化数。
主要区别
- 分析物的酸碱滴定是在酸和碱的存在下进行的,以形成生成物。相反,分析物的氧化还原滴定是在两种氧化还原物质存在的情况下进行的。
- 酸碱滴定涉及一个中和反应,这也导致水的形成导致分析物的滴定,另一方面,氧化还原滴定只涉及滴定氧化还原物种的氧化和还原反应。
- 在酸碱滴定法中,终点是由反应的ph值决定的,ph值随酸或碱的变化而变化,不需要特殊的指示剂;另一方面,氧化还原滴定的终点是由特殊的氧化还原指示剂确定的。
- 酸碱滴定法更为常见,可在分析物与酸碱之间进行,也不依赖酸碱的强弱。相反,氧化还原滴定法是特殊的,因为它们需要能够被还原或氧化的物质,因此在d-嵌段元素中常见。
结论
分析物的酸碱滴定是在酸碱通过中和反应作为滴定剂存在的情况下进行的;然而,分析物的氧化还原滴定是在两种氧化还原物质存在下通过氧化和还原反应进行的。