化学中周期律的定义
周期律规定,当元素按原子序数递增的顺序排列时,元素的物理和化学性质以系统和可预测的方式重现。许多属性每隔一段时间重复出现。当元素正确排列时,元素属性的趋势变得明显,并且可以简单地根据它们在表中的位置来预测未知或不熟悉的元素。


周期律的重要性
周期律被认为是化学中最重要的概念之一。每一位化学家在研究化学元素、它们的性质和化学反应时,无论是否有意识地使用周期定律。周期律导致了现代周期表的发展。
周期律的发现
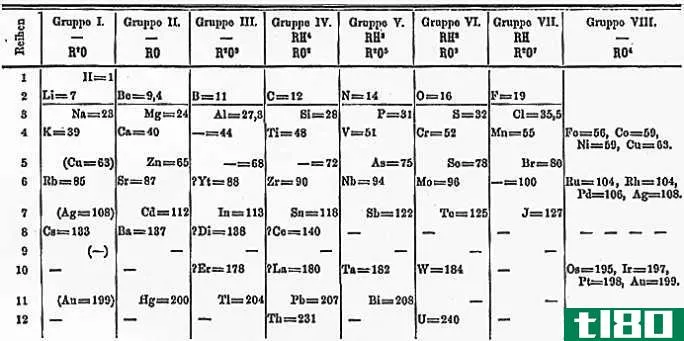
周期律是根据19世纪科学家的观察结果制定的。特别是,Lothar Meyer和Dmitri Mendeleev的贡献使元素属性的趋势变得明显。他们在1869年独立提出了周期律。元素周期表对元素进行了排列,以反映周期定律,尽管当时的科学家无法解释为何这些元素的性质会出现这种趋势。
一旦发现并理解了原子的电子结构,就很明显,间隔出现特征的原因是电子壳层的行为。
周期律影响下的性质
根据周期定律,遵循趋势的关键性质是原子半径、离子半径、电离能、电负性和电子亲和力。
原子和离子半径是单个原子或离子大小的量度。虽然原子和离子半径彼此不同,但它们遵循相同的总趋势。沿图元组向下移动时,半径会增加,而沿时段或行从左向右移动时,半径通常会减少。
电离能是从原子或离子中除去电子的容易程度的量度。该值减少了向下移动组的次数,并增加了在一段时间内从左向右移动的次数。
电子亲和力是原子接受电子的容易程度。利用周期律,碱土元素的电子亲和力很低。相比之下,卤素容易接受电子以填充其电子亚壳层,并且具有高电子亲和力。惰性气体元素几乎没有电子亲和力,因为它们有全价电子亚壳层。
电负性与电子亲和力有关。它反映了一种元素的原子吸引电子形成化学键的难易程度。电子亲和力和电负性都倾向于在向下移动一个基团时减小,而在一个周期内移动时增大。电正性是另一个受周期规律支配的趋势。电正性元素具有低电负性(例如铯、弗朗)。
除了这些性质外,还有其他与周期律相关的特征,这些特征可以被认为是元素群的性质。例如,组I(碱金属)中的所有元素都有光泽,具有+1氧化状态,与水反应,以化合物形式出现,而不是以游离元素形式出现。
- 发表于 2021-10-21 03:56
- 阅读 ( 231 )
- 分类:化学
你可能感兴趣的文章
门捷列夫(mendeleev)和现代周期表(modern periodic table)的区别
...e mendeleev) vs. 现代周期表(modern periodic table) 元素周期表是化学元素按其化学和物理性质排列的表。现代元素周期表是在一系列不同版本的元素周期表之后产生的。俄罗斯化学家/教授德米特里·门捷列夫(Dmitri mendelev)是第一个提...
- 发布于 2021-06-27 12:49
- 阅读 ( 223 )
卤素(halogen)和氙(xenon)的区别
.... 氙(xenon) 卤素和氙是分别包含在周期表第7组和第8组中的化学元素。卤素是非常活泼的元素。但氙气是一种反应性较弱的元素。卤素是周期表第7组中的化学元素,包括F、Cl、Br、I和At。它们具有不同的物理和化学性质。氙是周期...
- 发布于 2021-06-29 10:46
- 阅读 ( 446 )
锰(manganese)和镁(magnesium)的区别
... 锰的主要区别(main difference manganese) vs. 镁(magnesium) 化学元素是一种化学物质,代表原子核中质子数相同的原子。迄今为止发现的所有化学元素都被列入元素周期表。这个元素周期表根据原子核中质子数量的升序来显示化学...
- 发布于 2021-06-29 11:38
- 阅读 ( 479 )
锕系元素(actinides)和镧系元素(lanthanides)的区别
...系元素(lanthanides) 锕系元素和镧系元素是元素周期表f区的化学元素。这意味着它们的价电子在原子的f轨道上。这些化学元素以金属形式存在,被称为内过渡金属。f区块仅由镧系和锕系组成。因为锕系元素是从一种叫做锕的化学...
- 发布于 2021-06-29 13:14
- 阅读 ( 523 )
原子半径(atomic radius)和离子半径(ionic radius)的区别
...阳离子半径。 Figure 2: Atomic and Ionic Radii of Some Elements 同一化学元素的离子可以根据电荷的大小而有不同的大小。求离子半径最常用的方法是X射线晶体学。和原子半径一样,离子半径在周期表中也有变化趋势。当我们向下移动周...
- 发布于 2021-06-29 14:30
- 阅读 ( 973 )
d(d)和f块元素(f block elements)的区别
主要差异d(main difference d) vs. f块元素(f block elements) 化学元素是任何不能用化学方法分解或改变的物质。已知的化学元素有118种。这些化学元素是物质的组成部分。所有化学元素都按原子序数递增的顺序排列在元素周期表中。周...
- 发布于 2021-06-29 23:23
- 阅读 ( 454 )
电子亲和力(electron affinity)和电离能(ionization energy)的区别
... 电离能(ionization energy) 电子是原子的亚原子粒子。有许多化学概念可以解释电子的行为。电子亲和能和电离能是化学中两个这样的概念。电子亲和力是中性原子或分子获得电子时释放的能量。电子亲和力也可以被称为电子增益焓...
- 发布于 2021-06-30 00:27
- 阅读 ( 656 )
钠(sodium)和钾(potassium)的区别
...异钠(main difference sodium) vs. 钾(potassium) 钠和钾是高活性的化学元素,可以在周期表的第1组中找到。它们是s块元素,因为它们的价电子位于最外层的s轨道。钠和钾都是非常有用的化学元素,因为它们形成多种化合物。然而,钠和...
- 发布于 2021-06-30 09:06
- 阅读 ( 556 )
铑(rhodium)和银(silver)的区别
...金属,具有非常高的熔点和沸点。它的外观与银相似,但化学性质却截然不同。银是一种非常有光泽和贵重的金属,自古就有人知道。铑和银的主要区别在于铑是一种非常硬的金属,而银是一种软金属。 覆盖的关键领域 1.什么...
- 发布于 2021-06-30 11:45
- 阅读 ( 915 )
化学101-主题介绍和索引
欢迎来到化学101的世界!化学是研究物质的学科。像物理学家一样,化学家研究物质的基本性质,他们也探索物质和能量之间的相互作用。化学是一门科学,但它也被用于人类交流和互动、烹饪、医学、工程和许多其他学科。...
- 发布于 2021-09-15 11:49
- 阅读 ( 277 )