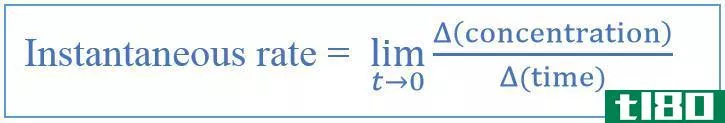反应速率与比速率常数
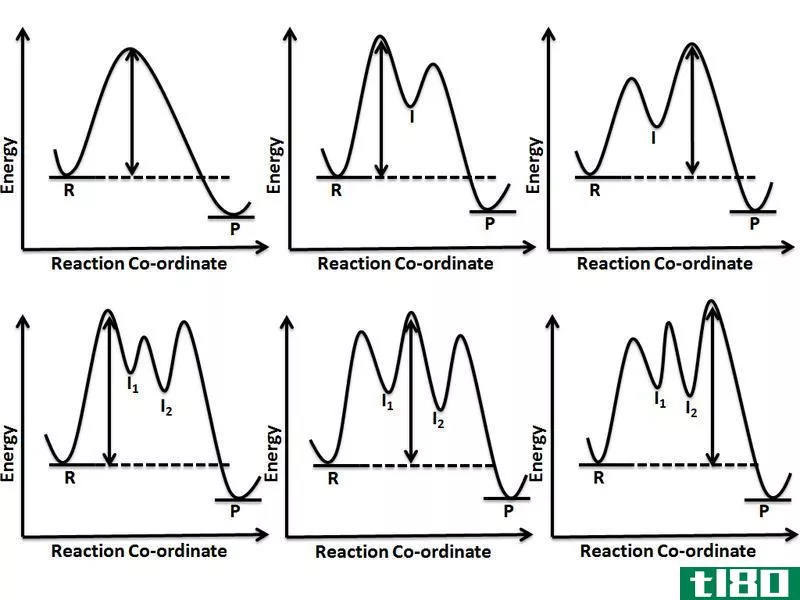
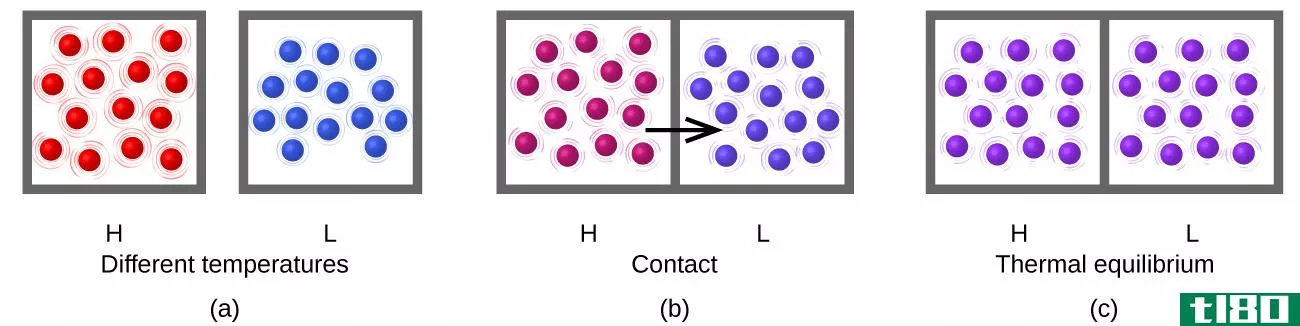
当一个或多个反应物转化为产物时,它们可能经历不同的修饰和能量变化。反应物中的化学键正在断裂,新的键正在形成,生成的产物与反应物完全不同。这种化学修饰被称为化学反应。有许多变量控制着反应。主要是通过研究热力学和动力学,我们可以得出很多关于反应的结论,以及我们如何控制它们。热力学是研究能量转换的学科。它只与能量的平衡状态有关。至于达到平衡的速度有多快,我们无话可说。这个问题是动力学的领域。
反应速率
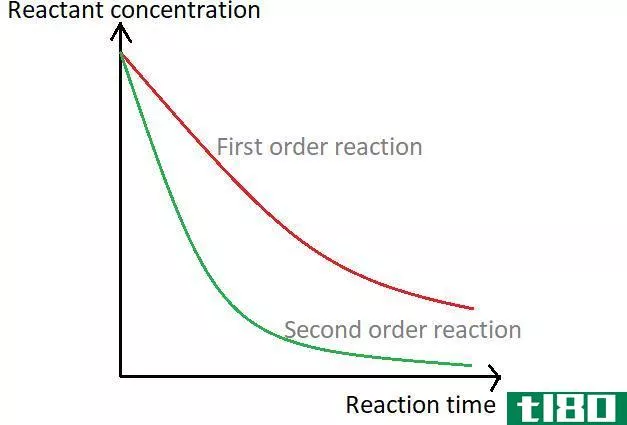
反应速率只是反应速度的指示。因此,它可以被看作是决定反应速度和速度的一个参数。当然,有些反应是非常缓慢的,所以我们甚至看不到反应的发生,除非我们观察很长时间。例如,岩石的化学风化过程是一个非常缓慢的反应,发生在多年。相比之下,一片钾与水的反应非常迅速,因而产生大量热量,被认为是一种剧烈的反应。
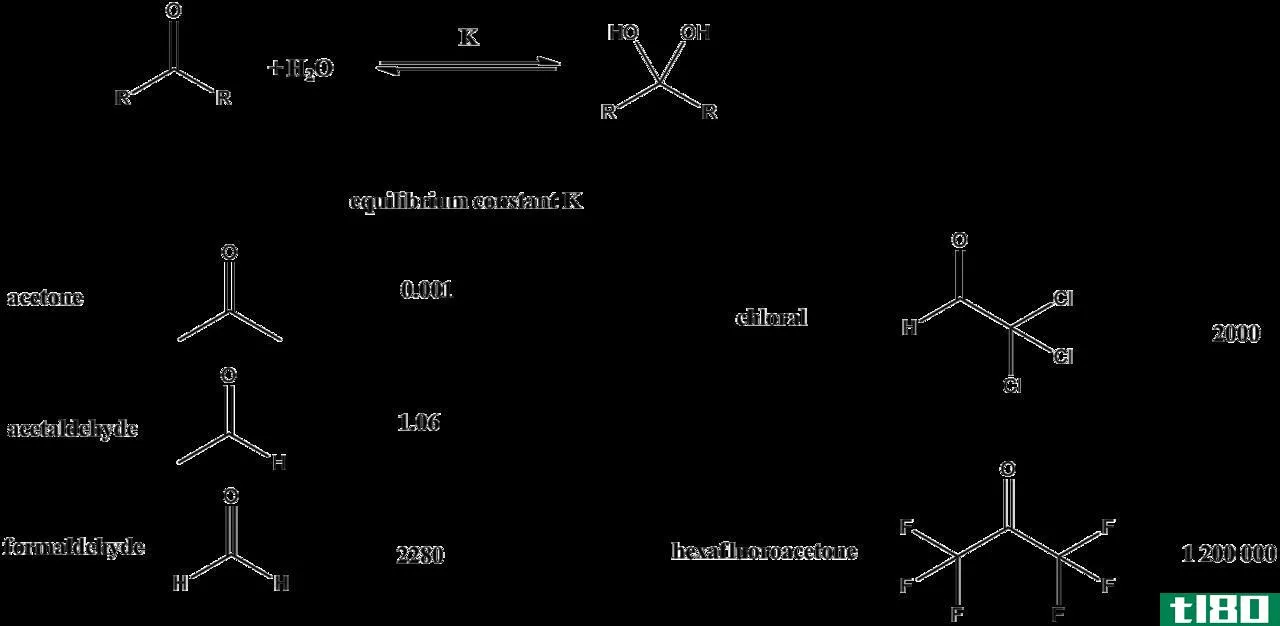
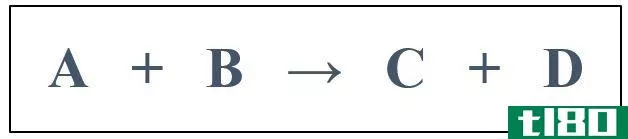
考虑下面的反应,反应物A和B会变成产物C和D。
a a+b b→c c+d d
反应速率可以用两种反应物或产物的任一种来给出。
速率=-(1/a)d[a]/dt=-(1/b)d[b]/dt=-(1/c)d[c]/dt=-(1/d)d[d]/dt
a、 b,c和d是反应物和产物的化学计量系数。对于反应物,速率方程是用负号写的,因为随着反应的进行,产物在消耗。然而,随着产品的增加,它们得到了积极的信号。
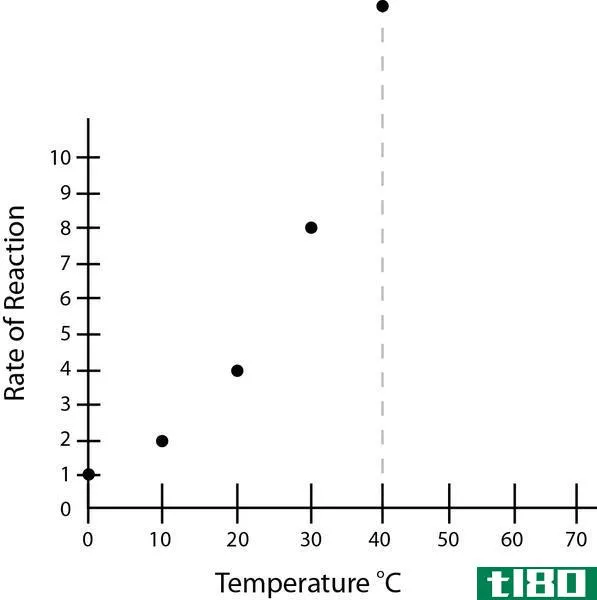
化学动力学是对反应速率的研究,影响反应速度的因素很多。这些因素包括反应物的浓度、催化剂、温度、溶剂效应、pH值,有时还有产物浓度等。这些因素可以被优化以获得最大的反应速率,或者可以调整以控制所需的反应速率。
比速率常数
如果我们写出与上述反应中反应物A有关的速率方程,如下所示。
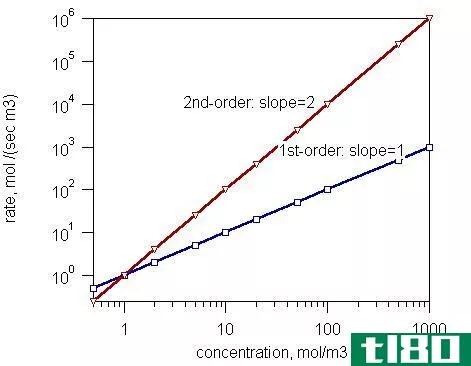
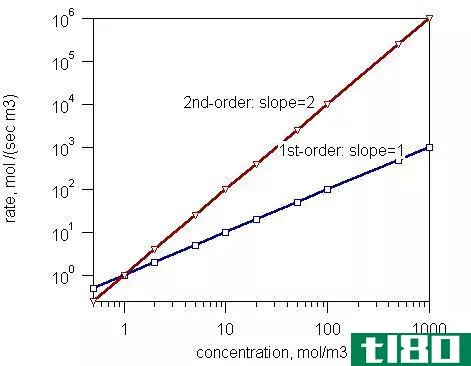
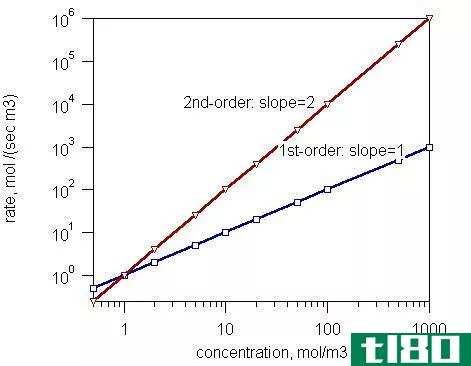
R=-K[A]A[B]B
在这个反应中,k是速率常数。当每一反应物的浓度为单位时,这称为比速率常数,即一摩尔/dm3。它是一个比例常数,它取决于温度。实验结果表明,反应速率和比速率常数均能得到。
| 反应速率和比速率常数有什么区别?•反应速率表示反应转化为产物的速度。比速率常数是比例常数。•比速率常数是反应速率的一部分。•只有比速率常数不能有效地说明反应速度。 |