原子质量单位和原子质量的关键区别在于,原子质量单位是我们用来测量原子质量的单位,而原子质量是特定单个原子的质量。
在早期阶段,表达原子或分子的重量是一个难题。由于原子非常小,我们不能用千克或克甚至微克这样的常规单位来测量它们的质量。因此,科学家们提出了一个新的概念来测量这些。
目录
1. 概述和主要区别
2. 什么是原子质量单位
3. 原子质量是多少
4. 并列比较-原子质量单位与表格形式的原子质量
5. 摘要
什么是原子质量单位(atomic mass unit)?
原子的质量非常小。因此,我们不能用正常的质量单位,如克或公斤来表示它们。因此,我们需要使用另一种叫做原子质量单位(amu)的单位来测量原子质量。一个原子质量单位是C-12同位素质量的十二分之一,即1.66×10−27千克。当我们把一个原子的质量除以碳12同位素质量的十二分之一,我们就可以得到它的相对质量。而且,这个值很小,很容易在计算和其他用途中使用。然而,一般来说,当我们说一个元素的相对原子质量时,我们指的是它们的原子量(因为我们计算时考虑了所有的同位素)。
在使用碳12作为测量原子质量单位的标准之前,人们使用其他元素。例如,首先使用H-1。后来,为了减少错误,他们改变了这一点。之后用更高质量的元素。下一个标准是氧-16。后来,随着氧同位素的发现以及与之相关的其他问题的发现,原子质量单位相对于碳12同位素进行了测量。
什么是原子质量(atomic mass)?
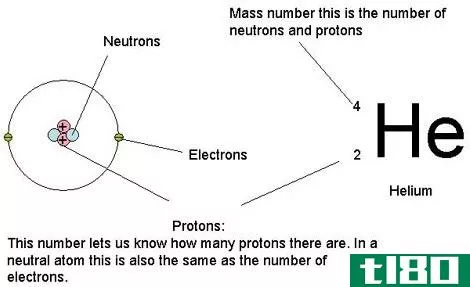
原子主要含有质子、中子和电子。原子质量就是原子的质量。换句话说,它是单个原子中所有中子、质子和电子的质量的集合,特别是当原子不运动时(静止质量)。我们应该取剩余质量,因为根据物理学的基本原理,当原子以非常高的速度运动时,质量会增加。

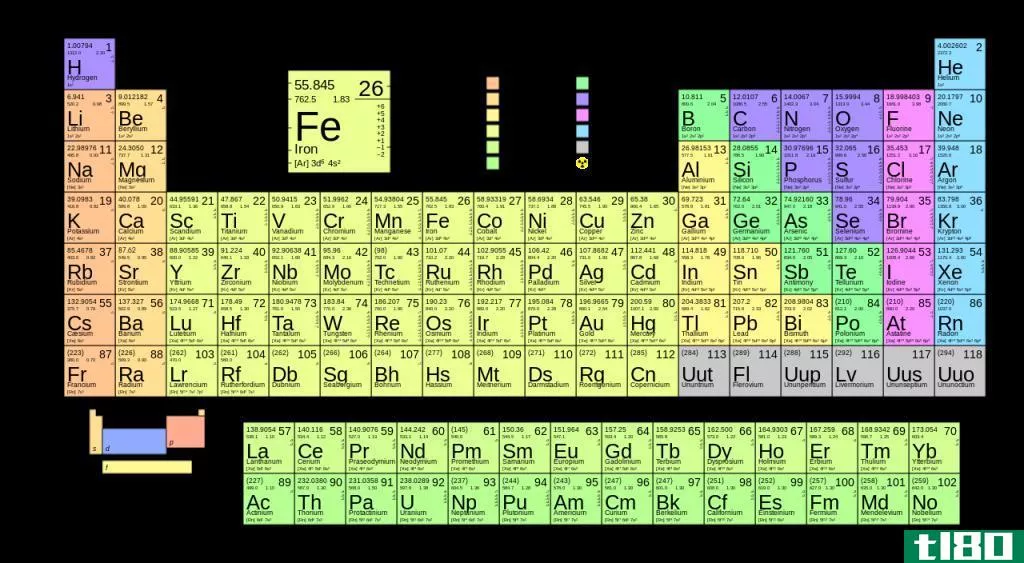
图01:汞的原子质量为200.59 amu
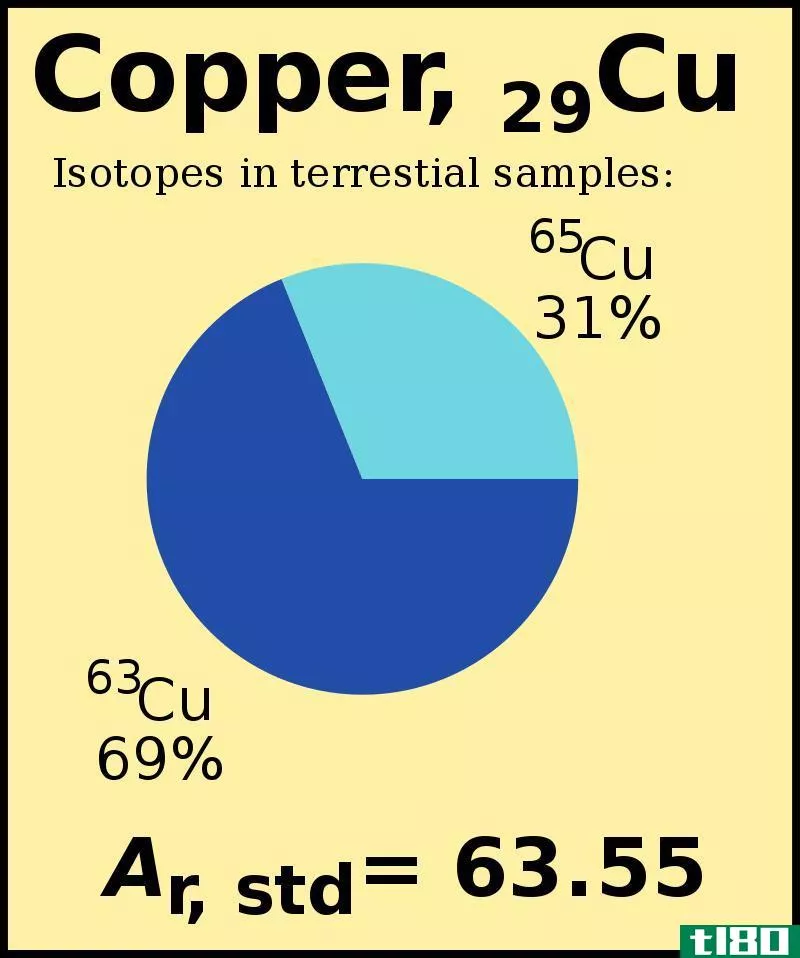
然而,与质子和中子的质量相比,电子的质量要小得多。因此,我们可以说电子对原子质量的贡献较小。元素周期表中的大多数原子都有两种或两种以上的同位素。同位素的不同之处在于它们有不同数量的中子,即使它们有相同的质子和电子量。由于它们的中子量不同,每种同位素的原子质量也不同。整个同位素质量的平均值就是原子量。因此,一个特定同位素的质量就是一个原子中有几个同位素的原子质量。
原子质量单位(atomic mass unit)和原子质量(atomic mass)的区别
原子质量是特定原子的质量(不考虑同位素的平均质量)。原子质量单位是碳12同位素质量的1/12。因此,原子质量单位和原子质量的关键区别在于,原子质量单位是我们用来测量原子质量的单位,而原子质量是特定单个原子的质量。此外,我们可以用原子质量单位来表示其他原子相对于C-12质量的相对质量。
下面关于原子质量单位和原子质量之间差异的信息图总结了所有这些差异。
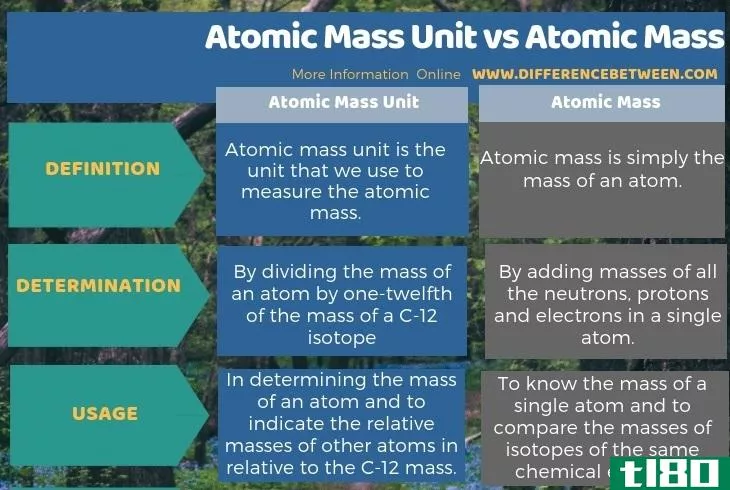
总结 - 原子质量单位(atomic mass unit) vs. 原子质量(atomic mass)
原子质量单位是测量单个原子原子原子质量的单位。原子质量单位和原子质量的关键区别在于,原子质量单位是我们用来测量原子质量的单位,而原子质量是特定单个原子的质量。
引用
1Helmenstine,Anne Marie博士,“原子质量和原子质量数(快速回顾)”,ThoughtCo,2018年6月13日。此处提供