主要区别
Daniell电池与原电池的主要区别在于,Daniell电池是一种用于自发氧化还原反应的电化学电池,由铜和锌的特定电极组成,电解液由硫酸铜和硫酸锌组成,而原电池则是一种电化学电池它的电极可以由各种金属和它们各自作为电解质的盐组成。
丹尼尔细胞(daniell cell) vs. 原电池(galvanic cell)
Daniell电池被认为是一种电化学电池,其中电极是金属特有的,即阴极和阳极仅由铜和锌组成。原电池是一种电化学电池,在这种电池中,这些电极可以由多种金属形成,从而使其对金属的特**降低。在Daniell电池中,为了进行自发的氧化还原反应,铜被用作阴极电极;然而在原电池中,阴极电极可以由任何可以还原的金属组成。
因此,为了在阳极电极上发生氧化,在丹尼尔电池的情况下使用锌电极,这是一种优良的氧化剂。相反,对于原电池,这种阳极电极可以是任何可以被氧化的金属。Daniell电池使用硫酸铜和硫酸锌作为电解液来完成氧化还原反应;然而,在原电池中,这些电解液是每个电极的金属盐,用于在该电化学电池中进行氧化还原反应。
比较图
什么是丹尼尔牢房(the daniell cell)?
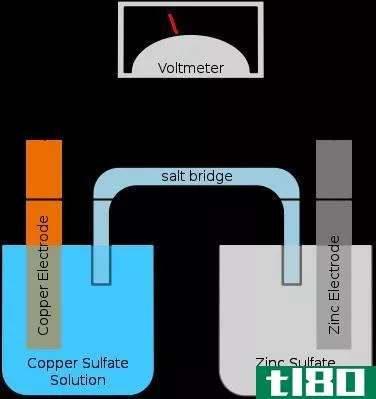
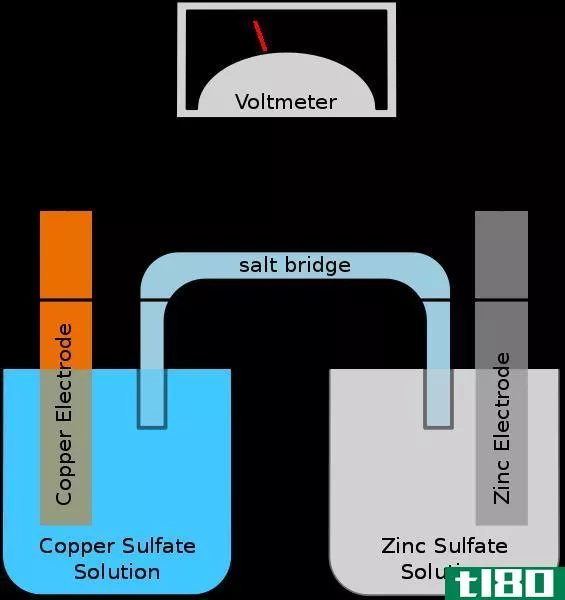
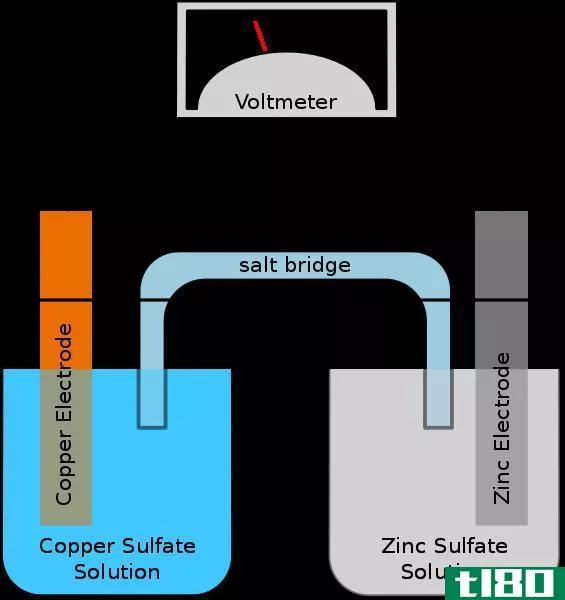
约翰·弗雷德里克·丹尼尔在1836年发明了丹尼尔电池。这些电池在19世纪被用作电力来源。丹尼尔电池是一种电化学电池,其中阴极或阳极等电极是金属专用的,即仅由铜和锌组成。
因此,在这种类型的电化学电池中,铜电极和锌电极分别浸入它们各自的盐中,如硫酸铜和硫酸锌。这些盐在水中溶解时起电解质的作用,它们分离成离子,即当硫酸铜溶解在水中时,铜和硫酸根离子都会释放到溶液中,从而使溶液成为电解液。
对于氧化还原反应,使用电解质完成整个过程。这些离子能通过这种物质的水溶液导电。丹尼尔电池的一半是铜阴极,另一半是锌阳极。阴极铜放入硫酸铜溶液中,锌阳极放入硫酸锌溶液中。
一种能被离子渗透的膜充当一个盐桥,使电子从一种溶液流向另一种水溶液。这种盐桥使电子的流动变得容易,并且填充了一种化合物,这种化合物不会与电池每半侧的其他溶液相互作用。
在真正的丹尼尔电池中,用来分离电解溶液的多孔屏障。这些多孔屏障不允许铜离子进入硫酸锌溶液或锌离子进入硫酸铜溶液。因此,这种屏障不能使它重新充电并限制它的能力——这些溶液用于获得所需的电能。
当电子流动的电路完成后,它就开始充当一个同时发生氧化和还原反应的装置。因此,这些反应在电路中自由移动的电子的帮助下,将化学能转化为电能。由此产生的电能可用于商业目的。
什么是原电池(galvanic cell)?
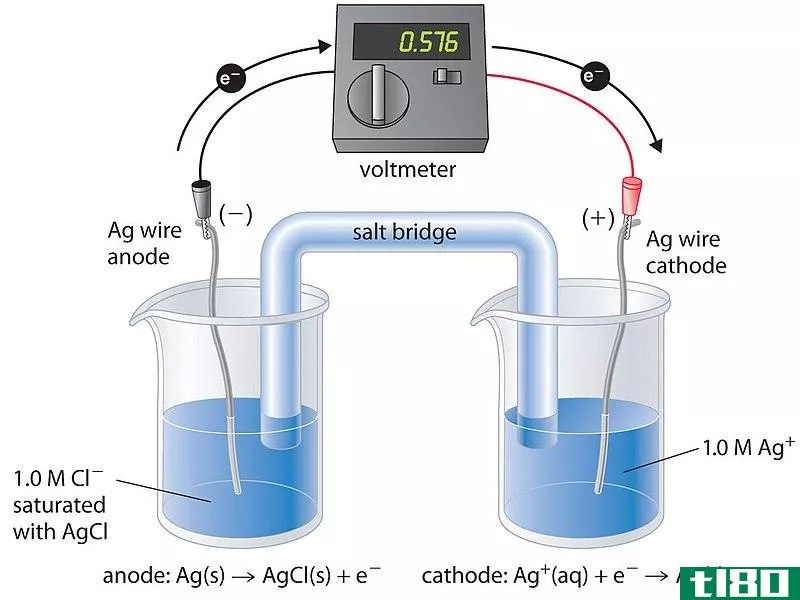
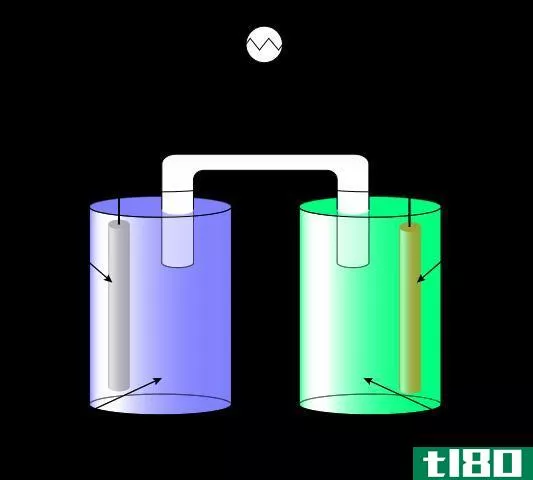
原电池是一种电化学电池,在这种电池中,用于进行氧化还原反应的电极可以由多种金属组成,因此这种电池对金属的特**较低。简单地说,它也被称为伏打电池。这种细胞也由两个半细胞组成。每面都由一个电极和一个电解液组成,电解液浸在电解液中以便电子流动。
与Daniell电池不同,阴极电极可以由原电池中的任何金属组成,但也有其可还原的局限性。在某些情况下,这些电解液可以像在其他容器中那样彼此分开放置,但在另一些情况下,这些电解液被多孔屏障隔开。当这些电解液被完全分离时,含有这种特殊化合物的盐桥用作电子在两种溶液之间移动的桥梁。
与原电池一样,阳极电极可以是任何可以被氧化的金属。因此,在这种类型的电化学电池中,氧化金属和还原金属浸泡在各自的盐中,就像丹尼尔电池一样。这些盐在水中溶解时起电解质的作用,并分离成离子。这些电解液是每个电极上的金属盐,它们可以在电化学电池中进行氧化还原反应。
通过测定阴极和阳极的自发反应能力来选择阴极和阳极。至于要发生的氧化还原反应,半个电池应进行氧化,另一半则进行还原反应。有了合适的电极,这些原电池用于发电,从而使其在商业上可以生产电流。
主要区别
- Daniell电池是一种电化学电池,其中电极由阴极组成,阳极仅由铜和锌制成;另一方面,原电池是指阳极和阴极电极可以由多种金属组成的电化学电池。
- 在Daniell电池中,阳极电极由锌电极组成,锌电极作为氧化剂进行氧化还原反应;相反,对于原电池,该阳极电极可以由任何可被氧化的金属组成。
- Daniell电池使用铜阴极电极进行自发氧化还原反应,因为它是一种优秀的还原剂;另一方面,在原电池中,这种阴极电极可以由任何可以还原的金属组成。
- Daniell电池采用硫酸铜和硫酸锌作为电解液,完成电化学电池并进行氧化还原反应。相反,在原电池中,这些电解液可由每个电极的金属盐组成,以进行氧化还原反应。
结论
Daniell电池是一种以硫酸铜和硫酸锌为电解液,由铜锌电极组成的电化学电池。原电池是一种电化学电池,其电极可以由多种金属及其各自的盐组成。