如何平衡氧化还原反应(balance redox reactions)
半反应法
首先,将方程式分为两个半反应:氧化部分和还原部分。这被称为平衡氧化还原反应的半反应法,或离子-电子法。每个半反应单独平衡,然后将方程式相加,得到平衡的整体反应。我们希望最终平衡方程两边的净电荷和离子数相等。
对于这个例子,让我们考虑在酸性溶液中KMnO4和HI之间的氧化还原反应:
MnO4.-+我-→ 我2.+锰2+

分离反应
将两个半反应分开:
I-→ 我2. MnO4.-→ 锰2+平衡原子
为了平衡每个半反应的原子,首先平衡除H和O之外的所有原子。对于酸性溶液,接下来添加H。
平衡碘原子:
2 I-→ 我2.高锰酸盐反应中的锰已经平衡,所以让我们平衡氧气:
MnO4.-→ 锰2++4小时2.o添加H+以平衡水分子:
MnO4.-+8小时+→ 锰2++4小时2.o两个半反应现在对原子进行了平衡:
MnO4.-+8小时+→ 锰2++4小时2.o平衡费用
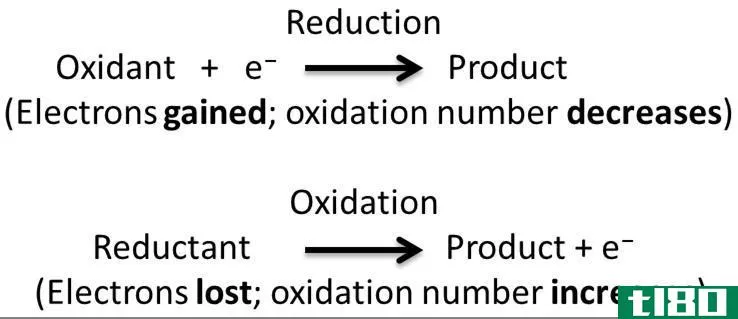
接下来,平衡每个半反应中的电荷,使还原半反应消耗的电子数与氧化半反应提供的电子数相同。这是通过向反应中添加电子来实现的:
2 I-→ 我2.+2e- 5 e-+8小时++mno4.-→ 锰2++4小时2.o接下来,乘以氧化数,使两个半反应具有相同的电子数,并且可以相互抵消:
5(2I-→ 我2.+2e-) 2(5e-+8h++mno4.-→ 锰2++4h2.o)加上一半的反应
现在加上两个半反应:
10 I-→ 5我2.+10 e- 16 H++2 mno4.-+10 e-→ 200万2++8小时2.o这将产生以下等式:
10 I-+10 e-+16小时++2 mno4.-→ 5我2.+200万2++10 e-+8小时2.o通过取消方程式两侧可能出现的电子和H2O、H+和OH-来简化整个方程式:
10 I-+16小时++2 mno4.-→ 5我2.+200万2++8小时2.o检查你的工作
检查数字,确保质量和电荷平衡。在这个例子中,原子现在在化学计量上与反应两侧的+4净电荷平衡。
总之:
- 步骤1:用离子将反应分解为半反应。
- 步骤2:通过向半反应中加入水、氢离子(H+)和羟基离子(OH-),以化学计量法平衡半反应。
- 步骤3:通过向半反应中添加电子来平衡半反应电荷。
- 步骤4:将每个半反应乘以一个常数,使两个反应的电子数相同。
- 步骤5:将两个半反应加在一起。电子应该抵消掉,留下一个平衡的完全氧化还原反应。
- 发表于 2021-10-14 15:36
- 阅读 ( 285 )
- 分类:化学
你可能感兴趣的文章
nabh4(nabh4)和lialh4反应(lialh4 reaction)的区别
...NaBH4与LiAlH4反应的表格形式 5. 摘要 什么是nabh4反应(nabh4 reaction)? NaBH4反应是一种以NaBH4为还原剂的氧化还原反应。化学式NaBH4代表硼氢化钠。它是氢化物亲核物质最常见的来源之一。这种化合物有极性的金属氢键。因此,在氧化...
- 发布于 2020-09-21 16:05
- 阅读 ( 1398 )
复分解(metathesis)和氧化还原反应(redox reactions)的区别
...中和。图01:双置换反应示例 什么是氧化还原反应(redox reaction)? 氧化还原反应是氧化和还原半反应同时发生的一种化学反应。在这个反应中,我们认为氧化和还原是互补的过程。这里,氧化是电子的损失或氧化状态的增加,而...
- 发布于 2020-10-05 04:10
- 阅读 ( 683 )
酸碱滴定法(acid-base titration)和氧化还原滴定(redox titration)的区别
主要区别-酸碱滴定与氧化还原滴定 通常,滴定法用于测定未知溶液(分析物)的浓度。最常用的两种滴定方法是酸碱滴定法和氧化还原滴定法。酸碱滴定和氧化还原滴定的关键区别在于滴定过程中滴定剂和被分析物之间发生...
- 发布于 2020-10-06 00:15
- 阅读 ( 661 )
歧化(disproportionation)和氧化还原(redox)的区别
歧化和氧化还原的关键区别在于,在歧化反应中,同一反应物经历氧化和还原。氧化和氧化反应通常会发生两种不同的氧化还原反应。 此外,歧化反应是一个分子转化为两个或两个以上不同产物的化学反应,而氧化还原反应...
- 发布于 2020-10-16 04:09
- 阅读 ( 356 )
羟醛缩合(aldol condensation)和cannizzaro反应(cannizzaro reaction)的区别
...应是形成碳-碳键的好方法。 什么是cannizzaro反应(cannizzaro reaction)? Cannizzaro反应是一种有机氧化还原反应,其中两个分子发生歧化反应,生成一个伯醇和一个羧酸。在这个反应中,不平衡是一个碱诱导反应。反应如下: 在这里...
- 发布于 2020-10-17 01:12
- 阅读 ( 561 )
氧化数法(oxidation number method)和半反应法(half reaction method)的区别
...衡的氧化还原反应:Zn+2HCl→ZnCl2+H2 什么是半反应法(half reaction method)? 半反应法是一种利用两个平行的半反应来平衡氧化还原反应的方法:氧化半反应和还原半反应。在氧化还原反应中,一种反应物起氧化剂的作用,氧化另一种...
- 发布于 2020-10-19 09:49
- 阅读 ( 844 )
平衡方程(balanced equation)和净离子方程(net ionic equation)的区别
...e behavior of a particular system. By writing the correct equation for the reaction, one can get an idea about the changes of different species in that system. For simple reacti*** such as dissolving of NaCl in water, the equation can be written easily by predicting the possible products of that rea...
- 发布于 2020-10-20 16:30
- 阅读 ( 735 )
结合(combination)和分解反应(decomposition reaction)的区别
结合(combination)和分解反应(decomposition reaction)的区别 化学反应是将一种或多种化合物转化为一种或多种不同的产物,从而改变化合物的特性。化学反应的起始物质称为反应物,生成的化合物称为产物。在化学反应过程中,由于...
- 发布于 2020-10-23 20:07
- 阅读 ( 344 )
分子内氧化还原(intramolecular redox)和不相称氧化还原反应(disproportionate redox reaction)的区别
...intramolecular redox)和不相称氧化还原反应(disproportionate redox reaction)的区别 氧化还原反应是氧化半反应和还原半反应平行发生的化学反应。分子内氧化还原和不相称氧化还原反应的关键区别在于,当两种不同物质的分子相互反应时...
- 发布于 2021-03-04 19:20
- 阅读 ( 446 )
氧化还原(redox)和非还原反应(nonredox reactions)的区别
氧化还原反应和非氧化还原反应的关键区别在于,在氧化还原反应中,某些化学元素的氧化状态会从一种状态改变到另一种状态,而在非氧化还原反应中,化学元素的氧化状态不会改变。 氧化还原和非氧化还原反应是两种主...
- 发布于 2021-03-04 19:49
- 阅读 ( 640 )