范德华相互作用与疏水相互作用的关键区别在于,范德华相互作用是非极性分子之间的吸引力,而疏水相互作用是水分子与其他分子之间的排斥力。
化学键主要有四种类型:共价键、离子键、氢键和范德华相互作用。除此之外,我们还可以观察到水分子与其他分子之间的相互作用力,即亲水相互作用和疏水相互作用。
目录
1. 概述和主要区别
2. 范德瓦尔斯的相互作用是什么
3. 什么是疏水相互作用
4. 并列比较——范德华与疏水相互作用的表格形式
5. 摘要
什么是范德华相互作用(van der waals interacti***)?
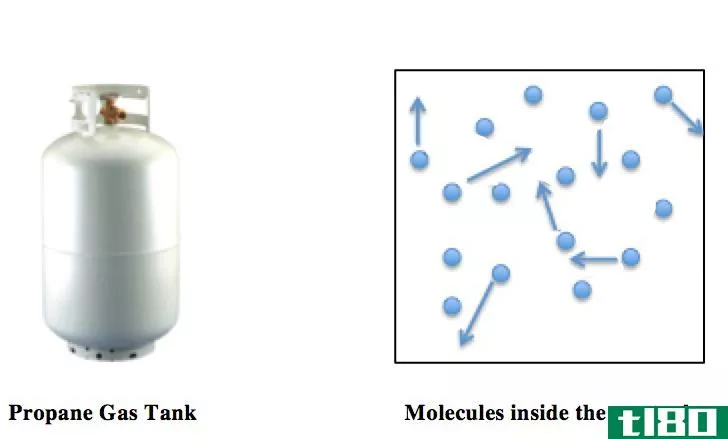
范德华相互作用是非极性分子之间的化学键。这些相互作用是一种非共价键。它们是两个非极性分子中两个原子之间的弱引力。范德华相互作用是一种诱导吸引或排斥,它是由附近粒子的波动极化的关联引起的。
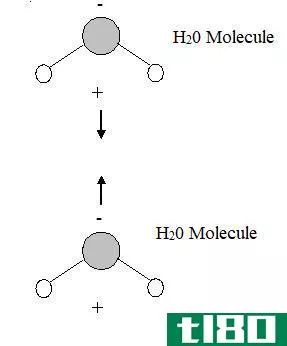
图01:范德华相互作用
范德华力主要发生在对称分子之间,如氢分子和二氧化碳分子。两个相反的电荷之间形成相互作用:正电荷和负电荷。在非极性分子中,不存在电荷分离,因此这些分子往往带有诱导电荷,从而形成感应偶极子。当两个分子彼此靠近时,一个分子的电子云排斥另一个分子的电子云,在该分子上施加轻微的正电荷。然后这个正电荷吸引着附近分子的带负电的电子云。这是一种弱的相互作用力。
什么是疏水相互作用(hydrophobic interacti***)?
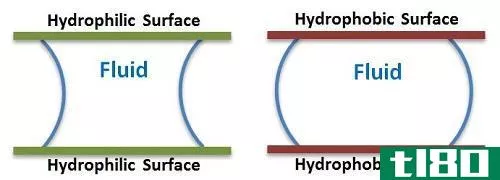
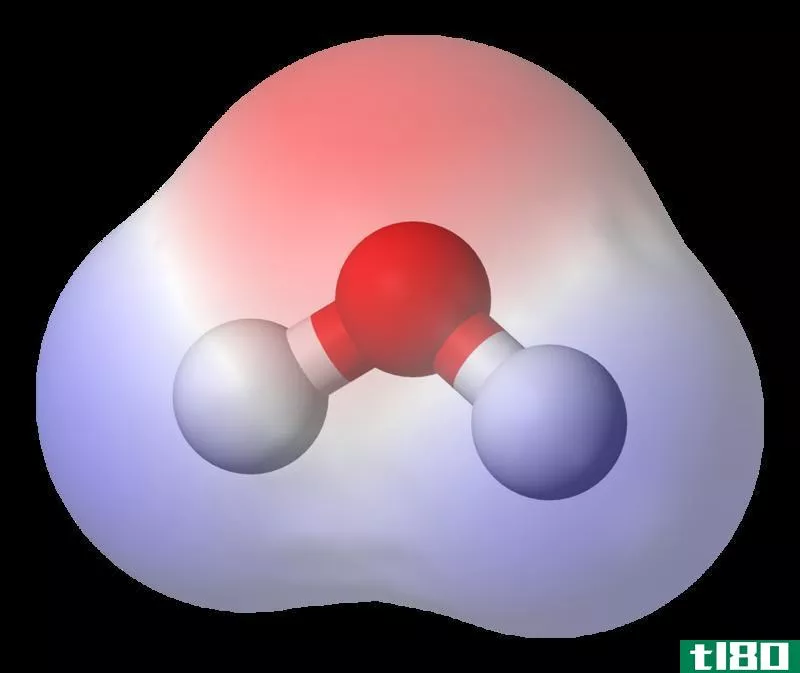
疏水相互作用是水分子与其它物质之间的排斥力。它是与亲水相互作用(水分子与其他物质之间的吸引力)相反的相互作用类型。在这个术语中,hydro的意思是“水”,“恐怖”的意思是“恐惧”。因此,我们可以将不喜欢水的物质命名为疏水性物质。这些物质排斥水分子。一般来说,非极性分子表现出这种相互作用是因为水分子是极性的。换句话说,疏水性物质倾向于吸引或与非极性物质(如油和己烷)相互作用或溶解。

图01:叶子是疏水的,所以水滴形成球形,以减少与表面的接触。
有时,疏水性物质被称为亲脂物质,因为这些物质会吸引脂质或脂肪成分。当疏水性物质加入水中时,这种物质的分子往往通过相互结合而形成团块。这使得疏水性溶剂在从水或极性溶液中分离非极性化合物时非常重要。
范德瓦尔斯(van der waals)和疏水相互作用(hydrophobic interacti***)的区别
范德华力和疏水相互作用是两种不同类型的化学键。范德华相互作用与疏水相互作用的关键区别在于,范德华相互作用是非极性分子之间的吸引力,而疏水相互作用是水分子与其他分子之间的排斥力。在范德华相互作用中,一个分子得到诱导正电荷,另一个分子得到诱导负电荷,而疏水相互作用中没有电荷分离。
下面是范德华和疏水相互作用之间的差异的表格形式的总结。
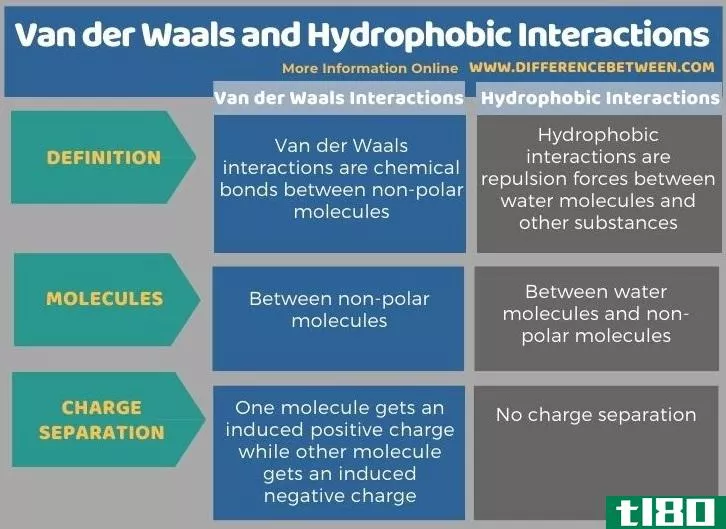
总结 - 范德瓦尔斯(van der waals) vs. 疏水相互作用(hydrophobic interacti***)
范德华力和疏水相互作用是两种不同类型的化学键。范德华相互作用与疏水相互作用的关键区别在于,范德华相互作用是非极性分子之间的吸引力,而疏水相互作用是水分子与其他分子之间的排斥力。
引用
1“范德瓦尔斯力量”,化学剧本,歌词,2020年8月15日,可在这里查阅。
2“叶子上的水滴”由Flickr用户tanakawo通过Comm*** Wikimedia拍摄