氮与磷
氮和磷是元素周期表中的V族元素。它们具有相同的价壳层电子,在合成化合物时具有一些相似的性质。它们都具有ns2np3价壳层电子构型。
氮气
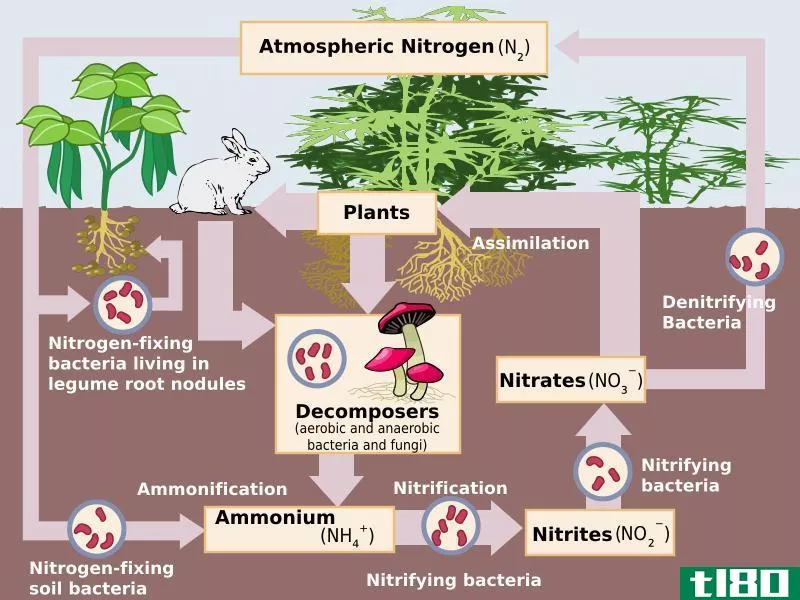
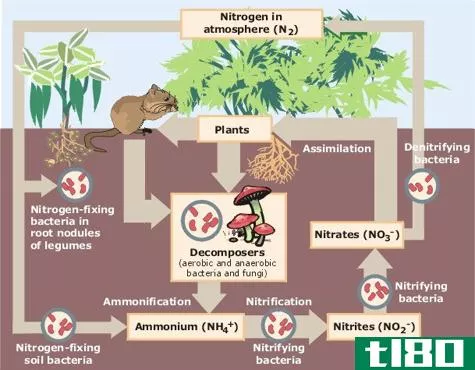
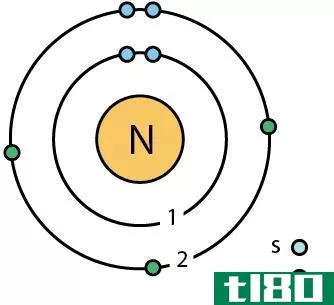
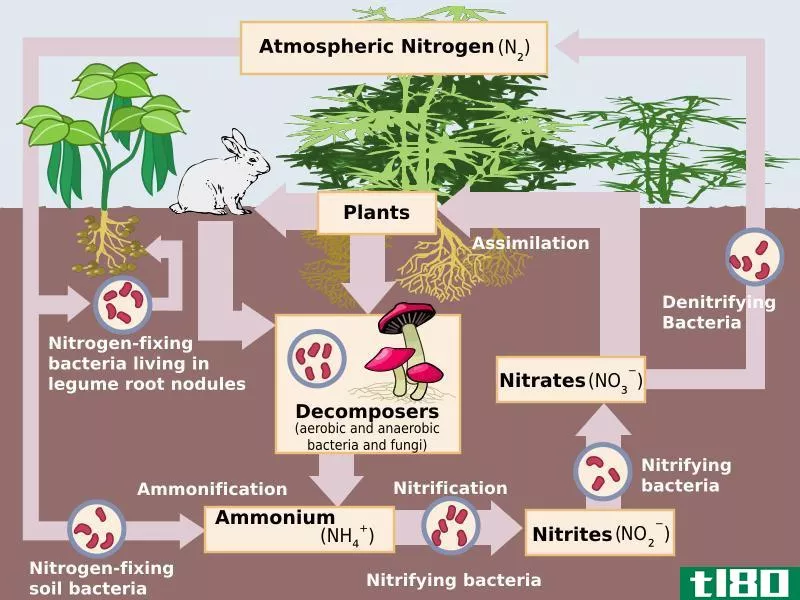
氮是我们体内第四丰富的元素。它在周期表的第15组,原子序数为7。氮是一种非金属元素,其电子构型为1s2 2s2 2p3。p轨道是半满的,这使氮有能力再吸收三个电子,以获得稳定的稀有气体结构。因此,氮是三价的。两个氮原子可以在它们之间形成三键,每个原子共享三个电子。这种双原子分子在室温下处于气相,形成无色、无味、无味的惰性气体。氮气是不可燃气体,因此,不支持燃烧。这是地球大气中含量最高的气体(约78%)。当然,氮有两种同位素,N-14和N-15。N-14的丰度较高,为99.6%。在很低的温度下,氮气变成液态。它的外观与水相似,但密度低于水。
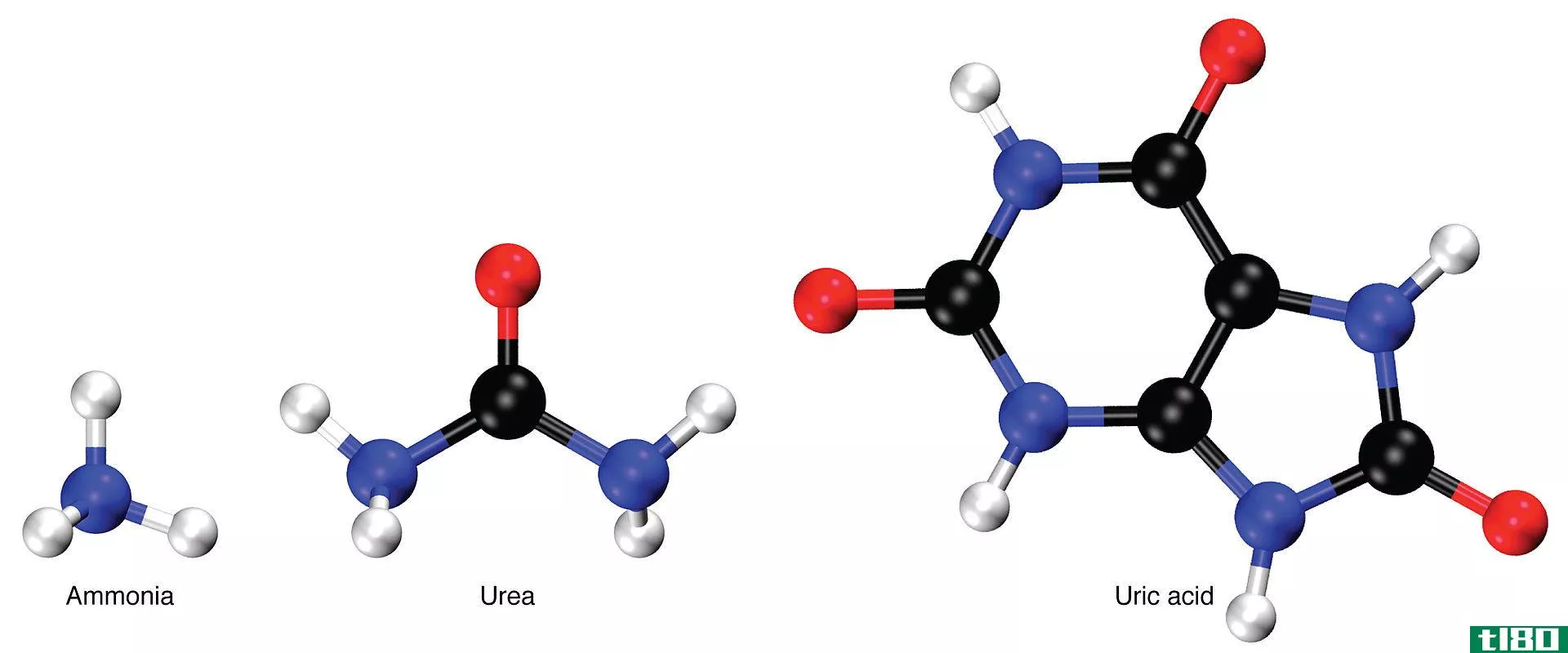
氮广泛应用于化学工业,是生物体所需的重要成分。氮最重要的商业用途是用作氨、硝酸、尿素和其他氮化合物生产的原料。氮是植物生长所需的主要元素之一。氮气也用于需要惰性环境的地方,特别是在进行化学反应时。液态氮用于立即冻结物体,并在各种设备(如计算机)中用作冷却剂。
磷
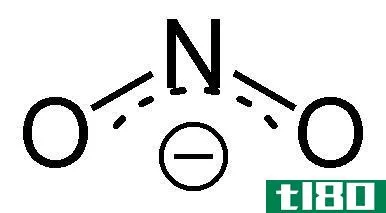
磷是元素周期表中的第15种元素,符号为P。它与氮一起属于第15族,分子量为31 g mol-1。磷的电子构型为1s2 2s2 2p6 3s2 3p3。它是一个多价原子,可以形成+3,+5阳离子。磷有几种同位素,但P-31很常见,丰度为100%。P-32和P-33同位素具有放射性,可以释放出纯β粒子。磷是非常活泼的,因此,不能以单个原子的形式存在。自然界中的磷有两种主要形式:白磷和红磷。白磷有四个四面体排列的磷原子。白磷是一种淡黄色透明固体。它具有高度的反应性和剧毒性。红磷以聚合物的形式存在,加热白磷,就可以得到红磷。除了白磷和红磷,还有另一种被称为黑磷的类型,它的结构类似于石墨。
| 氮和磷的区别是什么?•氮的原子序数为7,磷的原子序数为15。•氮处于第二周期,而磷处于第三周期。•天然氮以双原子气体的形式存在,而磷则以固态形式存在。•磷具有形成键的能力,直到其价壳层中有超过一个八位态。但是氮形成键直到八位体被填满。 |