关键区别——局部作用与极化
局部作用和极化这两个术语被用来命名电池中的两种缺陷。这些都存在于简单的电池中。这些缺陷降低了这些电池(或电池)的实用价值和性能。电池的局部作用是由于局部电流在板的不同部分之间流动而造成的电池内部损耗。这些局部电流是由化学反应产生的。极化是由于氢气在正极周围**而导致电池反应的终止。局部作用和极化之间的关键区别在于,使用纯锌可以使局部作用最小化,而使用锰氧化物等去极化剂可以使极化最小化
目录
1. 概述和主要区别
2. 什么是地方行动
3. 什么是两极分化
4. 并列比较-局部作用与极化的表格形式
5. 摘要
什么是地方行动(local action)?
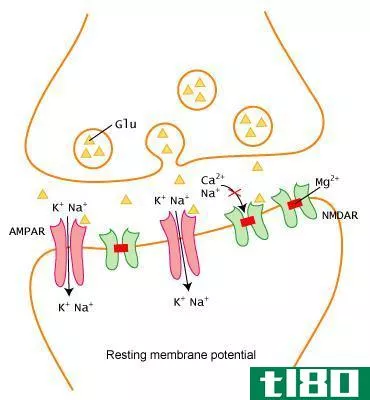
电池的局部作用是由于从同一电极流出或流入同一电极的电流而使电池劣化。电池包含一个或多个电化学电池。这些电化学电池与电力设备有外部连接。蓄电池有两个端子:正极或负极,负极或负极。电池把化学能转换成电能。
电池内有电极和电解质。电解液中含有保持蓄电池内部持续电流流动所需的阴离子和阳离子。当电解液提供电子来产生电流时,就会发生氧化还原反应。但是,有时电池内部会出现某些缺陷,例如降低电池的性能和价值。局部行动就是这样一个缺陷。
局部作用是指由于杂质的存在,即使电池没有连接到外部电源设备上,电池也会释放电流。这些杂质会在电极的某些部分之间产生电位差。它是一种自放电。
例如,当使用锌电极时,可能会嵌入铁和铅等杂质。与锌电极和锌电极相比,这些杂质可以充当正极。然后,当电池不使用时,电流通过这些电极,最终导致电池劣化。

图01:电池
使用一个没有杂质的纯锌电极可以使局部作用最小化。但这是一个非常昂贵的选择。因此,在锌与汞合金化生产锌汞合金时,使用一种更便宜的选择。这个过程叫做合并。
什么是极化(polarization)?
极化是简单电池中由于氢气在正极周围积聚而产生的一种缺陷。在简单的细胞中,氢气是细胞内发生化学反应的结果。当氢气**在正极周围时,最终导致正极与电解溶液绝缘。这个过程被称为极化。
电池的极化降低了电池的实用价值和性能。因此,它被认为是细胞缺陷。为了减小极化,可以使用去极化器,因为它可以与电池中产生的氢气发生反应。一种常见的去极化剂是氧化锰。它与氢气反应生成水作为副产品。
地方行动(local action)和极化(polarization)的区别
| 局部作用与极化 | |
| 电池的局部作用是由于从同一电极流出或流入同一电极的电流而使电池劣化。 | 极化是简单电池中由于氢气在正极周围积聚而产生的一种缺陷。 |
| 过程 | |
| 在局部作用下,嵌入在锌电极中的杂质可以充当正极,并在锌和该正极之间产生电流。 | 在电池内部的化学反应中产生的氢气会**在电极周围,造成绝缘。 |
| 原因 | |
| 由电极中的杂质如铁和铅引起。 | 由化学反应产生的氢气引起的。 |
| 最小化 | |
| 可使用纯锌将其最小化。 | 可使用诸如氧化锰等去极化剂将其最小化。 |
总结 - 地方行动(local action) vs. 极化(polarization)
局部作用和极化是电池组讨论的两种缺陷。局部作用和极化的区别在于,使用诸如氧化锰这样的去极化剂可以使局部作用最小化,而使用纯锌可以使极化最小化。
引用
1.“简单电池的缺陷。”简单电池的缺陷~,可在此处查阅2.“电池(电)。”维基百科,维基媒体基金会,2018年2月22日。此处提供
2.“电池(电)。”维基百科,维基媒体基金会,2018年2月22日。