状态函数(state function)和路径函数(path function)的区别
热力学是物理化学的一个重要分支,它揭示了不同形式的能量和功之间的热化学关系。有四个热力学定律用于描述热力学系统的行为。状态函数和路径函数是表示系统不同热力学性质的两种方式。状态函数与路径函数的关键区别在于,状态函数不依赖于路径或进程,而路径函数依赖于路径或进程。因此状态函数和路径函数是对立的。
目录
1. 概述和主要区别
2. 什么是状态函数
3. 什么是路径函数
4. 状态函数与路径函数的相似性
5. 并列比较-状态函数与路径函数的表格形式
6. 摘要
什么是状态函数(state function)?
状态函数是一个热力学术语,用于命名其值不依赖于达到该特定值的路径的属性。状态函数也称为点函数。状态函数只依赖于热力学系统的当前状态及其初始状态(与路径无关)。热力学系统的状态函数描述了该系统的平衡状态,而不管该系统是如何达到该状态的。
状态函数示例
- Mass
- Energy – enthalpy, internal energy, Gibbs free energy, etc.
- Entropy
- Pressure
- Temperature
- Volume
- Chemical composition
- Altitude
一个状态函数取决于三件事:属性、初始值和最终值。焓是一个状态函数。它可以作为数学表达式给出,如下所示。
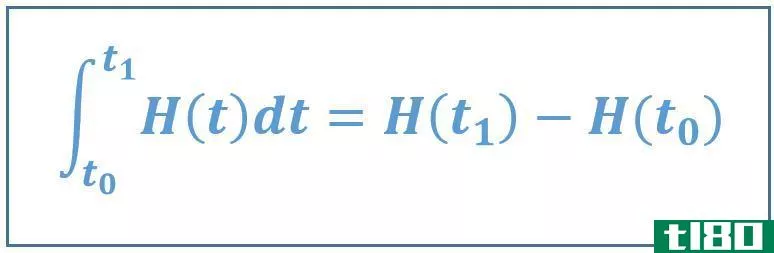
式中,t1为终态,t0为初始态,h为系统的焓。
什么是路径函数(path function)?
路径函数是一个热力学术语,用于命名一个属性,其值取决于达到该特定值的路径。换句话说,路径函数依赖于从初始状态到最终状态所采用的路径。路径函数也称为过程函数。
路径函数为不同路径提供不同的值。因此,路径函数根据路径具有可变值。因此,在数学上表示路径函数时,需要多个积分和极限来积分路径函数。
路径函数示例
- Mechanical work
- Heat
- Arc length
内能由下式给出:
∆U=q+w
式中∆U是内能的变化,q是热量,w是机械功。内能是状态函数,而热和功是路径函数。
状态函数(state function)和路径函数(path function)的共同点
- 两者都是热力学中描述的函数。
- 二者都是热力学系统的性质。
状态函数(state function)和路径函数(path function)的区别
| 状态函数与路径函数 | |
| 状态函数是一个热力学术语,用于命名其值不依赖于达到该特定值的路径的属性。 | 路径函数是一个热力学术语,用于命名一个属性,其值取决于达到该特定值的路径。 |
| 其他名称 | |
| 状态函数也称为点函数。 | 路径函数也称为过程函数。 |
| 过程 | |
| 状态函数不依赖于路径或进程。 | 路径函数依赖于路径或进程。 |
| 集成 | |
| 状态函数可以用系统热力学性质的初始值和最终值进行积分。 | 路径函数需要多重积分和积分极限来积分。 |
| 价值观 | |
| 无论步骤数是多少,state函数的值都保持不变。 | 单步过程与多步过程的路径函数值不同。 |
| 示例 | |
| 状态函数包括熵、焓、质量、体积、温度等。 | 路径函数包括热功和机械功。 |
总结 - 状态函数(state function) vs. 路径函数(path function)
状态函数和路径函数是给出热力学系统不同性质的两种形式的热力学表达式。这些术语彼此不同,状态函数和路径函数的关键区别在于状态函数不依赖于路径或进程,而路径函数依赖于路径或进程。