硫酸(sulfuric acid)和亚硫酸(sulfurous acid)的区别
硫酸(H2SO4)和亚硫酸(H2SO3)是两种以硫、氢和氧为元素的无机酸。硫酸和亚硫酸的主要区别在于硫的氧化数。此外,当我们比较两种酸的酸度时,硫酸的酸性比亚硫酸强。换句话说,硫酸是一种很强的酸,而亚硫酸相对较弱。
什么是硫酸(sulfuric acid)?
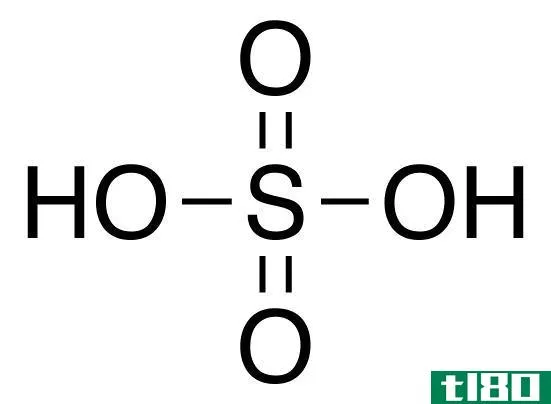
硫酸是一种非常强的双质子矿物酸,与水以任何比例完全混溶。在水中溶解硫酸是一种放热反应。它是一种腐蚀性和有害的液体,会对皮肤或眼睛造成许多伤害,如酸烧伤。这包括短期和长期影响,取决于酸的浓度和接触时间。硫酸具有很强的腐蚀性是由几个因素造成的:酸度、氧化能力、浓溶液引起的脱水以及放热反应释放的热量。
什么是亚硫酸(sulfurous acid)?
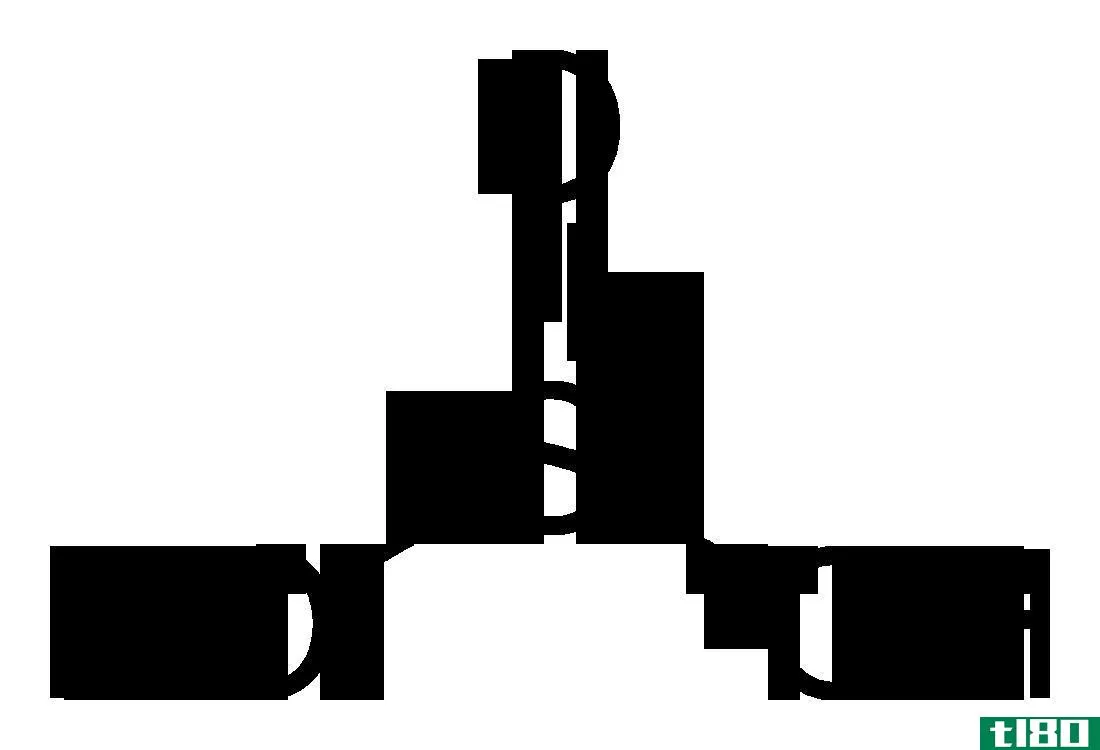
亚硫酸的化学式为H2SO3,其中硫的氧化数等于+4。它是一种透明、无色、弱而不稳定的酸。有一股刺鼻的硫磺味。当二氧化硫溶解在水中时,它就形成了,而纯无水形式的亚硫酸从未被分离或检测到。亚硫酸很快分解分解成化学成分,因为它是热力学不稳定的。分解反应是,
H2SO3(aq)→H2O(l)+SO2(g)
硫酸(sulfuric acid)和亚硫酸(sulfurous acid)的区别
结构及化学式:
硫酸:硫酸的化学式为H2SO4,其中硫的氧化数为+6。这种分子的几何结构是四面体的。
亚硫酸:硫酸的化学式为H2SO3,其中硫的氧化数为+4。这种分子的几何结构是三角锥体。
酸度:
硫酸:硫酸是最强的酸之一,是一种二元酸。硫酸的酸离解常数为:K1=2.4×106(强酸),K2=1.0×10−2。
亚硫酸:亚硫酸在pH标度上的酸度等于1.5。它不被认为是一种很强的酸,但它也不是一种太弱的酸。
属性:
硫酸:硫酸除具有酸性外,还具有氧化和还原特性。因此,它与金属和非金属都发生反应;它和其他酸一样,与金属发生反应,产生氢气和相应的金属盐。
与金属的反应:
铁(s)+H2SO4(aq)→H2(g)+FeSO4(aq)
Cu+2 H2SO4→SO2+2 H2O+SO42–+Cu2+
与非金属的反应:
二氧化硫+二氧化硫
S+2 H2SO4→3 SO2+2 H2O
亚硫酸:亚硫酸在无水硫酸中不存在。然而,有证据表明含硫分子存在于气相中。与硫酸不同,亚硫酸的化学反应非常有限。
CaCO3(s)+H2SO3(aq)→CO2(g)+H2O(l)+CaSO3(aq)
使用:
硫酸:硫酸在世界各地广泛应用于各个行业。例如,它被用来生产肥料、**、纸张、洗涤剂、染料和着色剂。此外,它在化学合成、表面处理、石油和纺织工业中也非常重要。
亚硫酸:亚硫酸是一种很强的还原剂。它具有一定的漂白性能,可用作漂白剂。
Image Courtesy:
1. Sulfuric acid chemical structure By DMacks (Own work) [Public domain], via Wikimedia Comm***















