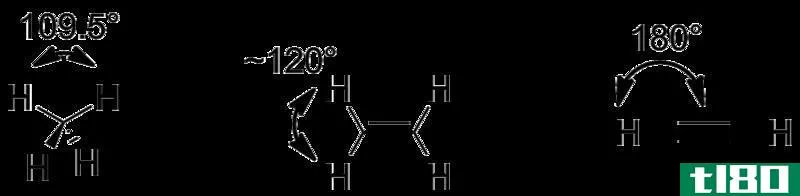
烷烃(alkanes)和烯烃(alkenes)的区别
烷烃和烯烃是分子结构中含有碳和氢的两种烃族。烷烃和烯烃的主要区别在于它们的化学结构;烷烃是饱和烃,分子式一般为CnH2n+2,烯烃被称为不饱和烃,因为它们在两个碳原子之间含有双键。它们的分子式是CnH2n。
什么是烷烃(alkanes)?
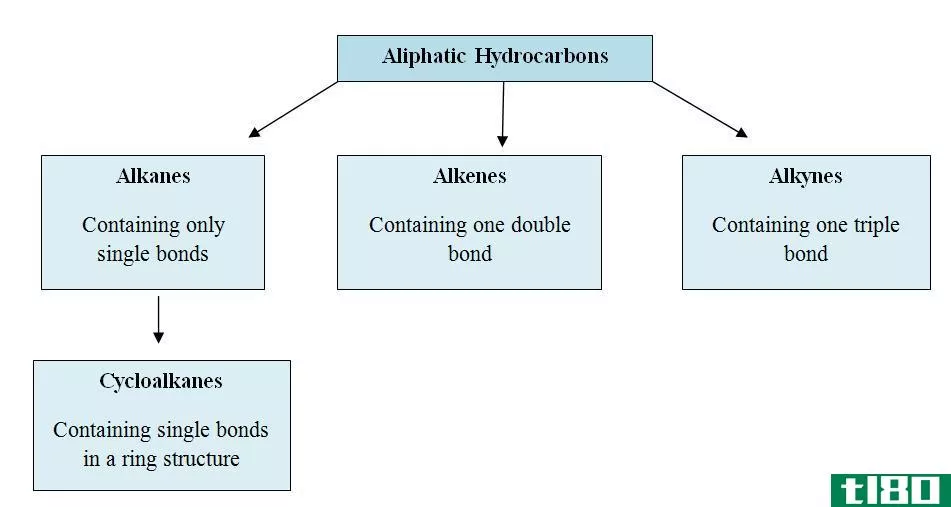
Alkanes contain only single bonds between Carbon and hydrogen atoms (C-C bonds and C-H bonds). Therefore, they are called “saturated hydrocarb***”. According to the orbital hybridization model, all the carbon atoms in Alkenes have the SP3 hybridization. They form sigma bonds with Hydrogen atoms, and the resulting molecule has the geometry of a tetrahedron. Alkanes can be sub-divided into two groups according to their molecular arrangements; acyclic alkanes (CnH2n.+2) and cyclic alkanes (CnH2n).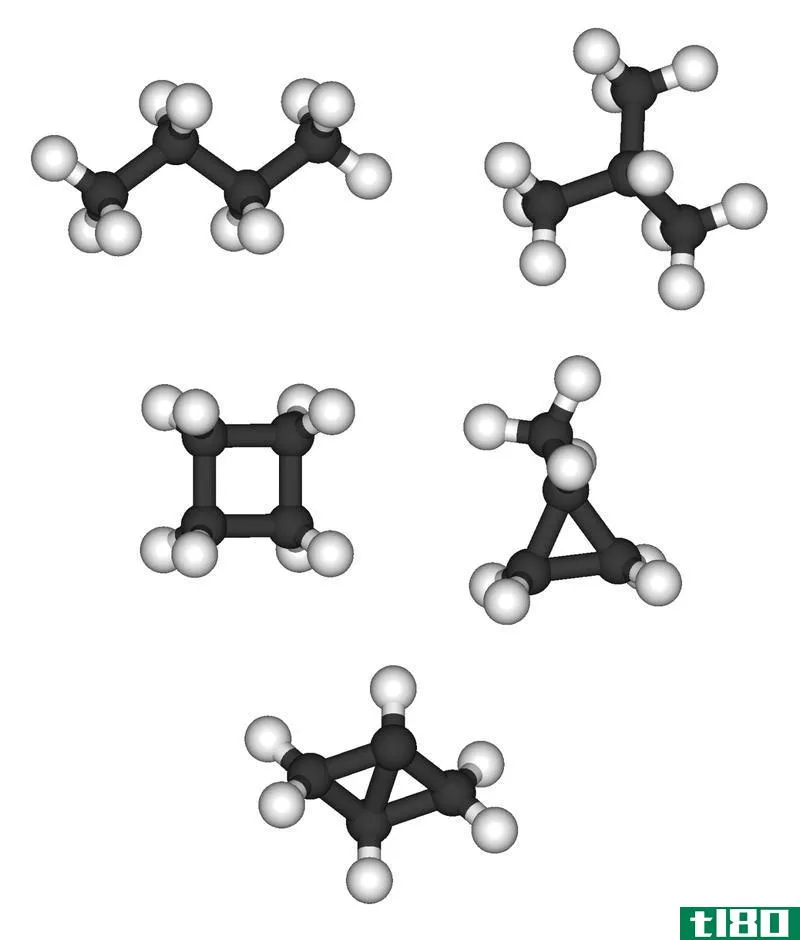
什么是烯烃(alkenes)?
Alkenes are the hydrocarb***, containing a Carbon-Carbon (C=C) double bond. “Olefins” is the old name used to refer to the alkene family. The **allest member of this family is ethane (C2H4); it was called olefiant gas (In Latin: ‘oleum’ means ‘oil’ + ‘facere’ means ‘to make’) in early days. This is because the reaction between C2H4 and Chlorine gives C2H2Cl2, oil.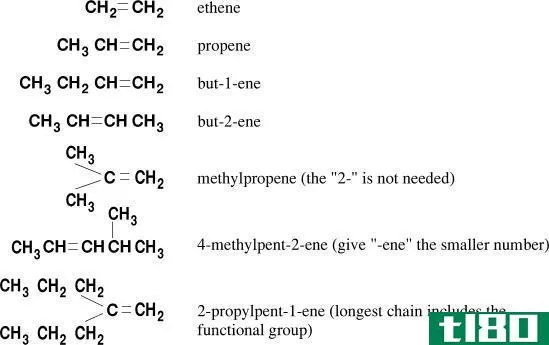
烷烃(alkanes)和烯烃(alkenes)的区别
烷烃和烯烃的化学结构
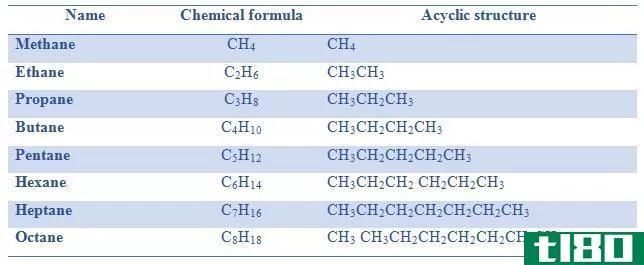
烷烃:烷烃分子式一般为CnH2n+2。甲烷(CH4)是最小的烷烃。
| 姓名 | 化学式 | 无环结构 |
| 甲烷 | 甲烷 | 甲烷 |
| 乙烷 | C2H6型 | CH3CH3 |
| 丙烷 | C3H8型 | CH3CH2CH3 |
| 丁烷 | C4H10型 | CH3CH2CH2CH3 |
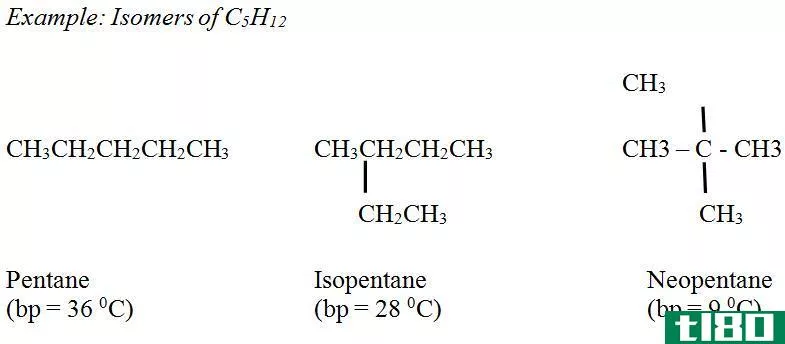
| 戊烷 | C5H12型 | CH3CH2CH2CH2CH3 |
| 己烷 | C6H14型 | CH3CH2CH2 CH2CH2CH3 |
| 庚烷 | C7H16型 | CH3CH2CH2CH2CH2CH2CH2CH2CH3 |
| 辛烷值 | C8H18型 | CH3 CH3CH2CH2CH2CH2CH3CH3 |
烯烃:烯烃的一般化学式为CnH2n。烯烃被认为是不饱和烃,因为它们不包含碳氢分子所能拥有的最大数量的氢原子。
| 姓名 | 化学式 | 结构 |
| 乙烯 | C2H4型 | CH2=CH2 |
| 丙烯 | C3H6型 | CH3CH=CH2 |
| 丁烯 | C4H8型 | CH2=CHCH2CH3,CH3CH=CHCH3 |
| 戊烯 | C5H10型 | CH2=CH2CH2CH3,CH3CH=CH2CH3 |
| 己烯 | C6H12型 | CH2CH3 CH2CH3=CH2CH |
| 庚烯 | C7H14型 | CH=CH2CH2CH2CH2CH3CH3CH=CH2CH2CH2CH2CH3 |
烷烃和烯烃的化学性质
烷烃:
反应性:
烷烃对许多化学试剂都是惰性的。这是因为碳-碳(C-C)和碳-氢(C-H)键非常强,因为碳原子和氢原子具有几乎相同的电负性值。因此,很难打破它们的键,除非它们被加热到相当高的温度。
燃烧:
烷烃在空气中容易燃烧。烷烃与过量氧的反应称为“燃烧”。在这个反应中,烷烃转化为二氧化碳(CO2)和水。
CnH2n+(n+n/2)O2→n CO2+nH2O
C4H10+13/2氧气→4二氧化碳+5H2O
丁烷氧二氧化碳水
燃烧反应是放热反应(它们放出热量)。因此,烷烃被用作能源。
烯烃:
反应性:
Alkenes react with Hydrogen in the presence of a finely divided metal catalyst to form the corresponding alkane. The rate of the reaction is very low without a catalyst.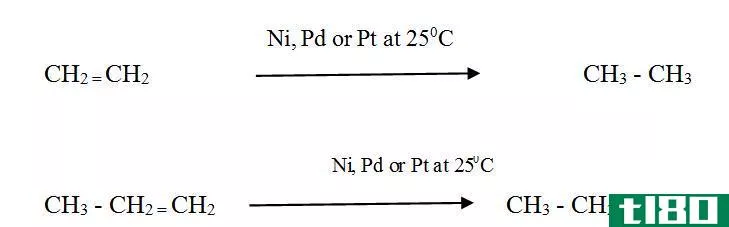
催化加氢在食品工业中被用于将液态植物油转化为半固态脂肪,用于**人造黄油和固体烹饪脂肪。
烷烃和烯烃的物理性质
形式
烷烃:烷烃以气体、液体和固体的形式存在。甲烷、乙烷、丙烷和丁烷是室温下的气体。正己烷、戊烷和庚烷的不分枝结构是液体。分子量较大的烷烃是固体。
CH4到C4H10是气体
C5H12至C17H36为液体,并且
分子量较大的烷烃是软固体
烯烃:烯烃表现出与相应烷烃相似的物理性质。低分子量烯烃(C2H4~4h8)是室温常压下的气体。分子量较大的烯烃是固体。
溶解度:
烷烃:烷烃不溶于水。它们溶解在非极性或弱极性有机溶剂中。
烯烃:由于C=C键,烯烃是相对极性的分子;因此,它们易溶于非极性溶剂或极性较低的溶剂中。水是一种极性分子,烯烃微溶于水。
密度:
烷烃:烷烃的密度低于水的密度。考虑到水的密度为1.0 g mL-1,它们的密度值接近0.7 g mL-1。
烯烃:烯烃的密度低于水的密度。
沸点:
烷烃:未支链烷烃的沸点随着碳原子数和分子量的增加而平稳地增加。一般来说,支链烷烃的沸点比无支链烷烃低,碳原子数相同。