阳极和阴极的主要区别在于阳极是正极,而阴极是负极。
阳极和阴极是极性相反的电极。要知道阳极和阴极之间的区别,我们首先需要了解它们是什么。阳极和阴极是用来将电流导入或引出任何利用电的设备的电极。电极是允许电流通过的导电材料。电极通常由铜、镍、锌等金属制成,但有些电极也由碳等非金属制成。此外,电极通过电流通过它来完成电路。
目录
1. 概述和主要区别
2. 什么是阳极
3. 什么是阴极
4. 并列比较-阳极与阴极的表格形式
5. 摘要
什么是阳极(anode)?
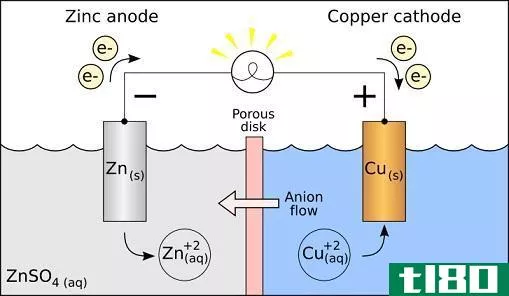
阳极是电流离开电池并发生氧化的电极。我们也叫它正电极。简单的电池由三个主要部分组成:阳极、阴极和电解液。传统上,电池的两端是电极。当我们把这些端部通电时,电池内部就会发生化学反应。在这里,电子受到干扰,必须重组。它们互相排斥,向电子较少的阴极移动。这就平衡了整个溶液(电解液)中的电子。
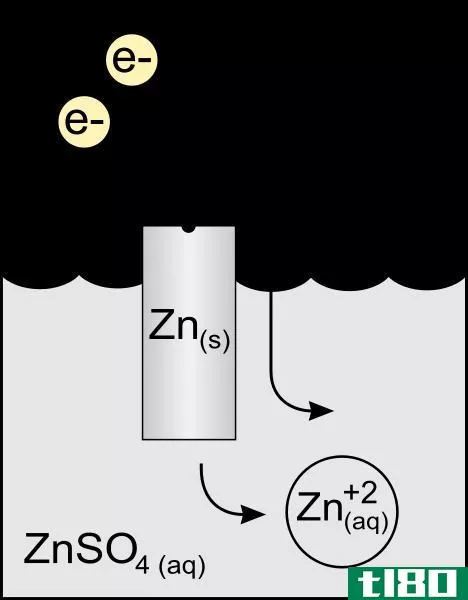
图01:锌阳极
一般来说,当器件放电时,电流从阴极流出。然而,当设备充电时,电流的方向相反,当阳极变成阴极时,阴极开始起到阳极的作用。
在原电池或电池中,端子是不可逆的,这意味着阳极永远是正的。这是因为我们总是用这个装置来释放电流。但对于二次电池或电池,电极是可逆的,因为设备放电,但也接受电流充电。
什么是阴极(cathode)?
阴极是电流进入电池并发生还原的电极。我们也可以称之为负电极。然而,在电解槽中阴极可以是负的,在原电池中可以是正的。
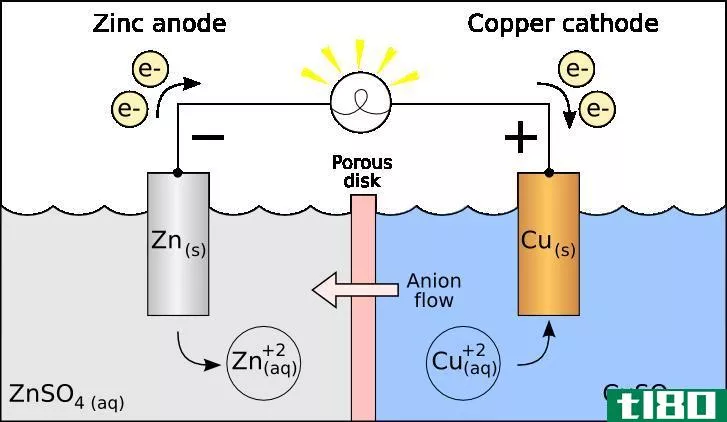
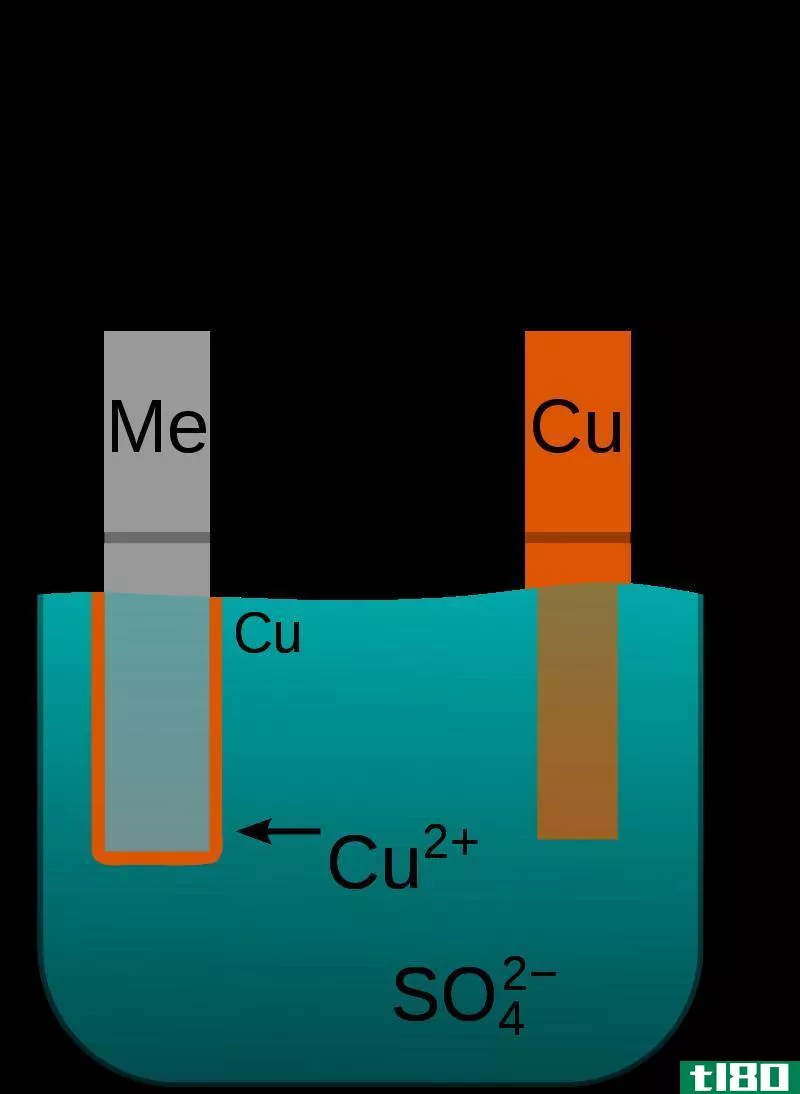
图02:电解槽中的阳极和阴极
阴极为阳离子(带正电荷的离子)提供电子。这些离子通过电解液流向阴极。此外,阴极电流是电子从阴极到溶液中阳离子的流动。然而,阴极和阳极这两个术语在不同的应用中可能有不同的含义。
阳极(anode)和阴极(cathode)的区别
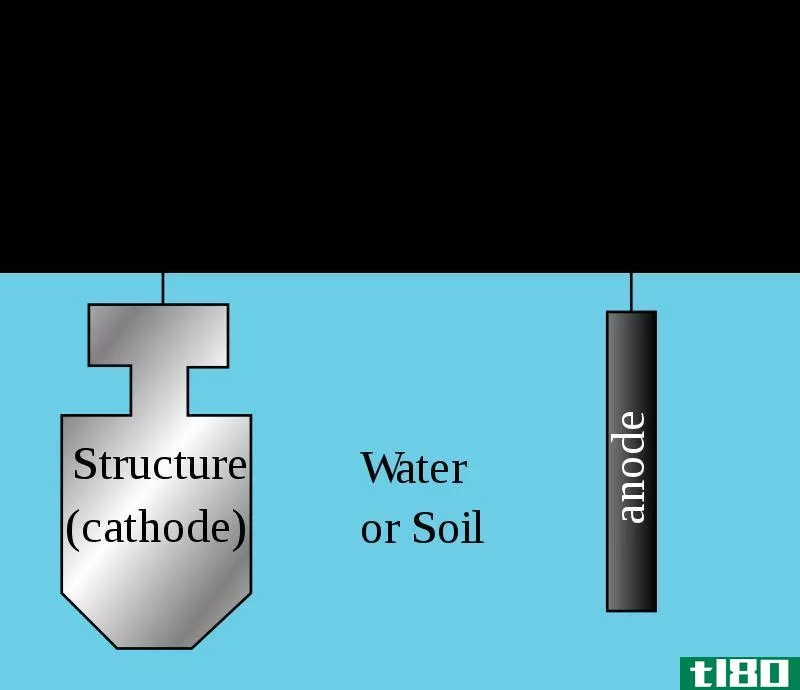
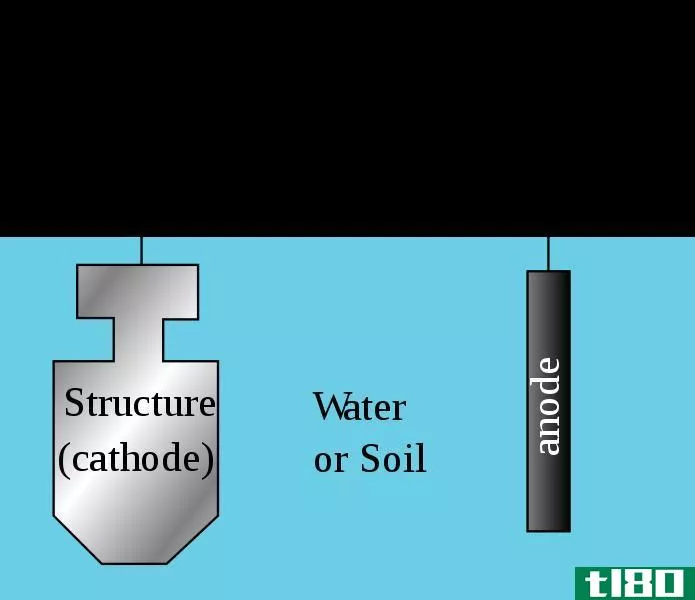
阳极是电流离开电池并发生氧化的电极,而阴极是电流进入电池并发生还原的电极。阳极和阴极的主要区别在于阳极是正极,而阴极是负极。然而,也有双极性电极,既可以作为阳极也可以作为阴极。一般来说,阳极吸引阴离子,阴极吸引阳离子,这就导致了这些电极的名称。
总结 - 阳极(anode) vs. 阴极(cathode)
阳极是电流离开电池并发生氧化的电极,而阴极是电流进入电池并发生还原的电极。阳极和阴极的主要区别在于阳极是正极,而阴极是负极。
引用
1“阴极”,维基百科,维基媒体基金会,2019年6月27日,可在这里查阅。