阳极保护和阴极保护的主要区别在于,在阳极保护中,被保护表面充当阳极,而在阴极保护中,被保护表面充当阴极。
阳极保护和阴极保护是我们用来防止表面腐蚀或生锈的两种电化学过程。在电化学过程中,我们使用一个有两个电极作为阳极和阴极的电化学电池。在阳极和阴极保护过程中,我们使用被保护的表面(基底)作为阳极或阴极,这导致了这些过程的名称。牺牲保护是一种阴极保护,我们用金属作为牺牲阳极。在这个过程中,这种牺牲金属腐蚀的同时避免了阴极的腐蚀。
目录
1. 概述和主要区别
2. 什么是阳极保护
3. 什么是阴极保护
4. 并列比较-阳极保护与阴极保护的表格形式
5. 摘要
什么是阳极保护(anodic protection)?
阳极保护是一种电化学过程,通过使金属表面成为电化学电池中的阳极来保护金属表面。我们可以用AP来表示。但是,此方法仅适用于显示相当宽的被动区域的材质环境组合。i、 钢和不锈钢在98%硫酸中。
在***,我们需要把金属带到一个高电位。然后,由于保护层的形成,金属变得被动。然而,AP并没有被广泛地用作阴极保护,因为它仅限于表面有足够可靠的钝化层的金属,例如不锈钢。
应用AP有两个主要考虑因素。首先,我们需要确保整个系统处于被动范围。其次,我们需要对离子有精确的了解,这会导致广泛的点蚀。
什么是阴极保护(cathodic protection)?
阴极保护是一种电化学过程,通过使金属表面成为电化学电池的阴极来保护金属表面。可以用CP来表示,CP可以防止金属表面的腐蚀。阴极保护有不同的类型;例如,电流保护或牺牲保护,外加电流系统和混合系统。
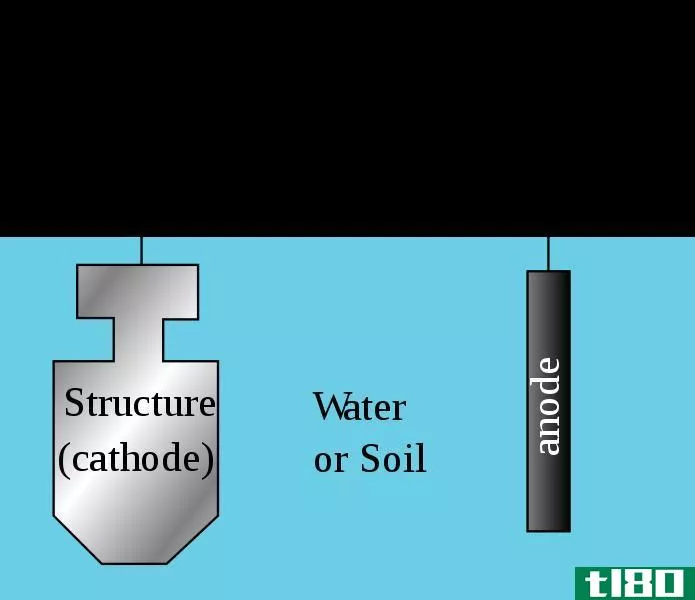
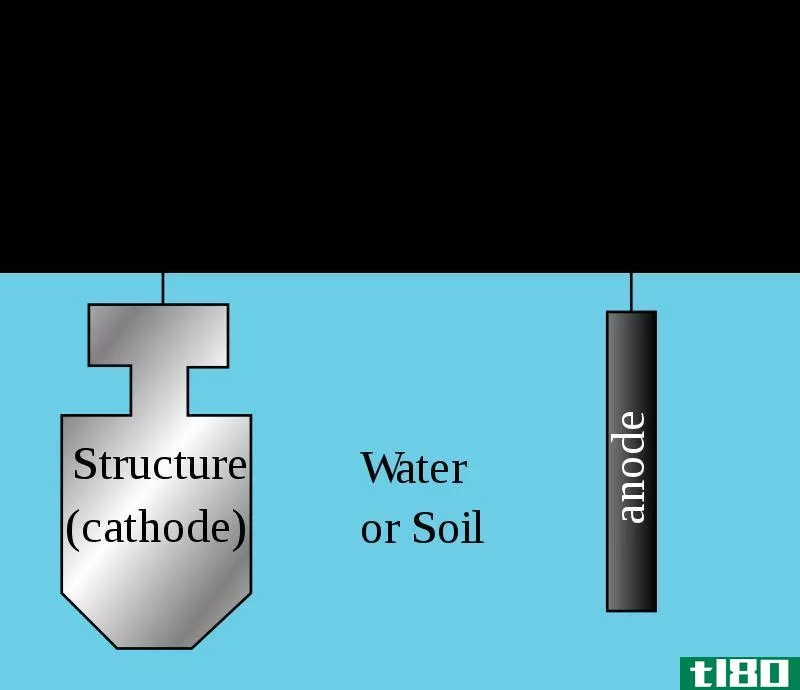
图01:外加电流系统
在这种方法中,牺牲金属而不是被保护金属腐蚀。对于长管道等大型构筑物,采用阴极保护技术是远远不够的。因此,我们需要使用外部直流电源提供足够的电流。

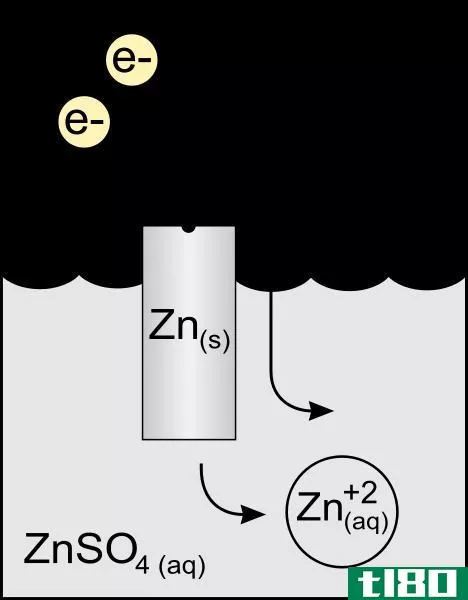
图02:牺牲阳极-锌层
此外,我们还可以用这种技术来保护由钢制成的燃料或水管、储罐、船舶和船壳、镀锌钢等制成的管道。
阳极的(anodic)和阴极保护(cathodic protection)的区别
阳极保护是一种电化学过程,在这种过程中,我们可以通过使金属表面成为电化学电池中的阳极来保护金属表面,而阴极保护则是通过使金属表面成为电化学电池中的阴极来保护金属表面的电化学过程。因此,阳极保护和阴极保护的关键区别在于,在阳极保护中,被保护表面充当阳极,而在阴极保护中,它是阴极。
此外,阳极保护包括通过调节更具活性的金属的电位来抑制金属的反应性;然而,阴极保护涉及两个不同电极之间的电流反向流动。因此,我们也可以认为这是阳极保护和阴极保护的区别。
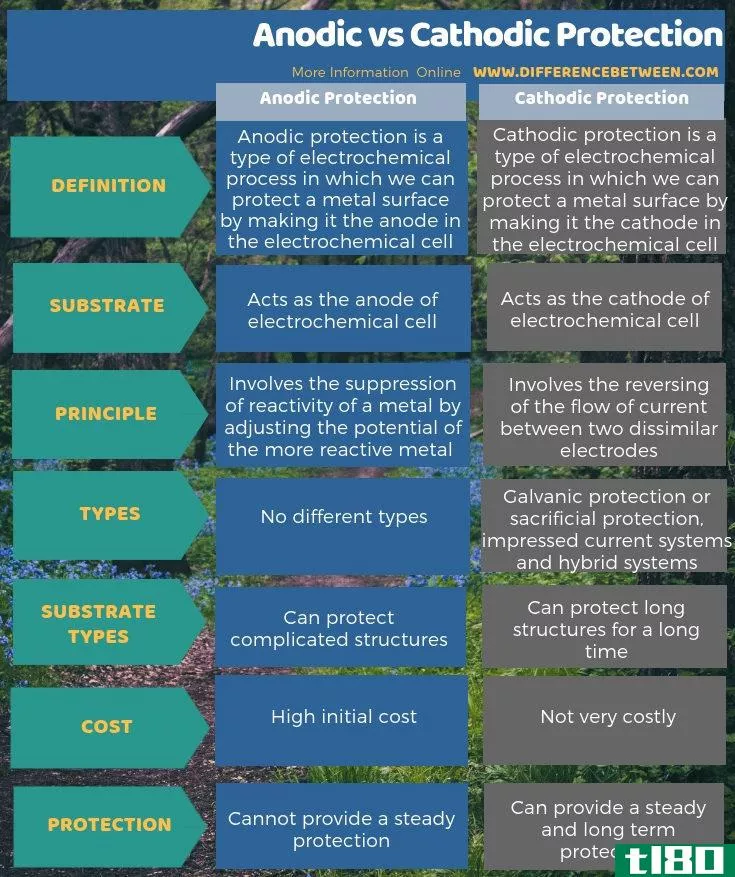
总结 - 阳极的(anodic) vs. 阴极保护(cathodic protection)
阳极保护是一种电化学过程,在这种过程中,我们可以通过使金属表面成为电化学电池中的阳极来保护金属表面,而阴极保护则是通过使金属表面成为电化学电池中的阴极来保护金属表面的电化学过程。阳极保护和阴极保护的主要区别在于,在阳极保护中,被保护表面充当阳极,而在阴极保护中,它是阴极。
引用
1“什么是牺牲保护?–来自Corrosionpedia的定义。“Corrosionpedia,可从这里获得。