查尔斯·劳vs波义耳定律
查尔斯定律和波义耳定律是有关气体的两个非常重要的定律。这两个定律可以描述理想气体的许多性质。这些定律广泛应用于化学、热力学、航空甚至军事等领域。要想在这两个领域出类拔萃,必须对这两个规律有充分的了解。在本文中,我们将讨论什么是查尔斯定律和波义耳定律,它们的定义,查尔斯定律和波义耳定律的应用,它们的相似之处,最后讨论查尔斯定律和波义耳定律的区别。
波义耳定律
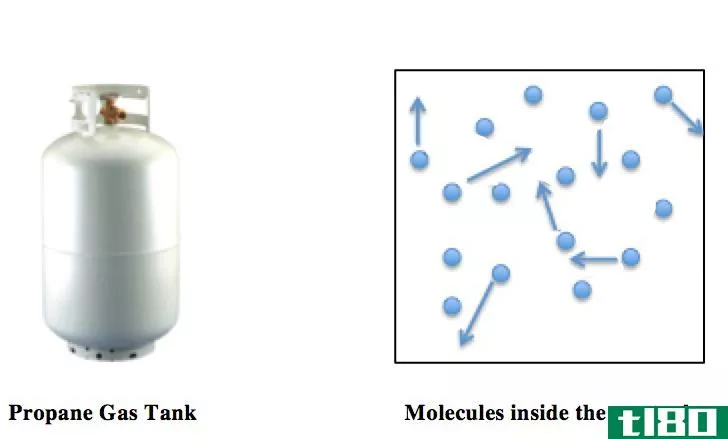
波义耳定律是气体定律。它被定义为理想气体。正确理解理想气体的这些定律是必要的。理想气体是指每个分子所占体积为零的气体,分子间的分子间吸引力也为零。这种理想气体在现实生活中并不存在。存在于现实生活中的气体被称为真实气体。真实气体有分子体积和分子间作用力。如果一个真实气体的所有分子的总体积与容器的体积相比可以忽略不计,而分子间的作用力与分子的速度相比可以忽略不计,那么气体就可以被认为是该系统中的理想气体。波义耳定律是1662年由化学家和物理学家罗伯特·博伊尔提出的,可以表述如下。对于一定量的理想气体,保持在一定的温度下,压力和体积成反比。
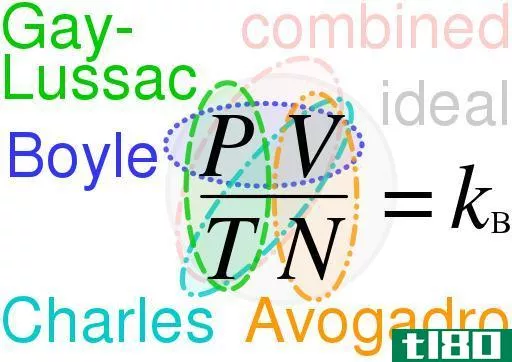
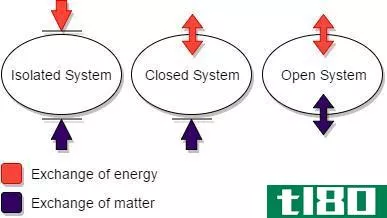
封闭系统是指周围环境和系统之间不可能发生质量交换,但可以进行能量交换的系统。波义耳定律表明,理想气体在恒定温度下的压力和体积的乘积是恒定的。换句话说,P V=K,其中P是压力,V是体积,K是常数。这意味着,如果这样一个系统的压力增加一倍,那么这个系统的体积就会变成原来的一半。
查尔斯定律
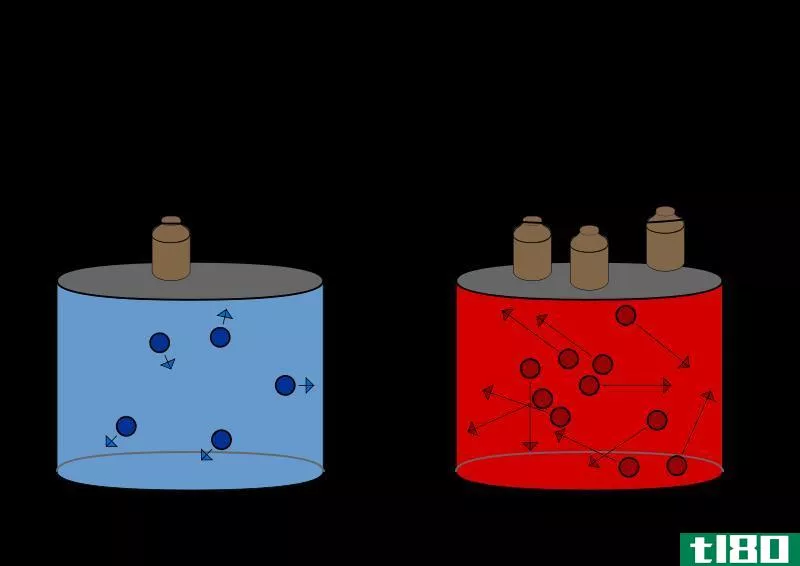
查尔斯定律也是一种气体定律,它被定义为封闭系统中的理想气体。这表明,对于一个定压封闭的理想气体系统,系统的体积与系统的温度成正比。这条定律最早由法国哲学家约瑟夫·路易斯·盖伊·卢萨克(Joseph Louis Gay Lussac)发表,但他将这一发现归功于雅克·查尔斯。这个定律表明,对于这样的系统,温度和体积的比值必须是常数。换句话说,V/T=K,其中V是气体的体积,T是气体的温度。必须注意的是,从数学上讲,这种比例仅适用于开尔文标度,即绝对温标。
| 查尔斯定律和波义耳定律有什么区别?•查尔斯定律是针对恒压系统定义的,而波义耳定律是针对恒温系统定义的。•查尔斯定律中涉及的两项是直接成正比的,而波义耳定律中涉及的项则是反比例的。 |