关键区别-速率定律与质量作用定律
速率定律和质量作用定律的关键区别在于速率定律表示化学反应速率和反应物浓度之间的关系,而质量作用定律则表示化学反应的速率与反应物质的质量成正比。
速率定律是化学中用来解释反应混合物行为的定律。速率定律表明反应速率与反应速率成正比。比例常数被称为速率常数。质量作用定律表明,化学反应的反应速率与反应物质量的乘积成正比,这些反应物的质量提高到实验确定的幂次(通常等于化学方程式中它们的化学计量系数)。
目录
1. 概述和主要区别
2. 什么是利率定律
3. 什么是质量作用定律
4. 并列比较-速率定律与质量作用定律的表格形式
5. 摘要
什么是费率律(rate law)?
速率定律表示化学反应速率与反应物浓度之间的关系。根据速率定律,一个反应的速率与反应物的浓度成正比,而反应物的浓度提高到实验确定的幂次(通常等于化学方程式中的化学计量关系)。
费率定律有两种类型:
- 微分速率定律
微分速率定律给出了在特定时间段内反应物浓度变化的反应速率。
- 综合费率法
积分速率定律给出反应速率,它是反应物在特定时间段初始浓度的函数。
让我们考虑一个例子来理解这一点。
aA+bB→cC+dD
速率=k[A]A[B]B
上面的方程给出了速率定律的数学表达式。在这里,“k”是一个比例常数。它被称为速率常数。指数“a”和“b”分别是相对于反应物a和b的反应级数。反应的总阶数(p)是速率定律方程中所有阶数之和。
p=a+b
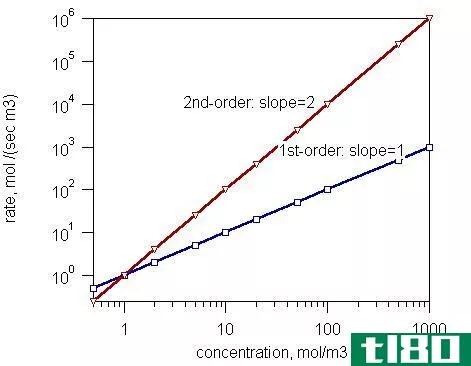
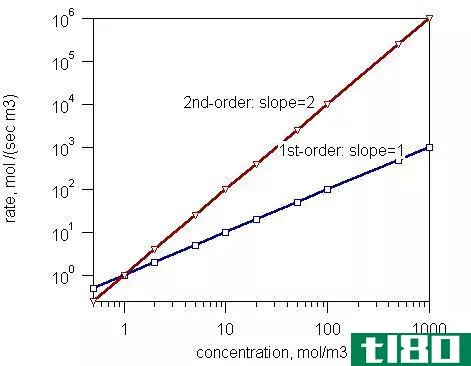
图1:一级反应和二级反应的速率和浓度。
根据反应的总体顺序,反应分为三类:
- 零级反应-反应速率与反应物浓度无关
- 一级反应-反应速率与一种反应物的浓度成正比。
- 二级反应-反应速率与两个反应物浓度的乘积或一个反应物浓度的平方成正比。
什么是质量作用定律(law of mass action)?
质量作用定律表明化学反应的速率与反应物质的质量成正比。它也被称为质量作用定律。这一定律有助于获得特定化学反应的精确平衡方程。这个定律也由反应物的活性或浓度给出。根据质量作用定律,反应混合物处于平衡状态时,产物浓度与反应物浓度之比为常数。
质量作用定律是一个普遍的概念,它适用于任何情况下的任何系统。这个定律可以用下面的数学表达式给出。
对于反应,
aA+bB型↔ 抄送+dD
平衡时产物与反应物的比率;
Keq=[C]C[D]D/[A]A[B]B
在给定温度下,上述比率是反应物(a和B)与产物(C和D)之间平衡的常数。这里,Keq被称为平衡常数。
费率律(rate law)和质量作用定律(law of mass action)的区别
| 速率定律与质量作用定律 | |
| 速率定律表明,反应速率与反应物的浓度成正比,反应物的浓度提高到实验确定的功率。 | 质量作用定律表明化学反应的速率与反应物质的质量成正比。 |
| 方程的组成部分 | |
| 速率定律方程有速率常数、反应物浓度和反应级数。 | 质量作用定律有一个方程,由产物和反应物的浓度增加到化学计量系数的幂次方组成。 |
| 产品 | |
| 速率定律方程不包含产物浓度。 | 质量作用定律方程包含了产物的浓度。 |
| 比例分量 | |
| 速率定律方程的比例常数称为速率常数K。 | 质量作用定律方程中没有比例常数。 |
总结 - 费率律(rate law) vs. 质量作用定律(law of mass action)
速率定律和质量作用定律被用来解释反应混合物的行为。速率定律和质量作用定律的关键区别在于速率定律表示化学反应速率和反应物浓度之间的关系,而质量作用定律则表示化学反应的速率与反应物质的浓度成正比。
引用
1“费率法”,《化学图书馆》,2016年7月21日,可在此处查阅。“12.3速率定律。”化学,这里有。Laidler,Keith J.“群众行动法则”,《大英百科全书》,2016年10月26日,可在此处查阅。
2“12.3速率定律”,化学,
三。Laidler,Keith J.“群众行动法则”,《大英百科全书》,百科全书,大英百科全书,2016年10月26日,