轨道(orbit)和轨道(orbital)的区别
轨道vs轨道
在原子理论中,这两个听起来相似的术语“轨道”和“轨道”常常使人困惑。你一定在照片中看到过,原子是一个简单的,类似太阳系的结构,其中的电子就像我们的行星,围绕着一个可能被认为是太阳的原子核旋转。事实上,真相要复杂得多。轨道和轨道是原子的不同路径。
在我们的太阳系中,行星旋转的轨道称为轨道。这些是奇怪的椭圆路径,每个行星都是固定的,这些行星以角速度和中心加速度沿着这条路径运动。原子也是如此。轨道是电子围绕原子核旋转的固定路径,遵循与行星相同的原理。
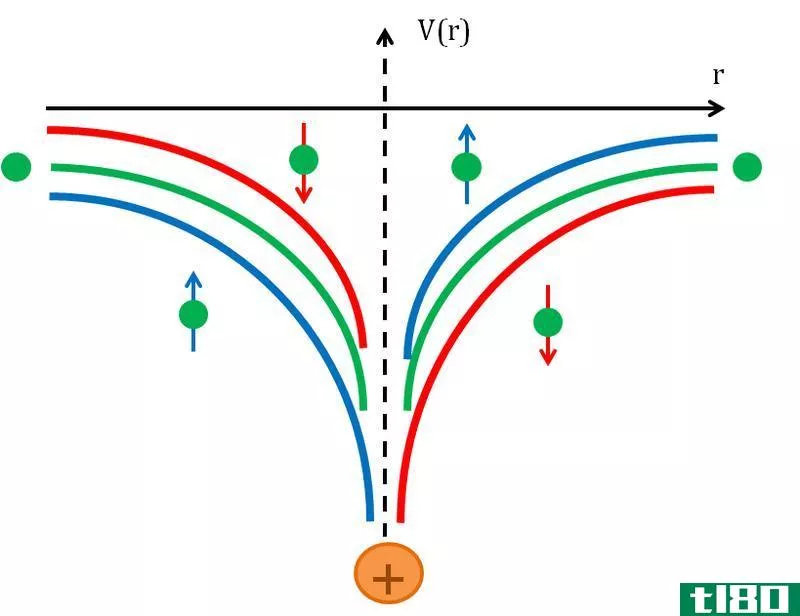
轨道是平面或二维的圆形路径。特定轨道上的最大电子数是2n2。轨道遵循牛顿运动定律。在原子理论中,由于带负电荷的电子以相同的角速度吸引带正电荷的原子核而形成轨道。但由于海森堡测不准原理证明它是不确定的,我们不能轻易地确定一个电子的确切轨道。
如果你认为一个人能在某个时间分辨出电子的确切位置,那你就错了。根据海森堡测不准原理:
“决定一个最小粒子(电子)运动的两个重要因素——它的位置和速度,人们永远无法精确地知道。不可能同时准确地确定粒子或电子的位置、方向和速度。”
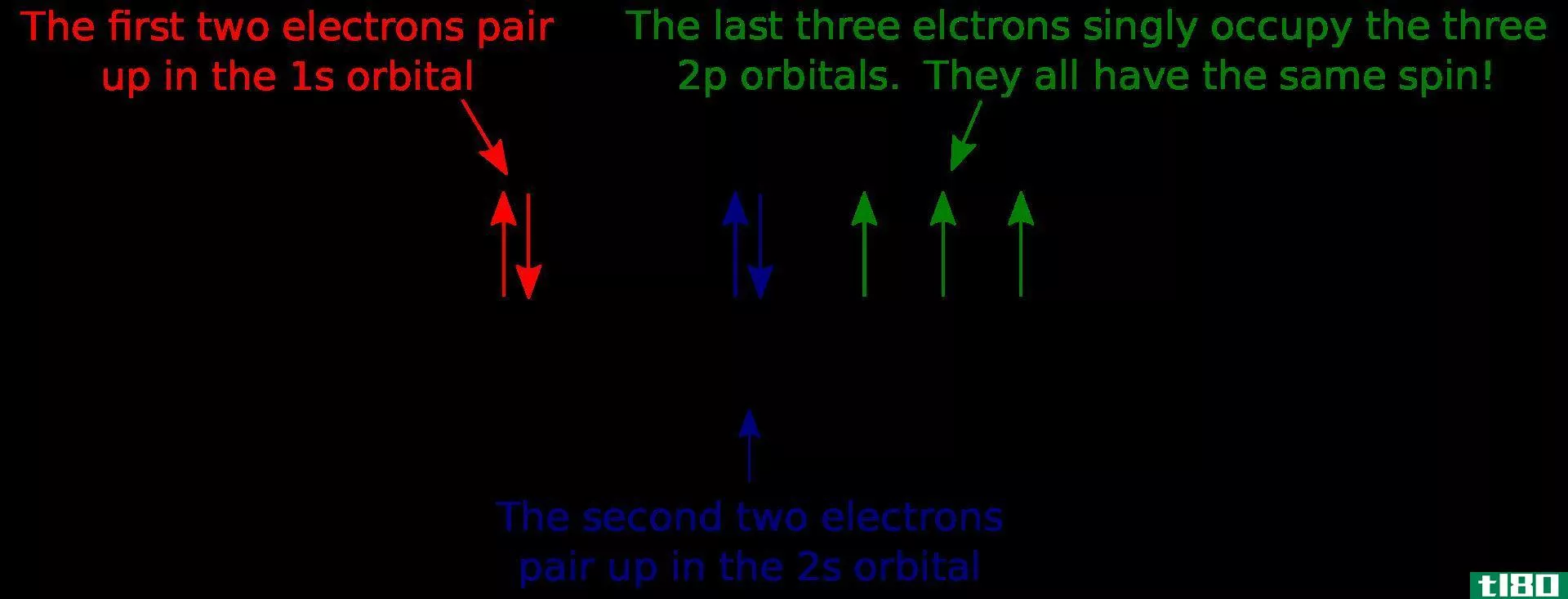
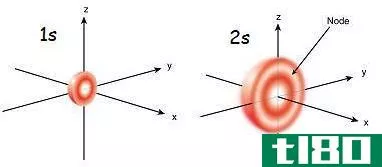
所以轨道是原子内部的一个不确定区域,在这个区域内找到电子的概率最高。它代表了原子核周围的三维空间。根据元素及其原子序数,轨道的形状和容量各不相同。它们被归类为s,p,d和f型轨道。这些轨道的最大容量are:s orbital –2个电子轨道–6个电子轨道–10个电子轨道–16个电子
总结:
1.轨道是重物体周围的固定路径,较轻的物体在重力或电磁力的作用下在轨道上运动,而轨道是原子核周围的不确定区域,在该区域内找到电子的概率最大。2.任何两个具有一定质量的物体都有轨道,而轨道只存在对于一个原子和一个电子。
- 发表于 2021-06-24 01:03
- 阅读 ( 155 )
- 分类:物理
你可能感兴趣的文章
自旋轨道耦合(spin-orbit coupling)和拉塞尔桑德斯效应(russell-saunders effect)的区别
自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。 分析化学中的耦合主要是指轨道和电子...
- 发布于 2020-09-29 23:05
- 阅读 ( 520 )
轨道图(orbital diagram)和电子组态(electron configuration)的区别
轨道图和电子构型的关键区别在于,轨道图用箭头表示电子,表示电子的自旋。但是,电子组态没有显示电子自旋的细节。 轨道图显示了由电子组态给出的电子排列。电子组态给出了电子在整个原子轨道上分布的细节。但是...
- 发布于 2020-10-14 00:32
- 阅读 ( 737 )
px py公司(px py)和pz轨道(pz orbitals)的区别
Px-Py和Pz轨道的关键区别在于Px轨道有两个沿x轴方向的波瓣,Py轨道有两个沿y轴方向的波瓣,而Pz轨道有两个沿z轴方向的波瓣。因此,Px-Py和Pz轨道之间的差异源于它们在空间中的取向。 An atomic orbital is a region around an atomic nucleu...
- 发布于 2020-10-14 02:27
- 阅读 ( 943 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。 有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论...
- 发布于 2020-10-15 22:50
- 阅读 ( 842 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
混合轨道和退化轨道的关键区别在于,混合轨道是两个或多个轨道混合形成的新轨道,而退化轨道最初存在于原子中。 正如它的名字所暗示的,混合轨道是两个或更多轨道的混合。虽然简并轨道的名称看起来是一样的,但它...
- 发布于 2020-10-16 17:47
- 阅读 ( 899 )
纯净的(pure)和杂化轨道(hybrid orbitals)的区别
纯轨道和杂化轨道的关键区别在于,纯轨道是原始原子轨道,而杂化轨道是由两个或多个原子轨道混合而成。 在简单分子的化学键形成过程中,我们可以简单地考虑原子轨道的重叠。但是如果我们要讨论复杂分子中的化学键...
- 发布于 2020-10-17 13:43
- 阅读 ( 559 )
轨道(orbit)和轨道(orbital)的区别
轨道与轨道的关键区别在于,轨道是一条围绕中心点有固定路径的环形路径,而轨道是围绕原子核的不确定区域。 虽然术语“轨道”和“轨道”听起来相似,但这是两个不同的术语。轨道一词主要与行星有关,而轨道一词则...
- 发布于 2020-10-23 03:43
- 阅读 ( 450 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
分子轨道和原子轨道的关键区别在于,原子轨道描述的是原子中找到电子的概率很高的位置,而分子轨道描述的是分子中电子的可能位置。 利用薛定谔、海森堡和保罗·狄拉克提出的新理论,人们以一种新的方式来理解分子...
- 发布于 2020-10-24 07:58
- 阅读 ( 561 )
1秒(1s)和2s轨道(2s orbital)的区别
1秒(1s)和2s轨道(2s orbital)的区别 原子是物质的最小单位。换句话说,所有物质都是由原子构成的。原子由亚原子粒子组成,主要是质子、电子和中子。质子和电子使原子核位于原子中心。但是电子被定位在位于原子核外的轨道...
- 发布于 2020-10-25 04:49
- 阅读 ( 585 )
结合(bonding)和反键分子轨道(antibonding molecular orbitals)的区别
成键与反键分子轨道 这两种分子轨道间的化学键可以用化学键和分子轨道键的不同来解释。键和反键分子轨道之间最显著的区别是它们相对于母原子轨道的能级。这种能级差异导致了两个分子轨道之间的其他差异。 成键和反...
- 发布于 2020-10-26 19:13
- 阅读 ( 646 )