分子轨道理论和价键理论的主要区别在于,分子轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。
不同的分子具有不同的化学和物理性质,不同的原子连接起来形成这些分子。为了了解原子和分子性质之间的这些差异,有必要了解几个原子之间形成化学键来形成一个分子。目前,我们用两种量子力学理论来描述分子的共价键和电子结构。它们是价键理论和分子轨道理论。
目录
1. 概述和主要区别
2. 什么是分子轨道理论
3. 什么是价键理论
4. 并列比较-分子轨道理论与价键理论的表格形式
5. 摘要
什么是分子轨道理论(molecular orbital theory)?
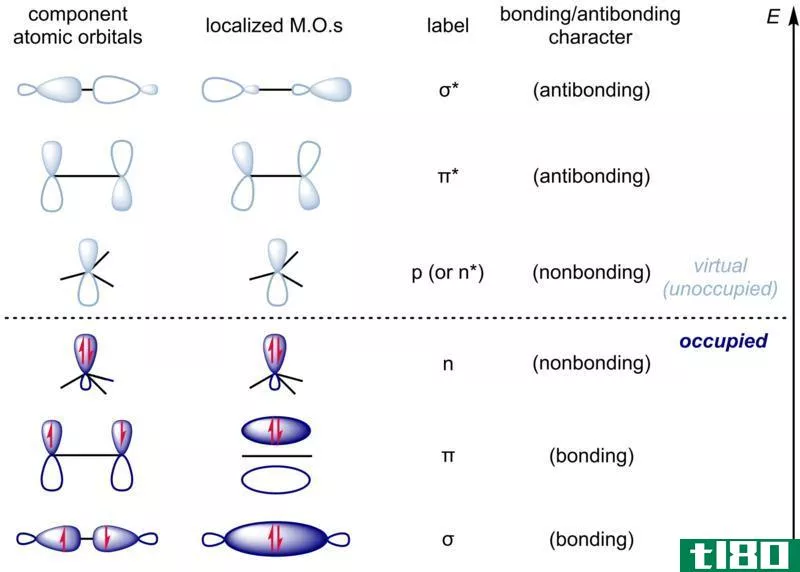
在分子中,电子位于分子轨道上,但它们的形状不同,它们与不止一个原子核有关。分子轨道理论是基于分子轨道对分子的描述。
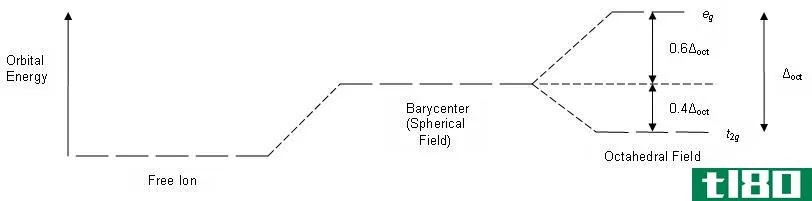
通过原子轨道的线性组合,可以得到描述分子轨道的波函数。当两个原子轨道在同一相位(构造相互作用)中相互作用时,键轨道形成。当它们相互作用时(破坏性相互作用),反键轨道从。因此,每个次轨道相互作用都存在键合轨道和反键轨道。键轨道能量低,电子更容易存在于这些轨道中。反键轨道能量高,当所有的键合轨道都被填满时,电子会进入反键轨道。
什么是价键理论(valence bond theory)?
价键理论是基于局域键方法,它假定分子中的电子占据单个原子的原子轨道。例如,在H2分子的形成过程中,两个氢原子重叠了它们的1s轨道。通过重叠两个轨道,它们在空间**享一个共同区域。最初,当两个原子相距甚远时,它们之间没有相互作用。因此,势能为零。
当原子彼此靠近时,每个电子都被另一个原子的原子核所吸引,同时,电子相互排斥,原子核也是如此。当原子仍处于分离状态时,引力大于斥力,因此系统的势能降低。当势能达到最小值时,系统处于稳定状态。这就是当两个氢原子聚在一起形成分子时发生的情况。

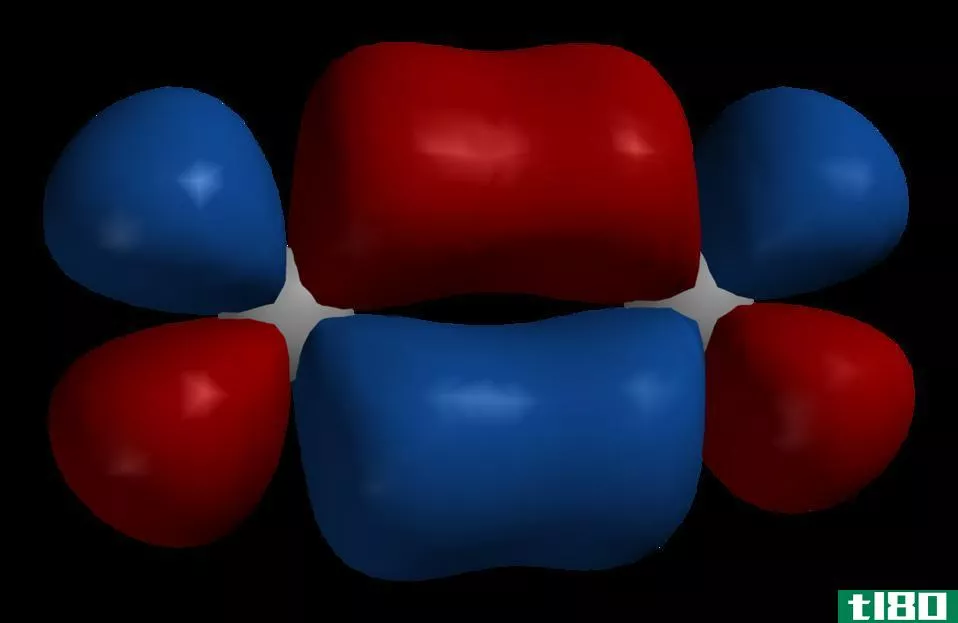
图01:π键的形成
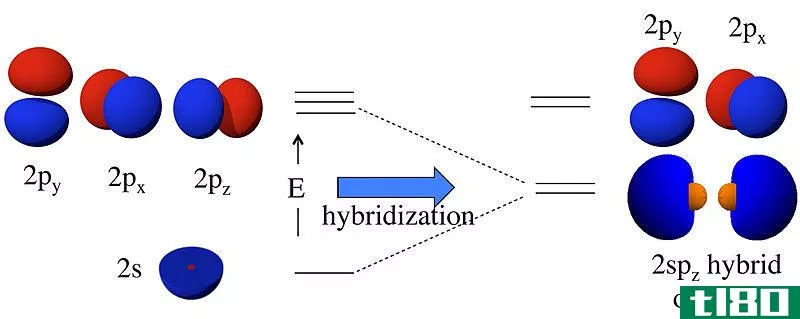
然而,这个重叠的概念只能描述简单的分子,如H2,F2,HF等,这个理论无法解释像CH4这样的分子。然而,将这一理论与杂化轨道理论相结合可以解决这个问题。杂化是两个不相等的原子轨道的混合。例如,在CH4中,C有四个杂化sp3轨道与每个H的s轨道重叠。
分子轨道理论(molecular orbital theory)和价键理论(valence bond theory)的区别
目前,我们用两种量子力学理论来描述分子的共价键和电子结构。它们是价键理论和分子轨道理论。分子轨道理论和价键理论的主要区别在于,分子轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。此外,价键理论只适用于双原子分子,而不适用于多原子分子。然而,我们可以将分子轨道理论应用于任何分子。
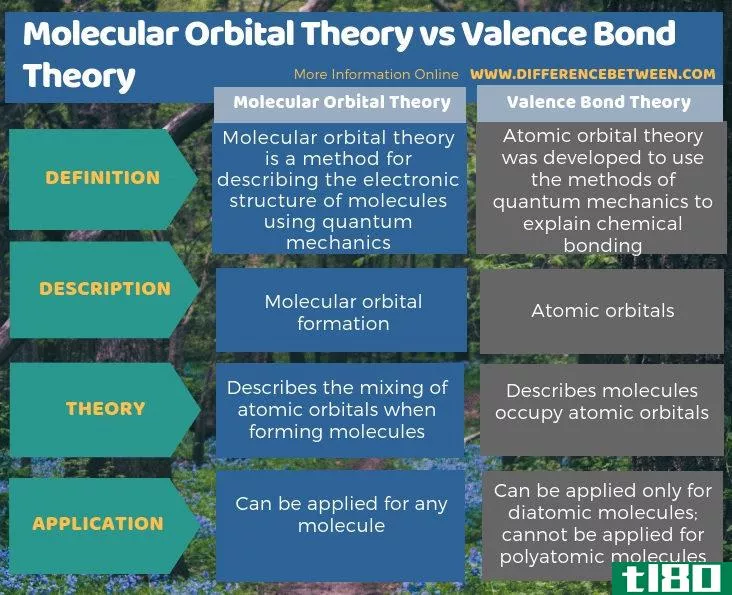
总结 - 分子轨道理论(molecular orbital theory) vs. 价键理论(valence bond theory)
价键理论和分子轨道理论是描述分子共价键和电子结构的两种量子力学理论。分子轨道理论和价键理论的主要区别在于,分子轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。
引用
1赫尔曼斯汀,安妮·玛丽。“价键(VB)理论定义”,ThoughtCo,2019年8月4日,可在此处查阅。