轨道(orbit)和轨道(orbital)的区别
刚接触原子理论的人,通常会发现“轨道”和“轨道”这两个词是一样的。然而,事实并非如此。这两个术语在多个方面都有很大的不同。
轨道(orbit) vs. 轨道(orbital)
轨道和轨道的区别在于,轨道被认为是电子旋转的确定路径,而轨道是一个不确定的区域,在这里找到电子的可能性最大。轨道是二维或平面区域。然而,一个轨道代表了一个三维区域,在那里找到一个电子的概率是最大的。

你可以把原子中的电子想象成太阳系的行星,原子核代表太阳。这些电子倾向于沿着称为轨道的路径旋转。当电子围绕其轨道旋转时,它们遵循行星围绕太阳旋转时遵循的每一个原则。
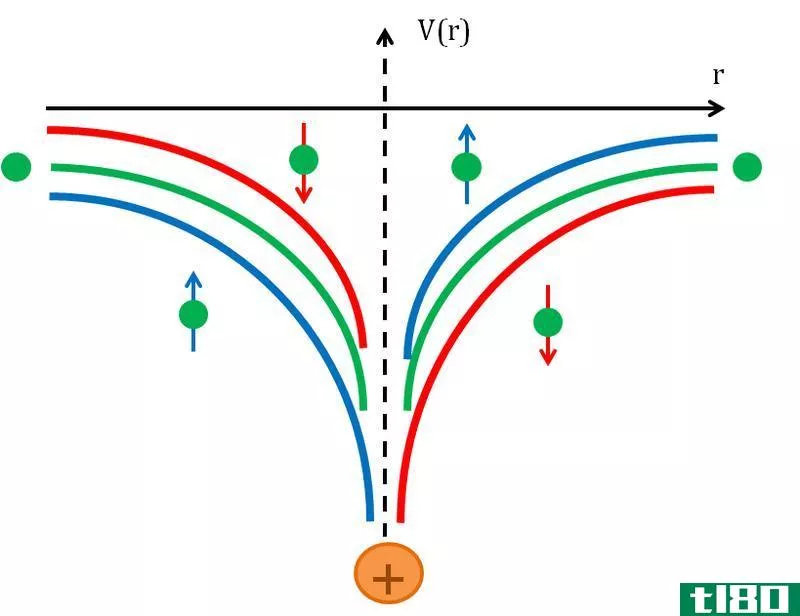
根据海森堡测不准原理,电子的位置不能准确地确定。为了表示电子在原子内部的位置,引入了轨道的概念。
然而,轨道也不能说明电子的速度、方向和位置。但它给出了一个准确的想法,电子可能在哪里。
| Parameter of Comparison | Orbit | Orbital |
|---|---|---|
| 定义 | 电子绕原子核旋转的路径称为轨道。 | 在三维空间中找到电子的几率很高,这就是所谓的轨道。 |
| 位置精度 | 它表示一个电子在原子内部的确切位置。 | 它不能代表电子的准确位置。 |
| 测不准原理 | 一个轨道并不遵循海森堡的测不准原理,因为它声称要说明一个电子的确切位置。 | 由于轨道并不代表电子的确切位置,它遵循海森堡测不准原理。 |
| 形状 | 每个轨道都有一个圆形。 | 轨道有不同的形式——球形、钟形等。 |
| 任命 | 轨道由字母K、L、M、N等定义。 | 轨道主要由字母s、p、d和f来定义。 |
轨道与轨道比较表(表格形式)
什么是轨道(orbit)?
轨道被定义为一条圆形的确定路径,在该路径上,由于电子对带正电的原子核的拉力,电子旋转。这就是玻尔的原子理论。
玻尔模型还指出,原子的第一层壳层只能容纳2个电子。然而,玻尔的模型后来被拒绝了。
目前被广泛接受的模型是陈述轨道概念的模型。为了理解阿诺比特的概念,你需要了解太阳系。
这样想,太阳系中的行星代表着电子,它们围绕着太阳旋转,在这种情况下,太阳是一个原子核。
像行星一样,电子在绕原子核旋转时也遵循牛顿运动定律。与轨道不同,轨道只是一条二维路径。单个轨道最多可容纳2n2个电子。
根据海森堡测不准原理,电子的准确位置是无法确定的。
这就是轨道概念的由来。
什么是轨道(orbital)?
根据海森堡原理,不能确定电子的确切位置。这就是向我们介绍理论的东西。
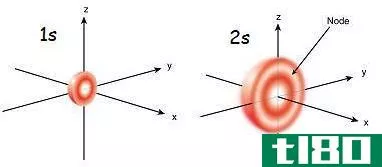
轨道是一个不确定的区域,它描述了在那里找到电子的最大可能性。原子核周围的三维空间代表了轨道。
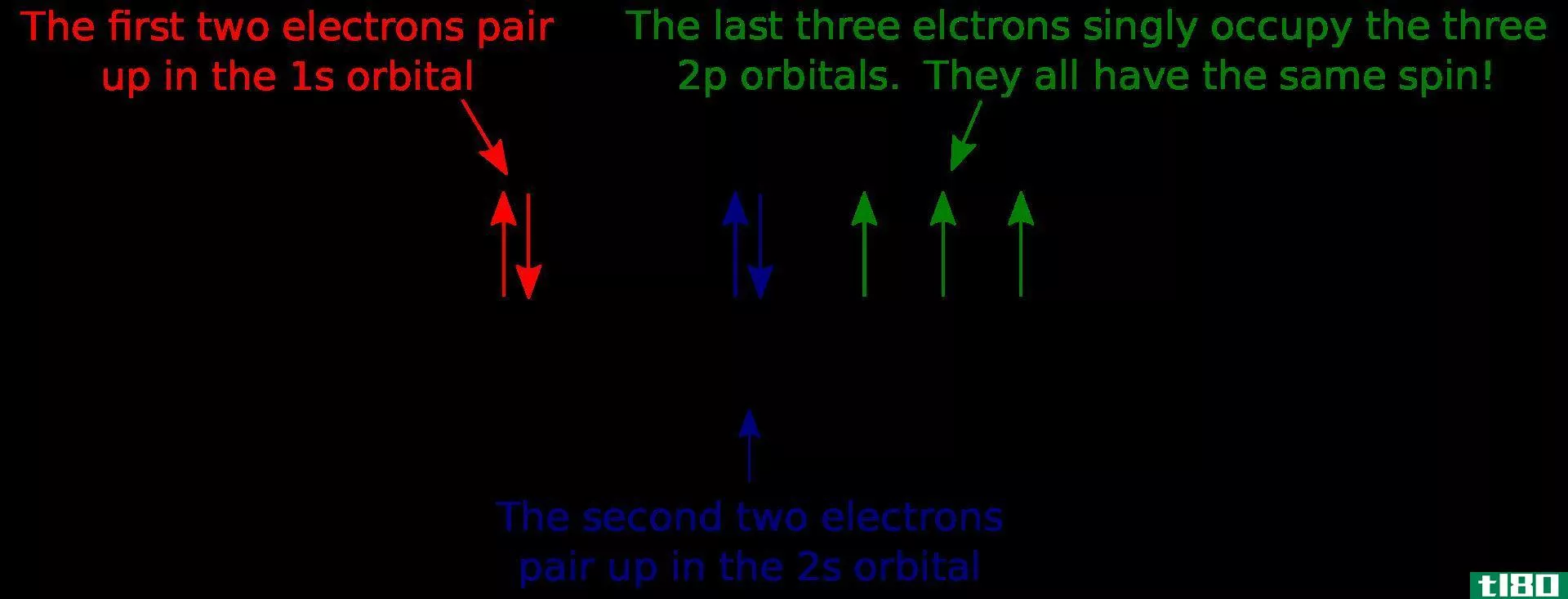
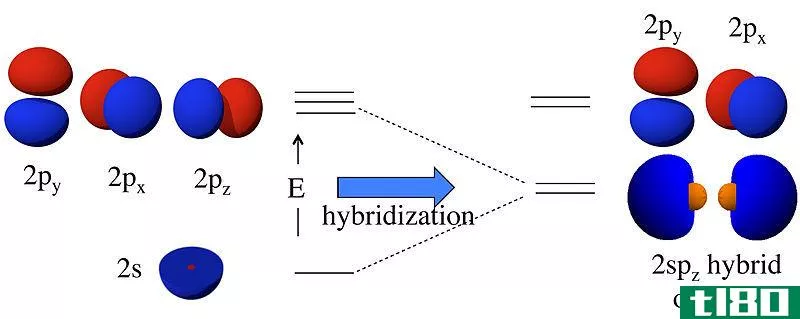
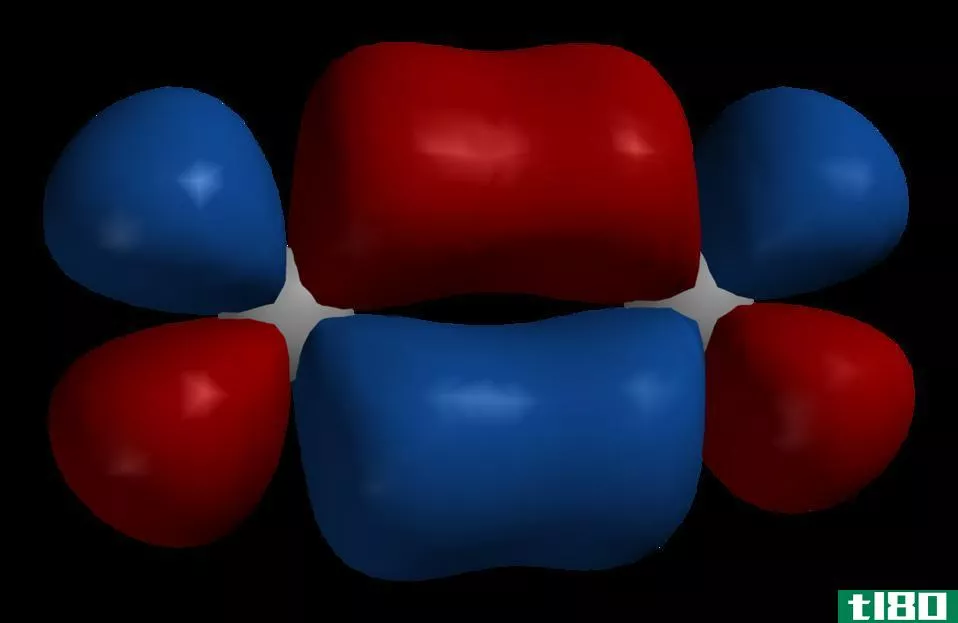
轨道有各种各样的形状。轨道一般分为四种形式——s、p、d和f。s轨道的最大容量可以容纳2个电子,p最多可以容纳6个,d最多可以容纳10个,而f最多可以容纳16个电子。
在原子的三维区域,找到电子的可能性相当高,也就是说,95%。
在轨道上,很容易确定分子的形状,因为它们是定向的。轨道高度依赖于海森堡原理。
轨道与轨道的主要区别
- 轨道是一条确定的电子在其上旋转的路径。然而,一个轨道是一个三维路径,在那里找到一个电子的可能性是相当高的。
- 轨道声称能描述电子在原子中的准确位置,而轨道并不声称能描述电子的准确位置。
- 电子在轨道上的二维或平面运动。然而,电子在一个轨道中绕着原子核在三维空间中运动。
- As Orbits claim to tell the accurate position of electr***, it does not go well with the Heisenberg’s Uncertainty Principle. 轨道并不能确定电子的位置,它可能在三维空间的任何地方。因此,它符合海森堡原理。
- 没有一个轨道显示出包括方向在内的任何特征,而在轨道的情况下,除了s轨道外,可以看到方向特征。
结论
轨道和轨道是两个不同的术语,它们都与原子有关。原子轨道的概念与太阳系中围绕太阳旋转的行星的概念完全相同。
轨道上的电子完全遵循牛顿运动定律。然而,它们并不符合海森堡的测不准原理。
一个轨道代表了原子核周围的三维空间,在这个空间中找到电子的概率非常高。它完全遵循海森堡的测不准原理。
根据海森堡测不准原理,不可能精确地确定原子中电子的运动、速度和方向。
你唯一能得到的是一个粗略的表示,你可能在原子中找到一个电子的位置。
参考文献
- https://www.birpublicati***.org/doi/pdf/10.1038/sj/dmfr/4600551
- https://www.oto.theclinics.com/article/S0030-6665(11) 00102-2/摘要
- 发表于 2021-07-07 06:44
- 阅读 ( 242 )
- 分类:科学
你可能感兴趣的文章
自旋轨道耦合(spin-orbit coupling)和拉塞尔桑德斯效应(russell-saunders effect)的区别
自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。 分析化学中的耦合主要是指轨道和电子...
- 发布于 2020-09-29 23:05
- 阅读 ( 520 )
轨道图(orbital diagram)和电子组态(electron configuration)的区别
轨道图和电子构型的关键区别在于,轨道图用箭头表示电子,表示电子的自旋。但是,电子组态没有显示电子自旋的细节。 轨道图显示了由电子组态给出的电子排列。电子组态给出了电子在整个原子轨道上分布的细节。但是...
- 发布于 2020-10-14 00:32
- 阅读 ( 737 )
px py公司(px py)和pz轨道(pz orbitals)的区别
Px-Py和Pz轨道的关键区别在于Px轨道有两个沿x轴方向的波瓣,Py轨道有两个沿y轴方向的波瓣,而Pz轨道有两个沿z轴方向的波瓣。因此,Px-Py和Pz轨道之间的差异源于它们在空间中的取向。 An atomic orbital is a region around an atomic nucleu...
- 发布于 2020-10-14 02:27
- 阅读 ( 943 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。 有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论...
- 发布于 2020-10-15 22:50
- 阅读 ( 842 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
混合轨道和退化轨道的关键区别在于,混合轨道是两个或多个轨道混合形成的新轨道,而退化轨道最初存在于原子中。 正如它的名字所暗示的,混合轨道是两个或更多轨道的混合。虽然简并轨道的名称看起来是一样的,但它...
- 发布于 2020-10-16 17:47
- 阅读 ( 899 )
纯净的(pure)和杂化轨道(hybrid orbitals)的区别
纯轨道和杂化轨道的关键区别在于,纯轨道是原始原子轨道,而杂化轨道是由两个或多个原子轨道混合而成。 在简单分子的化学键形成过程中,我们可以简单地考虑原子轨道的重叠。但是如果我们要讨论复杂分子中的化学键...
- 发布于 2020-10-17 13:43
- 阅读 ( 559 )
轨道(orbit)和轨道(orbital)的区别
轨道与轨道的关键区别在于,轨道是一条围绕中心点有固定路径的环形路径,而轨道是围绕原子核的不确定区域。 虽然术语“轨道”和“轨道”听起来相似,但这是两个不同的术语。轨道一词主要与行星有关,而轨道一词则...
- 发布于 2020-10-23 03:43
- 阅读 ( 450 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
分子轨道和原子轨道的关键区别在于,原子轨道描述的是原子中找到电子的概率很高的位置,而分子轨道描述的是分子中电子的可能位置。 利用薛定谔、海森堡和保罗·狄拉克提出的新理论,人们以一种新的方式来理解分子...
- 发布于 2020-10-24 07:58
- 阅读 ( 561 )
1秒(1s)和2s轨道(2s orbital)的区别
1秒(1s)和2s轨道(2s orbital)的区别 原子是物质的最小单位。换句话说,所有物质都是由原子构成的。原子由亚原子粒子组成,主要是质子、电子和中子。质子和电子使原子核位于原子中心。但是电子被定位在位于原子核外的轨道...
- 发布于 2020-10-25 04:49
- 阅读 ( 585 )
结合(bonding)和反键分子轨道(antibonding molecular orbitals)的区别
成键与反键分子轨道 这两种分子轨道间的化学键可以用化学键和分子轨道键的不同来解释。键和反键分子轨道之间最显著的区别是它们相对于母原子轨道的能级。这种能级差异导致了两个分子轨道之间的其他差异。 成键和反...
- 发布于 2020-10-26 19:13
- 阅读 ( 646 )