主要区别
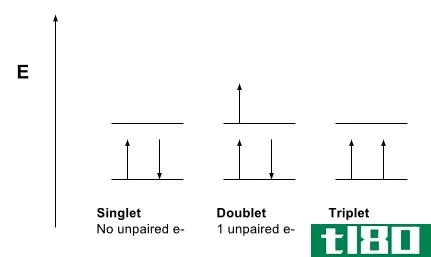
基态和激发态的主要区别在于,在原子基态中,电子处于最低能级,而在激发态时,原子中的电子比基态含有更高的能量。
基态(ground state) vs. 激发态(excited state)
基态是原子中电子能量最低的状态,而激发态是电子比基态能量更高的状态。在基态,一个系统被称为零能量;另一方面,在激发态,系统被称为具有更高的能量。
基态电子是高度稳定的,只要原子稳定就可以保持这种状态;相反,处于激发态的电子是高度不稳定的。基态电子具有较高的寿命,而激发态电子的寿命较短。
对于处于基态的电子,电子和原子核之间的距离是最小和最短的距离;然而,在激发态,电子和原子核之间的距离要大一些。在基态,电子处于它们的最低能级,而在激发态,电子处于较高的能级。
一个电子必须以光子的形式损失能量,才能接近更低的能级才能达到基态,但要达到激发态,电子会被激发并获得能量,因此,它会将最低能级留给更高的能级。
比较图
什么是基态(ground state)?
基态被称为原子的所有成分都处于其最低可能能级的状态。因此,在基态下,系统被称为具有零能量状态,其中电子为零能量,并且被发现更稳定。
它是一种原子中电子能量最低的状态,只要原子稳定,它就可以保持这种状态。因此,原子不再回到任何进一步的状态,而是保持在基态。这就是导致电子基态寿命更高的原因。量子场论中基态的另一个术语是真空态。
由于一些原子和分子含有一个以上的基态,一些原子在基态或激发态的倾向上可能具有不同的能力。其中一些有两个基态,在那里电子发现自己是稳定的。
对于有两个基态的原子,有一个特定的原子称为简并。例如,在氢的情况下,有两个基态,并且已知简并。原子或分子的退化是由一个非平凡幺正算符与哈密顿算符与特定系统的交换所导致的。对于包含较低温度或零温度的系统,已知处于基态。
对于处于基态的电子,电子和原子核之间的距离是最小和最短的距离,因为它们位于原子中,因为低能级离原子核更近。因此,在这些能级中发现了稳定的能量电子,也就是说,这些电子位于它们的最低能级。
如果电子已经处于激发态,通过吸收能量达到基态。因此,这些电子以光子的形式损失能量,以接近更低的能级。现在,有一些元素及其相对基态配置的例子。和锂一样,基态配置将是1s22s1。
什么是激发态(excited state)?
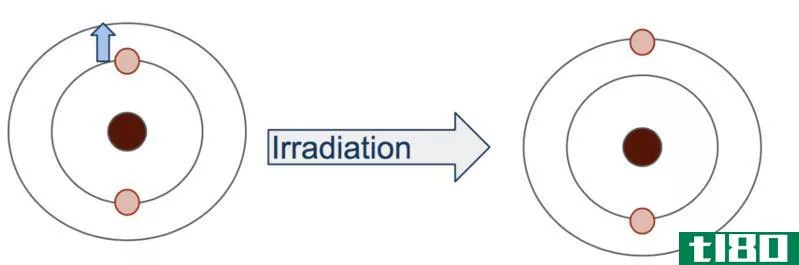
相反地,激发态被称为原子的所有组成部分都处于比基态低能级更高的能级的状态。因此,在激发态,一个系统被称为有一个更高的能量状态,其中电子有更高的能量,因此被发现不太稳定。因此,在原子的这个能级上,这些电子不能长时间保持这种状态,而是释放能量,达到稳定状态。
激发态总是倾向于失去能量而变成基态。这是因为,在激发态下,这些电子会调整它们的能量。它会因为失去能量而回到一个较低的能量状态,而能量是它在基态吸收到激发态的。这种失去能量并回到基态的过程被称为衰变,这就是这些激发态电子寿命较短的原因。
处于基态的原子是用能量激发的;激发电子的能量应该等于两个能级之间的差。如果减少,激发过程将无法完成,电子将保持在那个能级。
对于处于激发态的电子,电子和原子核之间的距离更大,因为这些电子所在的壳层位于外层区域。因此,高能电子在这些能级中被发现,它们在高能中的位置有关。
电子必须获得能量才能达到激发态。因此,在获得能量后,它们从较低的能量水平转移到更高的能量水平。此时,以锂为例说明它们的相对激发态构型。在锂中,激发态组态为1s23p1。
主要区别
- 基态是原子中电子所含能量最低的状态,相反,激发态是电子比基态能量更高的状态。
- 为了达到基态,电子必须失去能量才能达到较低的能级;另一方面,为了达到激发态,电子被激发离开最低能级而进入更高能级。
- 基态方法被称为零能量;另一方面,激发态系统被称为具有更高的能量。
- 基态电子是高度稳定的;然而,处于激发态的电子是高度不稳定的。
- 基态电子具有较高的寿命;相反,激发态电子的寿命较短。
- 处于基态的电子与原子核的距离最小;然而,在激发态下,电子与原子核之间的距离更大。
- 在基态,电子处于最低能级;另一方面,在激发态,电子处于较高的能级。
结论
基态是电子在原子中能量最低且趋于高度稳定的状态,但激发态是电子比基态能量更高、稳定性更低的状态。