生成热和反应热的关键区别在于,生成热是在标准条件下形成一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。
生成热和反应热是化学反应的重要焓值。我们将这些术语定义为标准条件,即标准压力和标准温度。在这里,热或焓是在化学反应过程中从系统中释放或被系统吸收的能量。
目录
1. 概述和主要区别
2. 什么是生成热
3. 什么是反应热
4. 并列比较-生成热与反应热的表格形式
5. 摘要
什么是生成热(heat of formation)?
生成热是在标准条件下纯元素形成一摩尔物质过程中焓的变化。在这里,标准条件是1大气压和298.15开尔文温度。因为我们考虑一摩尔的形成,这个能量的单位是kJ/mol。这个能量要么是形成反应释放的能量,要么是反应在前进过程中消耗的能量。这个焓的方程如下:;
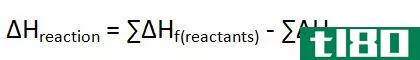
这里,∆是一个符号,表示焓的变化,H是能量的量,f表示生成反应。在这个反应中,所有成分都在标准条件下,否则就不是生成热。例如,二氧化碳的形成如下。
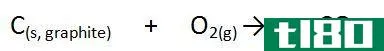
碳的纯元素形式是石墨,氧的来源是双原子氧分子。当我们在标准条件下进行生成反应,测量焓的变化,我们称之为生成热。
什么是反应热(heat of reaction)?
反应热是在恒定压力下发生的反应的焓的变化。我们以kJ/mol为单位测量能量差,它给出了在化学反应中释放或吸收的能量。这个焓变的符号是∆H。如果这个值是正值,我们称之为吸热反应。如果值为负,我们称之为放热反应。热焓变化的方程如下:;

生成热(heat of formation)和反应热(heat of reaction)的区别
生成热是在标准条件下纯元素形成一摩尔物质过程中焓的变化。焓变化的符号为∆Hf。反应热是在恒定压力下发生的反应的焓的变化。焓变的符号为∆H。

总结 - 生成热(heat of formation) vs. 反应热(heat of reaction)
焓是能量的含量。焓的变化反映了反应物、产物和周围环境之间的能量交换量。生成热和反应热的区别在于,生成热是在标准条件下形成一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。