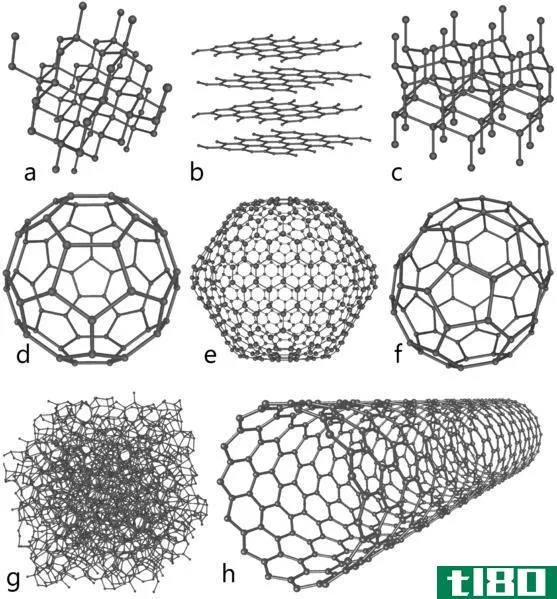
Q碳与金刚石的主要区别在于Q碳(或淬火碳)具有随机结构,而金刚石具有金刚石立方晶体结构。
碳和金刚石是碳的同素异形体。同素异形体是同一化学元素的不同结构形式。另一种常见的碳同素异形体是石墨。此外,钻石被认为是地球上最坚硬的材料。然而,根据最新研究,Q碳已取代金刚石成为最坚硬的物质。
目录
1. 概述和主要区别
2. 什么是Q碳
3. 什么是钻石
4. 并列比较——Q碳与金刚石的表格形式
5. 摘要
什么是q碳(q carbon)?
Q碳(淬火碳)是碳的同素异形体。这种材料是在2015年发现的。它是一种铁磁性导电材料。此外,当我们把它暴露在低能量下时,它会发光。与钻石相比,它**成本低廉。根据最近的一些研究,Q碳比金刚石硬。
此外,该材料具有随机的非晶态结构,并且具有sp2杂化碳原子和sp3杂化碳原子。此外,它的生产过程包括熔化碳(使用纳秒激光脉冲)和快速淬火。有时,这是Q碳和金刚石的混合物。
q碳的性质
- 非晶态结构
- sp2和sp3混合键合
- 独特的硬度
- 导电
- 导热
- 键长比金刚石小
- 铁磁性的
- 可以是半导体或金属
- 即使在低能量水平下也会发光
什么是钻石(diamond)?
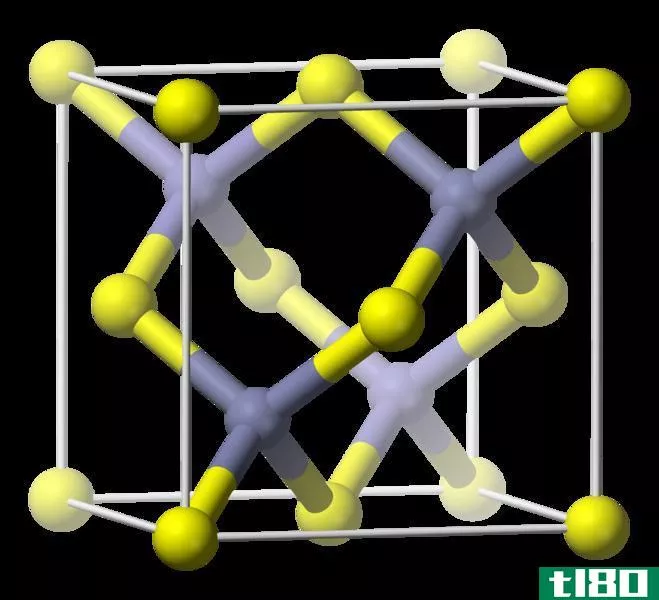
金刚石是碳的同素异形体,被认为是地球上天然存在的最坚硬的材料。它的结构是晶态的,它有金刚石立方晶体结构。此外,它的导热系数是任何天然材料中最高的。钻石是在非常高的温度和压力下在地幔中形成的(离地表100英里以下)。

图01:钻石
金刚石的性质
- 大多是棕色或黄色,但珠宝业青睐无色钻石
- 四个方向的完全八面体解理
- 含有sp3杂化碳原子
- 与工程材料相比,韧性较差。
- 超高屈服强度
- 优良的电绝缘体
- 亲脂性和疏水性
- 在室温下,金刚石不与任何化学试剂发生反应
q碳(q carbon)和钻石(diamond)的区别
碳是淬火碳,它是碳的同素异形体,而金刚石也是碳的同素异形体,被认为是地球上天然存在的最坚硬的材料。Q碳与金刚石的主要区别在于Q碳具有随机结构,而金刚石具有金刚石立方晶体结构。这些结构使Q碳成为最坚硬的材料;同时,金刚石也是地球上天然存在的最坚硬的材料。
Q碳与金刚石的一个显著区别是Q碳是一种合成的同素异形体,而金刚石则是天然存在的。此外,在Q碳中,sp2和sp3杂化碳原子都可以看到,而在金刚石中,只有sp3杂化碳原子存在。所以,我们也可以把它作为Q碳和金刚石的区别。当考虑Q碳的形成时,首先我们应该熔化碳(使用纳秒激光脉冲)并快速淬火形成Q碳,而金刚石则是在地幔中(距离地表100英里以下)形成的。

总结 - q碳(q carbon) vs. 钻石(diamond)
简言之,Q碳和金刚石是化学元素碳的同素异形体。Q碳与金刚石的主要区别在于Q碳具有随机结构,而金刚石具有金刚石立方晶体结构。此外,Q碳比金刚石硬,但金刚石是地球上天然存在的最坚硬的材料。
引用
1邓普顿,格雷厄姆。“Q-Carbon比钻石更硬,**极其简单。”ExtremeTech,2015年12月11日,可在这里查阅。“钻石”。地质学,这里有。
2“钻石”地质学,