碳是金刚石和碳的一个关键元素。
碳是一种原子序数为6,化学符号为C的化学元素,它以不同的结构存在于自然界中,我们称之为碳的同素异形体。这些结构只含有碳作为化学元素,但碳原子的空间排列是不同的。钻石也是同素异形体的一种。同素异形体的物理性质也不同。
目录
1. 概述和主要区别
2. 什么是碳
3. 什么是钻石
4. 并列比较-碳与钻石的表格形式
5. 摘要
什么是碳(carbon)?
碳是一种原子序数为6,化学符号为C的化学元素,它是一种非金属元素,位于元素周期表中的p块元素。根据碳([He]2s2 2p2)的电子构型,一个碳原子可以形成四个共价化学键。此外,这种元素有同位素(同一元素的原子有不同数量的中子)。碳最丰富和稳定的同位素是12C,而13C是稳定但不太丰富的同位素;而14C则是放射性同位素。
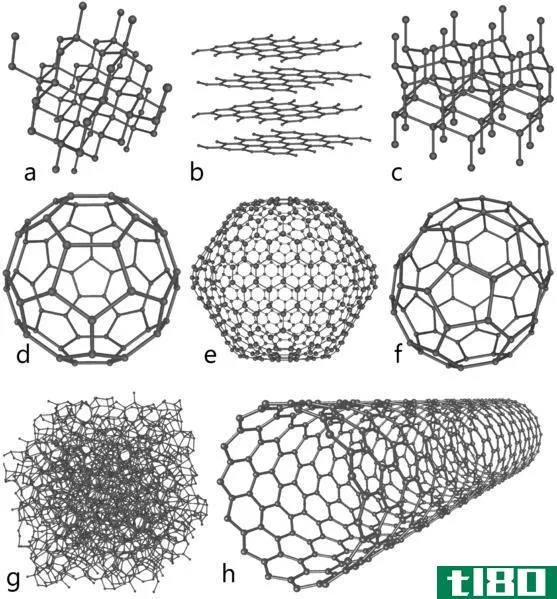
图01:碳的同素异形体
碳同素异形体是碳的不同结构形式,只有碳原子,但空间排列不同。这些都是碳的自然存在形式。最常见的例子是金刚石和石墨。虽然这两种结构都只由碳原子组成,但由于空间排列的不同,它们具有不同的物理性质。例如,钻石是透明的,而石墨是不透明的。此外,关于碳的一些其他化学事实如下:
- 原子序数是6
- 质量数为12.011
- 第14组和第2阶段
- p块元素
- 反应性非金属
- 在标准温度和压力下,它是固态的
- 升华点为3642°C
- 三相点为4600 K,10800 kPa
- 最常见的氧化状态是+4
什么是钻石(diamond)?
金刚石是碳的同素异形体。它是一种固体形式的碳,具有三维形状。此外,每个碳原子通过共价化学键与其他四个碳原子相连。这种晶体结构被称为“金刚石立方”结构。此外,在所有天然材料中,这种化合物具有最高的硬度和热导率。因此,金刚石在工业中被广泛用于切割和抛光工具。

图02:金刚石与石墨
关于钻石的一些重要事实如下:
- 属于天然矿物的范畴
- 重复单元为碳纤维
- 公式质量为12.01 g/mol
- 颜色通常为黄色、棕色或灰色至无色
- 骨折不规则/不均匀
- 而且,它的矿物条纹是无色的
碳(carbon)和钻石(diamond)的区别
碳是原子序数为6,化学符号为C的化学元素,而金刚石是碳中最强的同素异形体。碳和金刚石的主要区别在于碳是一种化学元素,而金刚石是碳的同素异形体。此外,碳的外观取决于同素异形体的类型,例如石墨颜色较深且不透明,而钻石则为透明,呈现典型的黄色、棕色或灰色至无色。尽管大多数碳的同素异形体的强度较低,但金刚石是地球上天然存在的最坚固的材料。
下表列出了碳和金刚石的区别。

总结 - 碳(carbon) vs. 钻石(diamond)
碳有许多共同的同素异形体,而其中最强的结构是金刚石。因此,碳和金刚石的关键区别在于碳是一种化学元素,而金刚石是碳的同素异形体。
引用
1“碳”,维基百科,维基媒体基金会,2019年4月26日,可在这里查阅。“钻石。”地质学.com,此处提供。
2“钻石。”地质学.com,