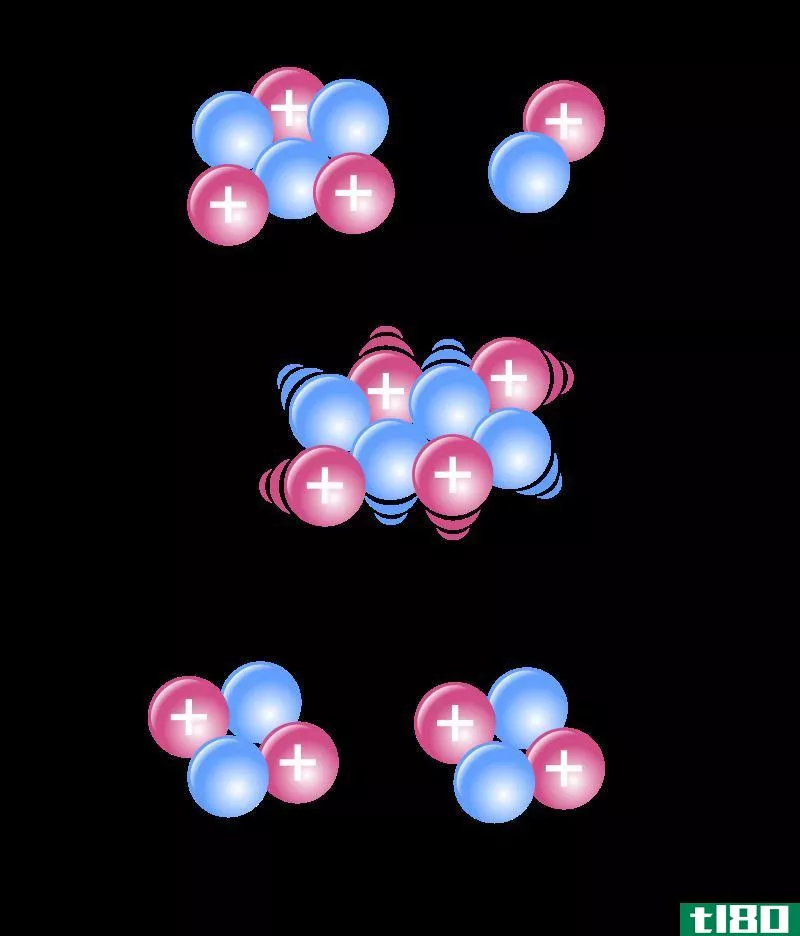
结合(combination)和分解反应(decomposition reaction)的区别
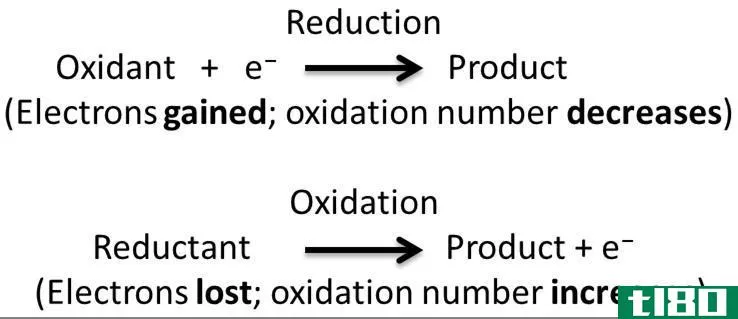
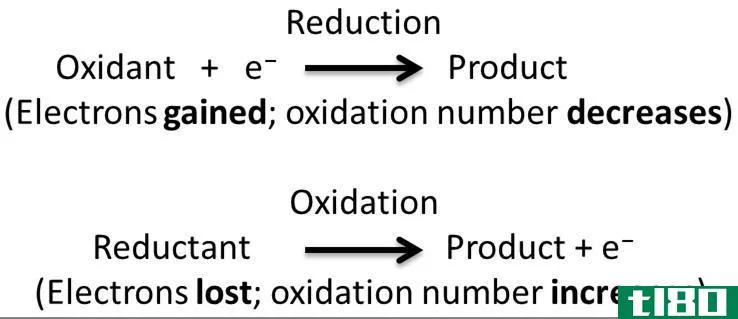
化学反应是将一种或多种化合物转化为一种或多种不同的产物,从而改变化合物的特性。化学反应的起始物质称为反应物,生成的化合物称为产物。在化学反应过程中,由于化合物原子间的键以不同的方式断裂和生成,所以化合物的分解或化合物的结合以及新化合物的形成都会发生。化学反应可分为几大类。其中氧化还原反应或氧化还原反应是非常重要的。氧化和还原反应称为电子转移反应,因为反应物的电子从一种化合物转移到另一种化合物以引起反应。在氧化还原反应中,同时发生两个平行的反应,称为半反应。这些半反应显示了电子的转移。通过平衡这些半反应,我们可以猜测在最后发生的总体反应。复合反应和分解反应是氧化还原反应的两种主要类型。合成反应和分解反应的主要区别在于,合成反应是将反应物组合成一个单一产物,而分解反应是将单一化合物分解成两个或两个以上的产物。
内容1。概述和主要区别2。什么是组合反应3。什么是分解反应4。并列比较-组合与分解反应5。摘要
什么是混合反应(a combination reaction)?
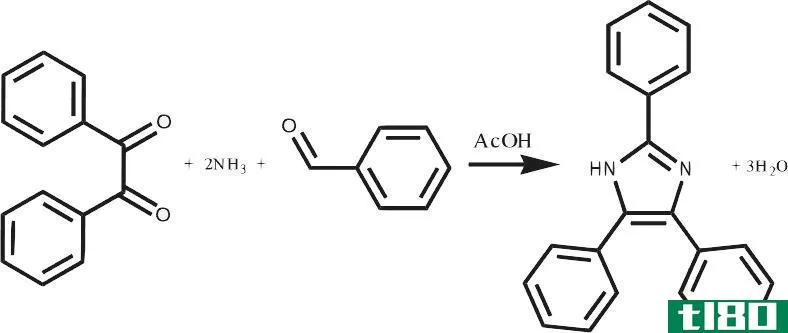
合成反应,又称合成反应,是反应物化合物结合形成不同的化合物作为产物的反应。换句话说,简单分子的反应产生复杂的分子。该化合物的某些或全部原子间的键被破坏;同时,原子将结合形成新的化合物,即产物。在分解反应中,同一反应物作为两个半反应的起始原料。与分解反应不同,组合反应中的半反应有不同的反应物。合成反应生成单一产物。下面是一个常见的例子,可以作为燃烧反应给出。
例如,当铝(Al)置于液态溴(Br2)中时,发生组合反应并生成溴化铝(AlBr3)。在这里,氧化数在铝中增加,在溴中减少。因此,这是一个氧化还原反应,是一个结合反应,因为两个反应物反应得到一个特定的产物。

图01:组合反应
什么是分解反应(decomposition reaction)?
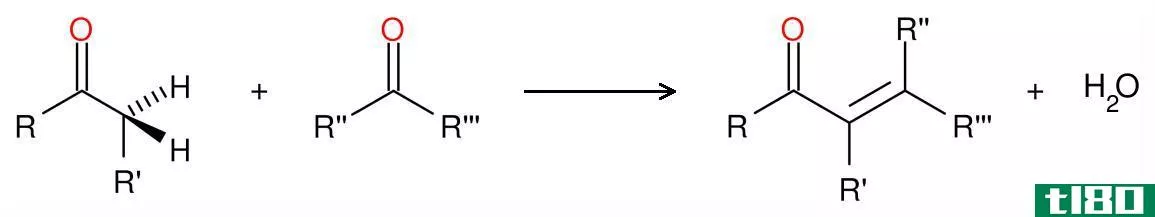
分解反应是氧化还原反应中的另一个重要反应。它基本上与组合反应相反。分解反应是反应物化合物分解成产物的反应。在这里,一半的反应与氧化反应和还原反应同时发生。但与组合反应不同,在分解反应中,两个半反应的反应物是相同的。分解反应产生几种产物。
在水的电解过程中,当直流电通过水时,水分子被分解产生氧气和氢气。在这里,氧化数在氧原子中增加,在氢原子中减少。因此,它是一个氧化还原反应和分解反应,由于水分子分解成氧气和氢气。

图02:组合与分解
结合(combination)和分解反应(decomposition reaction)的区别
| 结合与分解反应 | |
| 两种或两种以上的反应物参与组合反应。 | 一种化合物参与分解反应。 |
| 产品 | |
| 合成反应生成单一产物。 | 分解反应产生几种产物。 |
| 半反应 | |
| 在组合反应中,两个半反应有两个不同的起始分子。 | 在分解反应中,一个单分子作为两个半反应的起始原料。 |
| 化学键 | |
| 结合反应导致原子键合以产生单一的最终产物。 | 在分解反应中,化学键被分解成两个或两个以上的最终产物。 |
| 分子 | |
| 组合反应使简单分子发生反应并产生复杂分子。 | 分解反应使复杂的分子分解成简单的分子。 |
总结 - 结合(combination) vs. 分解反应(decomposition reaction)
氧化还原反应是我们周围世界的一部分,因为大多数重要的化学反应都是氧化还原反应。合成反应和分解反应是相互对立的简单反应。结合反应与分解反应的主要区别在于,组合反应是指两个或两个以上反应物分子的结合,得到一个单一的最终产物,而分解反应则是将单个分子分解成两个或两个以上的产物。
R参考文献:1.Chang,R.,2010年。化学。第10版,纽约:McGraw-Hill.2.氧化还原。(2009年7月30日)。2017年5月29日检索自https://weakinteracti***.wordpress.com/primers/redox/3.Reacti***。(未注明)。2017年5月29日检索自http://www.ric.edu/faculty/ptiskus/reacti***/