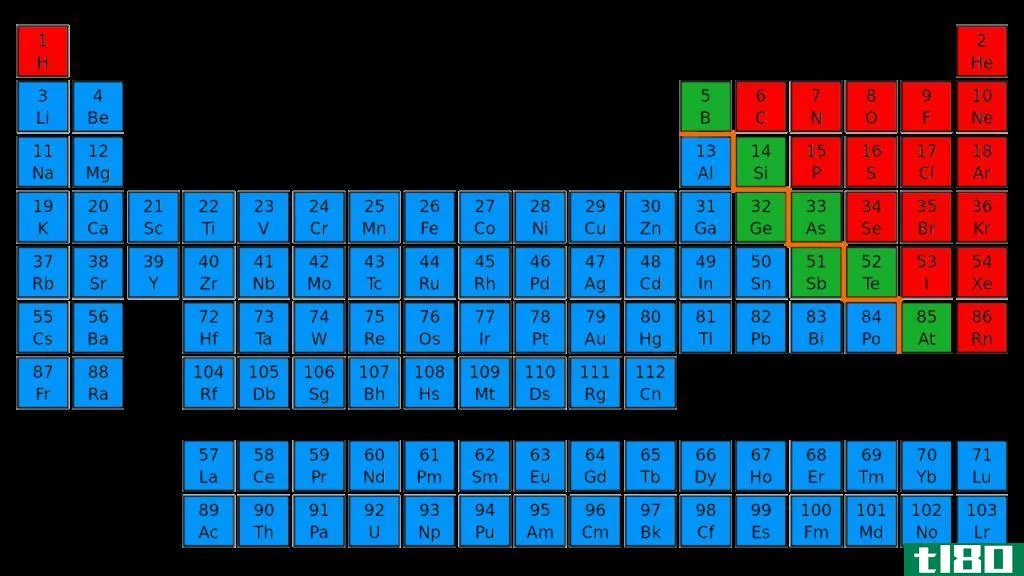
第1族金属与过渡金属的主要区别在于,第1族金属形成无色化合物,而过渡金属形成有色化合物。
第1类金属也被称为碱金属,因为这些元素可以形成碱性化合物。然而,元素周期表的第1组含有非金属氢。另一方面,过渡金属是d块元素,但并非所有d块元素都是过渡金属。第1组金属和过渡金属相似,因为它们都有未成对电子。
目录
1. 概述和主要区别
2. 什么是第一组金属
3. 什么是过渡金属
4. 并列比较——1组金属与过渡金属的表格形式
5. 摘要
什么是第1组金属(group 1 metals)?
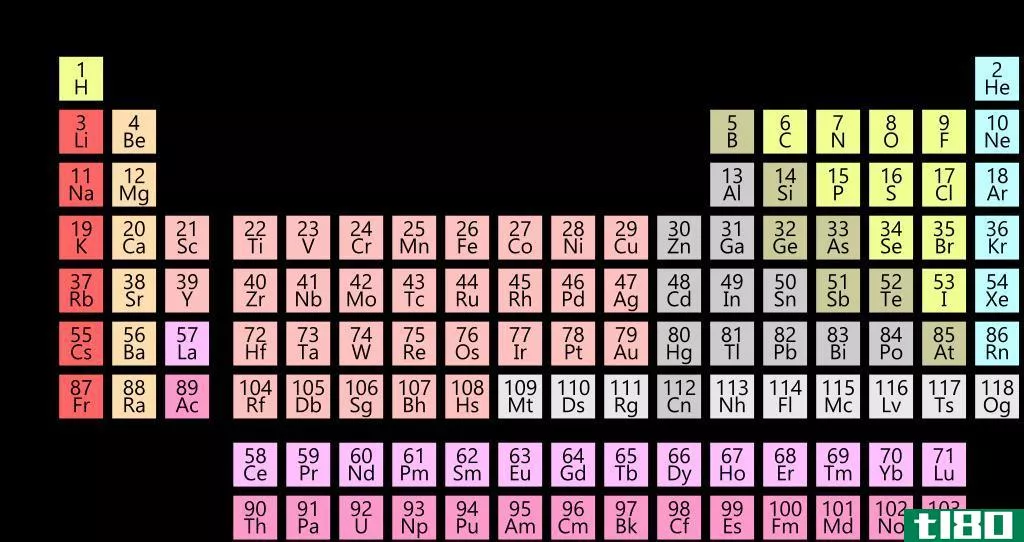
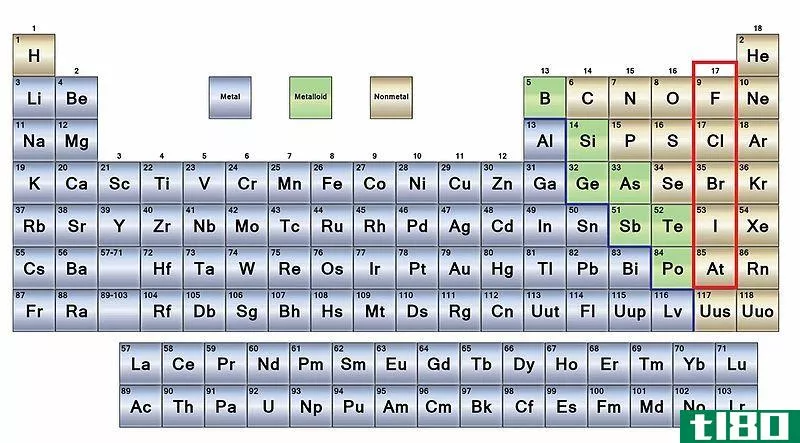
第一类金属是在s轨道最外层有一个不成对电子的化学元素。这些金属之所以被称为碱金属,是因为它们在水中溶解时会形成碱性化合物。我们可以在周期表s块的第一列观察到这些元素。第1组金属的成员如下:
- 锂(Li)
- 钠(Na)
- 钾(K)
- 铷(Rh)
- 铯(Cs)
- 弗朗(法国)
Group 1 metals are all shiny, highly reactive, and very soft (we can easily cut them using a simple knife). Generally, the metals in this group show low densities, low melting points, low boiling points and have body-centred cubic crystal structures. Furthermore, they have distinct flame colours, so we can easily distinguish them by exposing a sample to a Bunsen burner.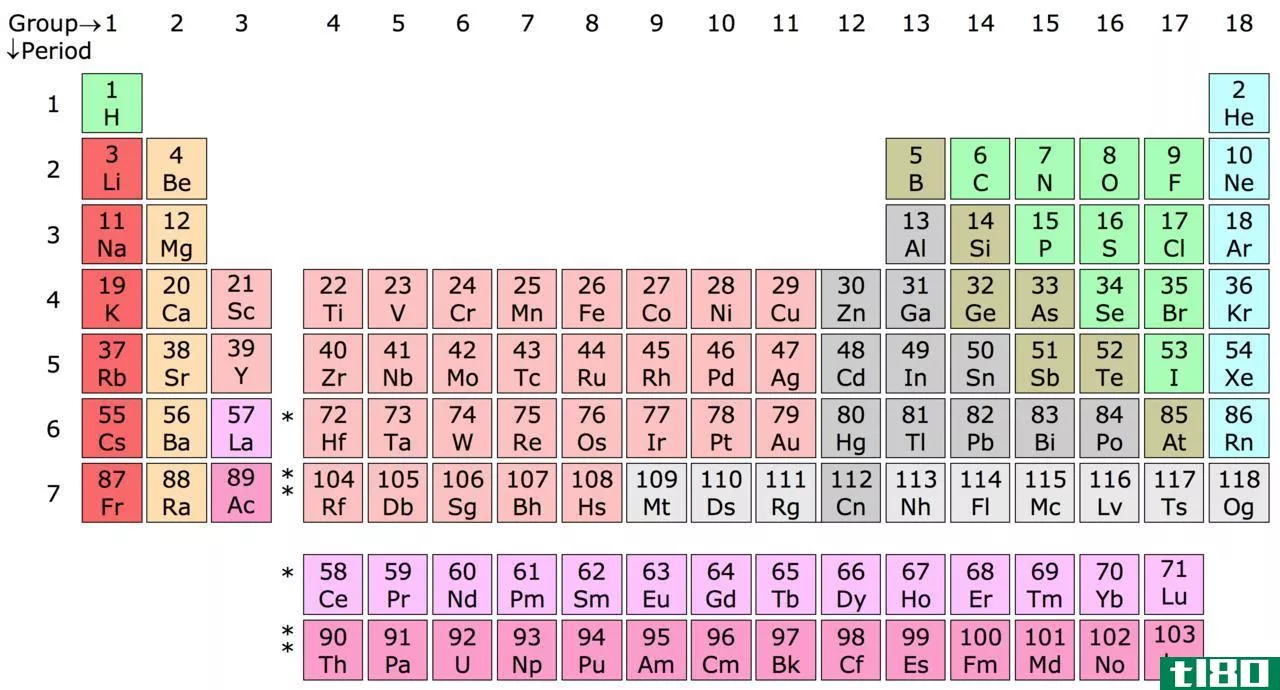
此外,第1组金属之间存在一些周期性变化。例如,当进入该族时,元素的原子尺寸增大,熔点和沸点降低,密度增加,第一电离能增加,反应性降低,等等。
什么是过渡金属(transition metals)?
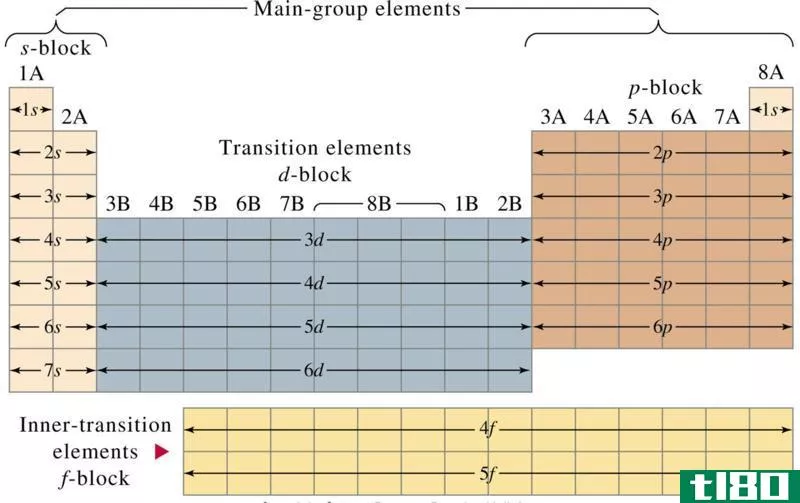
过渡金属是一种化学元素,其原子具有不成对的d电子。在这些元素中,至少它们形成的稳定阳离子应该有不成对的电子。因此,大多数d块体元素是过渡金属。我们不能认为钪和锌是过渡金属,因为它们即使在稳定的阳离子中也没有未配对的电子。这些原子有d电子,但它们都是成对电子。

此外,过渡金属元素可以形成不同颜色的化合物。这些元素之所以具有这种能力,是因为这些元素可以有不同的氧化状态,它们非常丰富多彩。这些化学元素的不同氧化状态可以有不同的颜色。此外,这些颜色是由于d-d电子跃迁而产生的。此外,由于这些未配对电子的存在,这些金属要么是顺磁性的,要么是铁磁性的。几乎所有这些元素都能与配体结合形成配位络合物。
第1组金属(group 1 metals)和过渡金属(transition metals)的区别
第1类金属和过渡金属彼此不同,主要取决于它们形成的化合物的颜色。也就是说,第1组金属和过渡金属之间的关键区别在于,第1组金属形成无色化合物,而过渡金属形成彩色化合物。
此外,第1族金属是在最外层的s轨道上有一个不成对电子的化学元素,而过渡金属是具有不成对d电子的原子的化学元素。
下面的信息图表更详细地列出了第1组金属和过渡金属之间的差异。
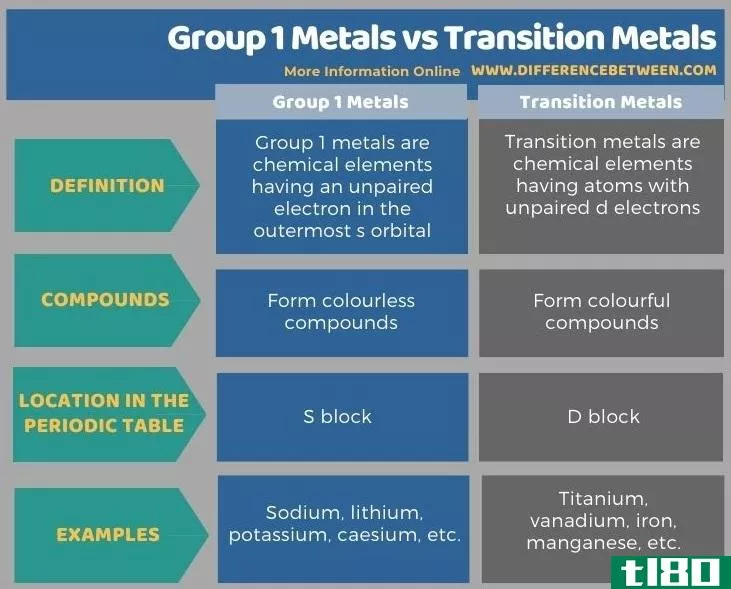
总结 - 第1组金属(group 1 metals) vs. 过渡金属(transition metals)
第1类金属和过渡金属彼此不同,主要取决于它们形成的化合物的颜色。第1族金属与过渡金属的主要区别在于,第1族金属形成无色化合物,而过渡金属形成有色化合物。
引用
1科顿,艾伯特。“过渡金属”,不列颠百科全书,不列颠百科全书,2019年4月3日,可在此处查阅。