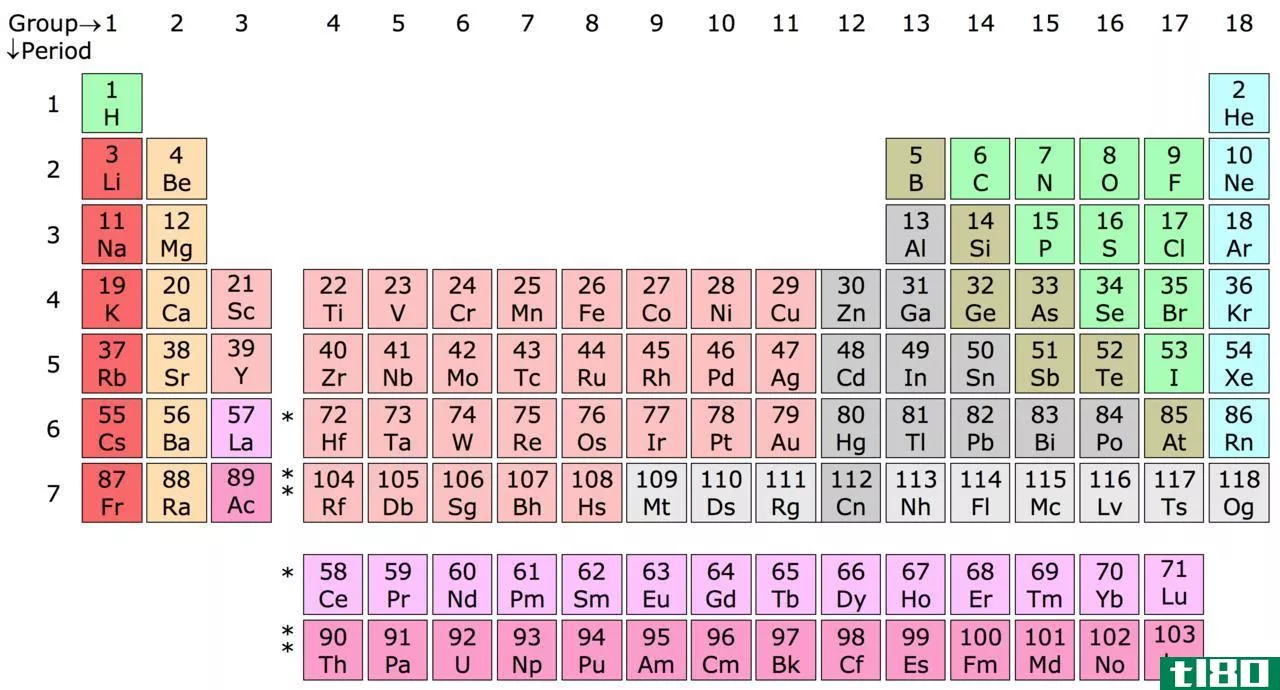
过渡金属与类金属的主要区别在于,过渡金属是具有不成对d电子原子的化学元素,而类金属则是具有介于金属和非金属之间性质的化学元素。
过渡金属本质上是金属元素。但是,并不是所有的金属都是过渡金属,因为它必须满足这样一个事实:原子有不成对的电子,原子才能变成过渡金属。另一方面,非金属也不是。然而,它们的化学和物理性质介于金属和非金属之间。
目录
1. 概述和主要区别
2.什么是过渡金属
3. 什么是类金属
4. 并列比较-过渡金属与类金属的表格形式
5. 摘要
什么是过渡金属(transition metals)?
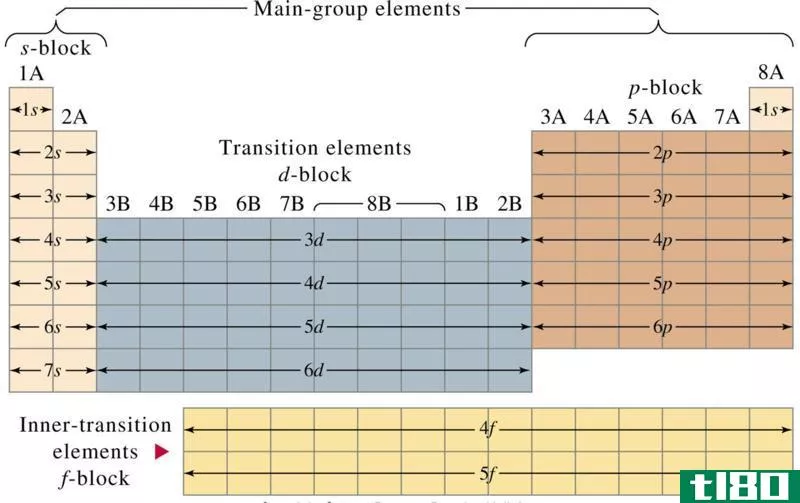
过渡金属是一种化学元素,其原子具有不成对的d电子。至少,它们形成的稳定阳离子应该有不成对的电子。此外,d块体元素大多为过渡金属。然而,我们并不认为钪和锌是过渡金属。这是因为,即使在它们稳定的阳离子中也没有任何未配对的电子。这些原子有d电子,但它们都是成对电子。

图01:过渡金属的彩色化合物
此外,过渡金属元素可以形成不同颜色的化合物。主要是因为这些元素的氧化状态非常不同。这些化学元素的不同氧化状态可以有不同的颜色。这些颜色是由d-d电子跃迁产生的。此外,由于这些未配对电子的存在,这些金属要么是顺磁性的,要么是铁磁性的。几乎所有这些元素都能与配体结合形成配位络合物。
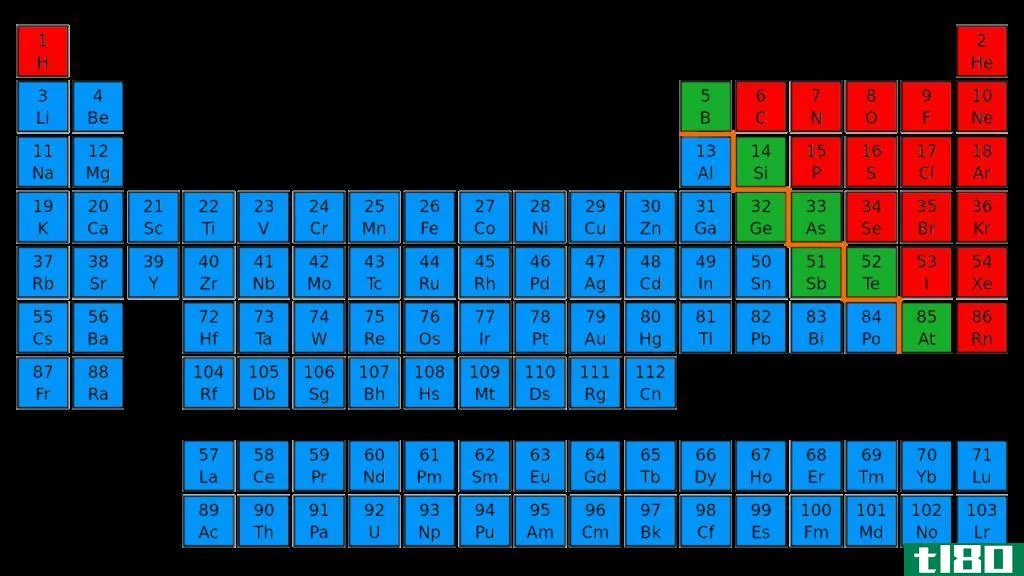
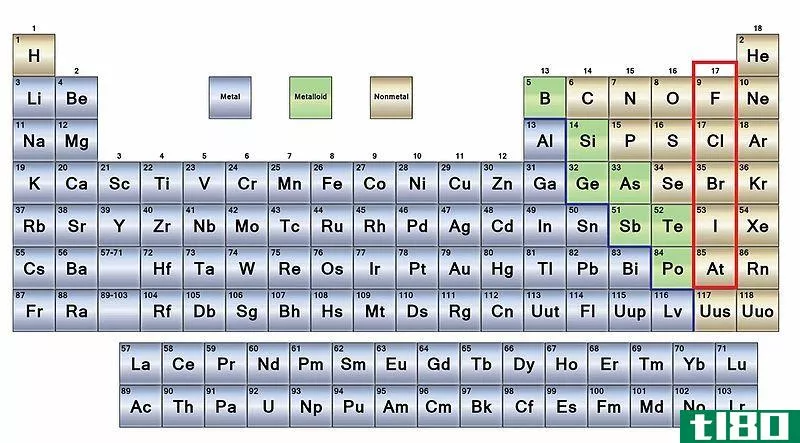
什么是类金属(metalloids)?
类金属是指在金属和非金属之间具有性质的化学元素。大多数时候,它们都是金属和非金属的混合体。常见金属有六种;
- 硼
- 硅
- 锗
- 砷
- 锑
- 碲
通常,这些元素具有金属外观。但它们非常易碎,而且是不良的导电体。当考虑到它们的化学性质时,它们大多与非金属有关,而不是金属。其他物理性质是介于金属和非金属之间的。这些化学元素在生产合金、生物制剂、催化剂、玻璃等方面都很重要。更重要的是,我们可以将它们用于生产半导体,特别是硅和锗。

图02:半导体电子元件
这些类金属主要以固相形式存在,并且有光泽。它们具有中等电离能,电负性值约为2.0。当考虑到它们的氧化物形式时,它们是两性的或弱酸的。
过渡金属(transition metals)和类金属(metalloids)的区别
过渡金属是具有不成对d电子的原子的化学元素,而类金属则是具有介于金属和非金属之间性质的化学元素。这就是过渡金属和类金属之间的关键区别。过渡金属和类金属之间的另一个区别是,过渡金属具有金属性质,与类金属相比具有很高的导电性,因为类金属由于具有中等导电能力而作为半导体很常见。
导致过渡金属和类金属之间区别的另一个特性是硬度。通常,过渡金属的硬度较高,而类金属则更脆。重要的是,类金属的化学性质与非金属有关,而过渡金属具有金属的一般化学性质。
下面的信息图表更详细地列出了过渡金属和类金属之间的区别。
总结 - 过渡金属(transition metals) vs. 类金属(metalloids)
过渡金属是金属的一个子类。类金属根据其化学和物理性质是金属和非金属的中间化学元素。过渡金属与类金属的主要区别在于,过渡金属是具有不成对d电子的原子的化学元素,而类金属是介于金属和非金属之间的化学元素。
引用
1“过渡金属”,维基百科,维基媒体基金会,2018年10月6日。这里有2个。“类金属”,维基百科,维基媒体基金会,2018年10月6日。可在此处查阅
2“类金属”,维基百科,维基媒体基金会,2018年10月6日