离子键合和金属键合的关键区别在于,离子键合发生在正离子和负离子之间,而金属键合发生在正离子和电子之间。
正如美国化学家G.N.Lewis所说,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。这些原子趋向于相互反应以变得稳定。因此,每一个原子都可以实现稀有气体的电子组态。这是通过形成离子键、共价键或金属键来实现的。
目录
1. 概述和主要区别
2. 什么是离子键
3. 什么是金属键合
4. 并列比较-离子键与金属键的表格形式
5. 摘要
什么是离子键合(ionic bonding)?
原子可以获得或失去电子,并分别形成负电荷或正电荷粒子。这些粒子是“离子”。这些离子之间存在静电相互作用。因此,离子键是这些带相反电荷的离子之间的吸引力。
离子键中原子的电负性影响静电相互作用的强度。因此,电负性可以测量原子对电子的亲和力。高电负性的原子可以从低电负性原子中吸引电子形成离子键。
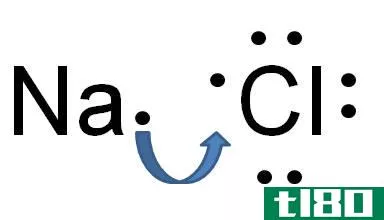
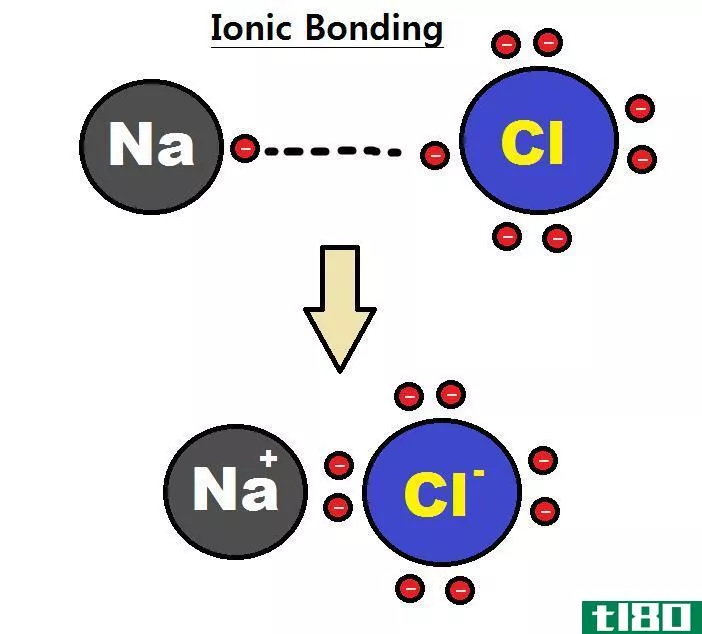
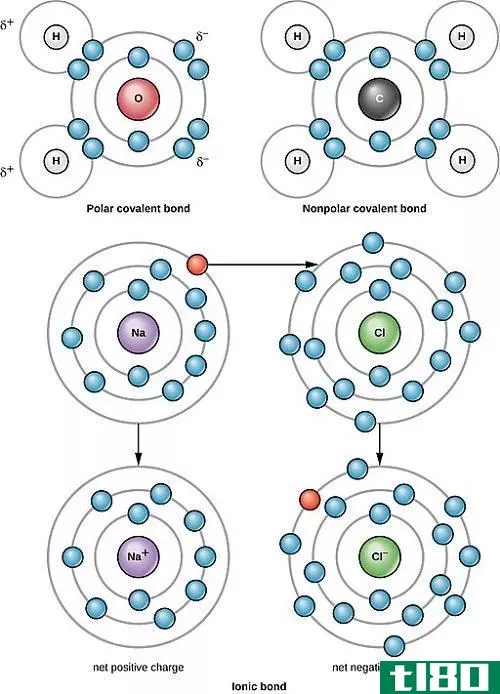
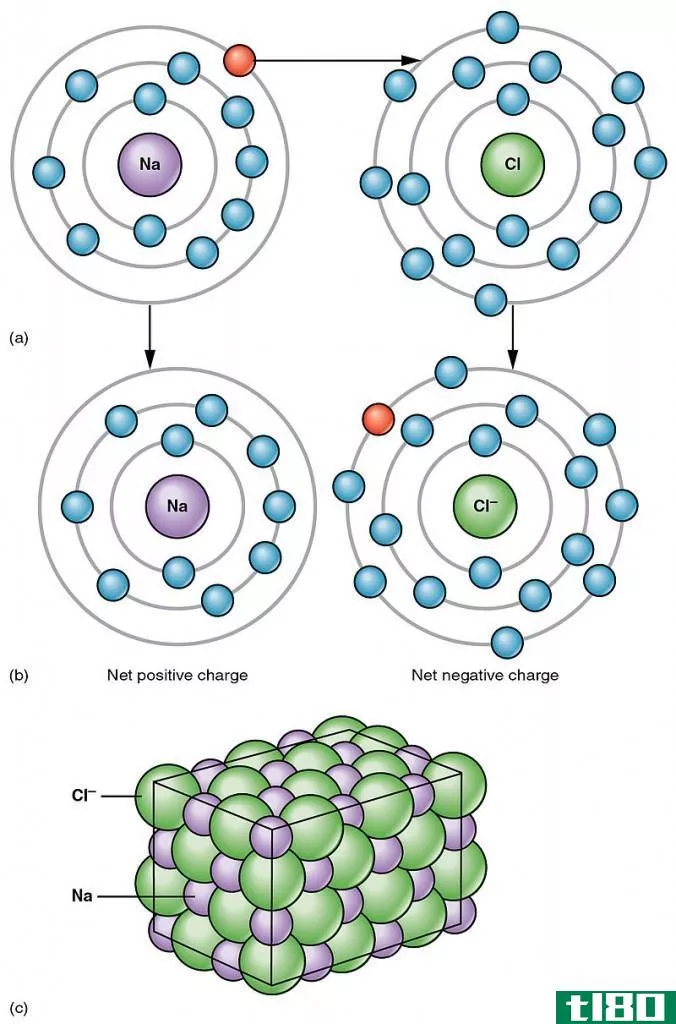
图01:离子键合
例如,氯化钠在钠离子和氯离子之间有一个离子键。钠是一种金属,因此它的电负性(0.9)比氯(3.0)低。由于这种电负性的差异,氯可以从钠中吸引一个电子,形成氯离子和钠离子。因此,两个原子都获得了稳定的惰性气体电子组态。Cl-和Na+被吸引的静电力结合在一起,从而形成离子键。
什么是金属键合(metallic bonding)?
金属是原子,可以通过除去电子而形成阳离子。族1,族2和过渡元素是金属。大多数情况下金属是固相。金属原子间的键形式是“金属键”。
金属在外层释放电子,这些电子分散在金属阳离子之间。因此,我们称之为“离域电子之海”。电子和阳离子之间的静电相互作用称为金属键合。

图02:金属连接
金属原子释放到海里的电子数和阳离子的大小决定了金属键的强度。阳离子的大小与键的强度成反比,金属原子释放的电子数也与金属键的强度成正比。
此外,电子可以移动,因此,金属具有导电的能力。由于金属键合,金属具有有序的结构。金属的高熔点和沸点也是由于这种牢固的金属结合。由于同样的原因,金属是坚固而不易碎的。
离子键合(ionic bonding)和金属键合(metallic bonding)的区别
离子键合是发生在两个相反带电离子之间的化学键,而金属键是发生在金属晶格中的化学键。因此,离子键合和金属键合的关键区别在于,离子键合发生在正离子和负离子之间,而金属键合发生在正离子和电子之间。
作为离子键和金属键的另一个重要区别,我们可以考虑原子的电负性对键强度的影响。也就是说,电负性对金属键合没有影响,因为键合涉及到同一类型的原子,但离子键合中正负离子的电负性差异对键合强度有很大影响。此外,离子键合比金属键合强得多。
下面关于离子键和金属键之间区别的信息图显示了两种键之间的更多差异。
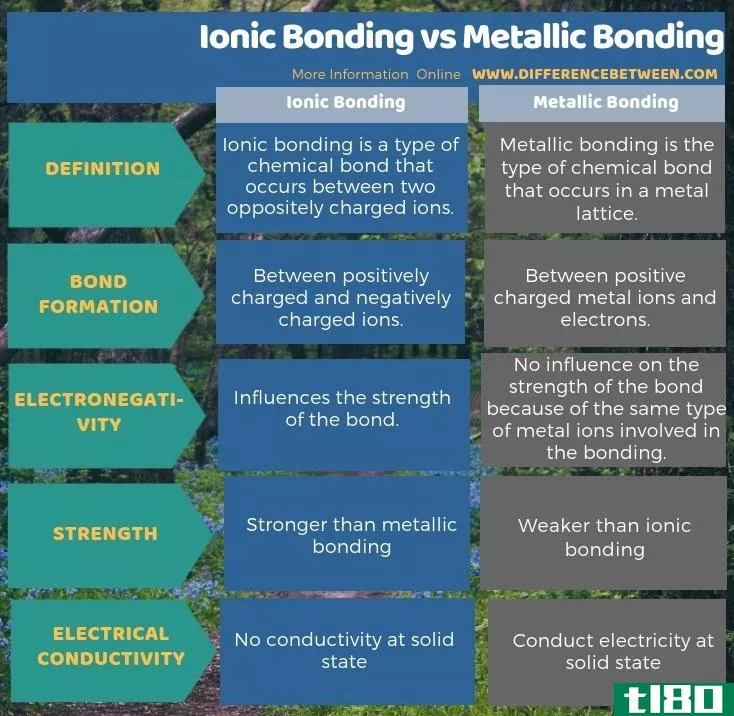
总结 - 离子键合(ionic bonding) vs. 金属键合(metallic bonding)
化学键合主要有三种类型。它们是离子键、共价键和金属键。离子键合和金属键合的关键区别在于,离子键合发生在正离子和负离子之间,而金属键合发生在正离子和电子之间。
引用
1歌词。“离子和共价键”,化学图书馆,国家科学基金会,2018年2月28日。这里有2个。歌词。“金属键合”,化学剧本,国家科学基金会,2018年7月31日。此处提供
2歌词。“金属键合”,化学剧本,国家科学基金会,2018年7月31日。