硝酸和亚硝酸的关键区别在于,硝酸分子包含三个与中心氮原子结合的氧原子,而亚硝酸分子包含两个与中心氮原子结合的氧原子。
硝酸和亚硝酸是氮的无机酸。这两种酸都含有氮、氧和氢原子。
目录
1. 概述和主要区别
2. 什么是硝酸
3. 什么是亚硝酸
4. 并列比较-硝酸与亚硝酸的表格形式
5. 摘要
什么是硝酸硝酸(nitric acid)?
硝酸的化学式为硝酸。它是一种腐蚀性很强且危险的酸。此外,它可以具有稀释或浓缩的化学性质。不管怎样,它都有硝酸分子溶解在水中。二氧化氮和水的反应形成硝酸。硝酸有两种类型:发烟硝酸和浓硝酸。

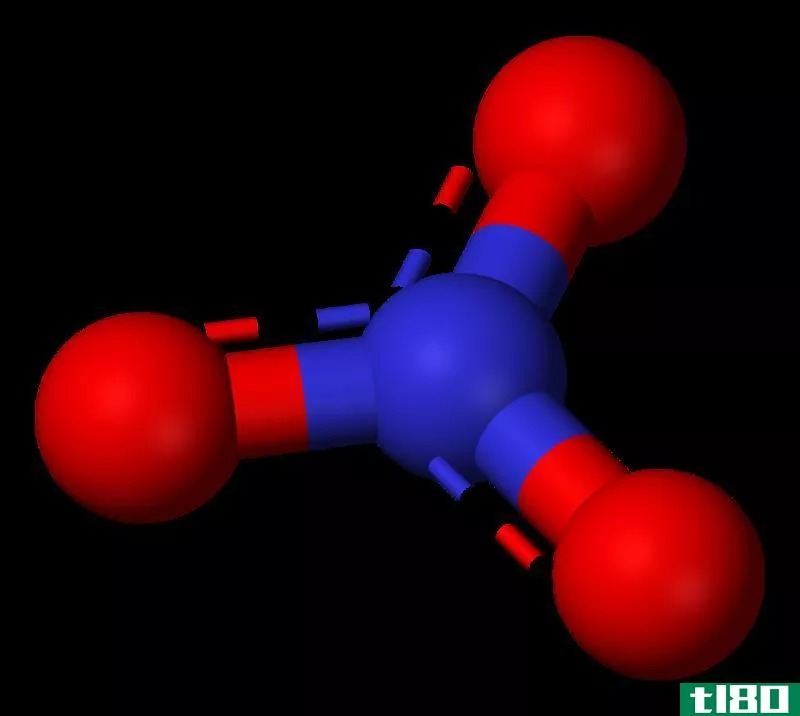
图01:硝酸分子的共振结构
发烟硝酸是一种商业级硝酸,具有很高的浓度和密度。它含有90-99%的硝酸。我们可以通过在硝酸中加入过量的二氧化氮来制备这种液体。它形成无色、淡黄色或褐色的发烟液体,具有很强的腐蚀性。因此,这种酸性溶液中含有与水结合的气态分子,其中没有水。这种酸的烟雾从酸的表面升起;这导致了它的名字“烟化”。该化合物的化学式为HNO3-xNO2。
浓硝酸是一种在较少的水中含有较多硝酸的溶液。这意味着这种酸的浓缩形式所含的水比其中的溶质少。在商业规模中,68%或以上被认为是浓硝酸。此外,该溶液的密度为1.35g/cm3。如此高的浓度不会产生烟气,但这种酸的浓度非常高,可能会产生淡白色的烟气。我们可以通过二氧化氮和水反应来生产这种液体。
什么是亚硝酸(nitrous acid)?
亚硝酸是一种无机酸,化学式为HNO2。它是一种弱酸和一元酸。这种酸以溶液状态、气相和丁腈盐的形式出现。这种酸可用于**重氮盐,重氮盐是偶氮偶合反应生成偶氮染料的试剂。

图02:亚硝酸的结构
亚硝酸溶液呈淡蓝色。这种酸的共轭碱是腈离子。在气相中,亚硝酸呈平面形状,可以采用顺式和反式两种形式。在室温下,反式异构体占优势,并且比顺式异构体稳定。
亚硝酸可由亚硝酸钠水溶液与矿物酸酸化制备。我们可以在冰温下进行酸化过程,在原位条件下消耗HNO2。游离亚硝酸分子不稳定,容易迅速分解。此外,我们还可以通过溶解三氧化二氮制备亚硝酸。
硝酸硝酸(nitric acid)和亚硝酸(nitrous acid)的区别
硝酸和亚硝酸是含有氮原子的无机酸。硝酸和亚硝酸之间的关键区别在于硝酸分子包含三个与中心氮原子结合的氧原子,而亚硝酸分子包含两个与中心氮原子结合的氧原子。
此外,硝酸和亚硝酸之间的一个容易识别的区别是,硝酸是无色、淡黄色或红色发烟液体,而亚硝酸是淡蓝色溶液。除此之外,硝酸是一种比亚硝酸强的酸。
下面的信息图表列出了硝酸和亚硝酸之间的差异。
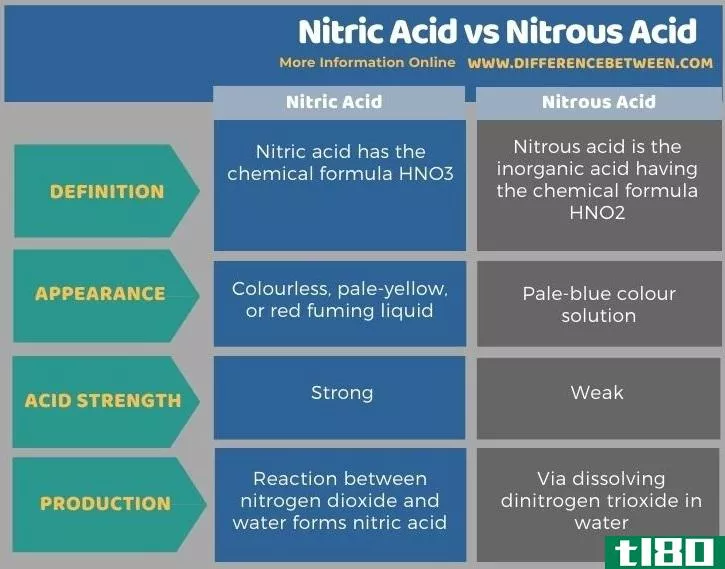
总结 - 硝酸硝酸(nitric acid) vs. 亚硝酸(nitrous acid)
硝酸和亚硝酸是含有氮原子的无机酸。硝酸和亚硝酸之间的关键区别在于硝酸分子包含三个与中心氮原子结合的氧原子,而亚硝酸分子包含两个与中心氮原子结合的氧原子。
引用
1亚硝酸。(未注明)。科学指导。检索日期:2020年10月13日,此处提供。