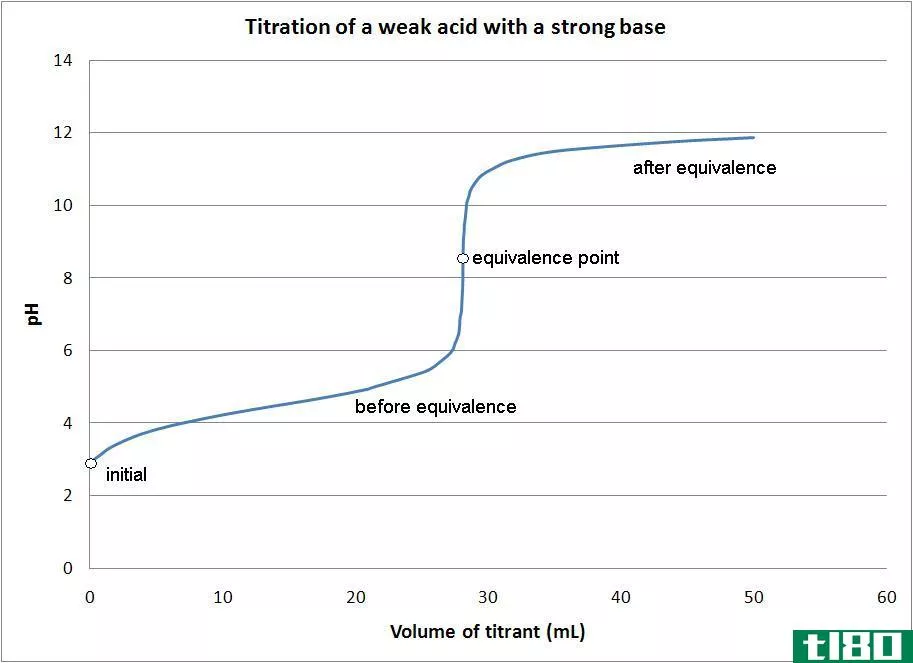
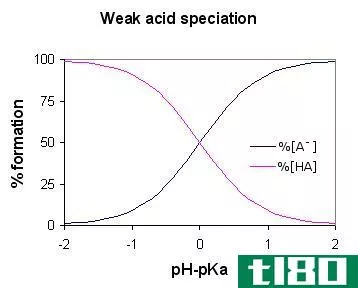
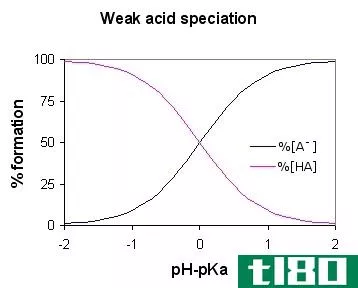
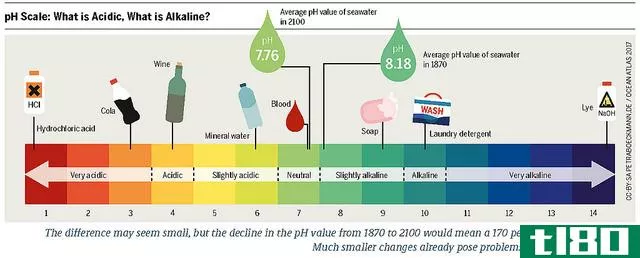
强酸(strong acid)和弱酸(weak acid)的区别
世界上的一切事物都与科学有某种联系,或包含着科学,它可以是任何东西,任何形式或状态,如固体、液体或气体。有肉眼看不见的化学反应。
不同的化学物质有各自的特点。有时两种化学物质混合得到第三种产品,但反应只能由专业人员进行,因为它们也可能导致严重的结果。
在做任何化学反应之前,有几件事是要牢记在心的,地球上的一切都有原子和分子。因此,在反应中最重要的是分子。
例如,水有两个氢分子和一个氧分子,这使它成为H2O。这是基本的,不能改变,这个公式不能像两个氧分子和一个氢分子那样改变。
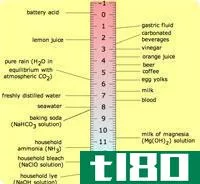
同样,也有不同的水溶液在使用前需要了解。例如酸、碱、中性物质等。在混合任何溶液之前,都需要检查溶液的PH值。例如,酸会造成严重伤害,碱的PH值较低,而中性的PH值正常。
强酸(strong acid) vs. 弱酸(weak acid)
强酸和弱酸的区别在于它们的PH值和电离能力。强酸和弱酸都是酸,但它们的PH值不同,还有其他特性。

| Parameters of Comparison | Strong Acid | Weak Acid |
|---|---|---|
| 导电性 | 良导体 | 不良导体 |
| 反应的 | 高反应性 | 反应较少 |
| PH值 | 0到3 | 5到7以下 |
| 可食用的 | 不可食用 | 食用(大部分) |
| 反应速率 | 高 | 低 |
强酸与弱酸对比表
什么是强酸(strong acid)?
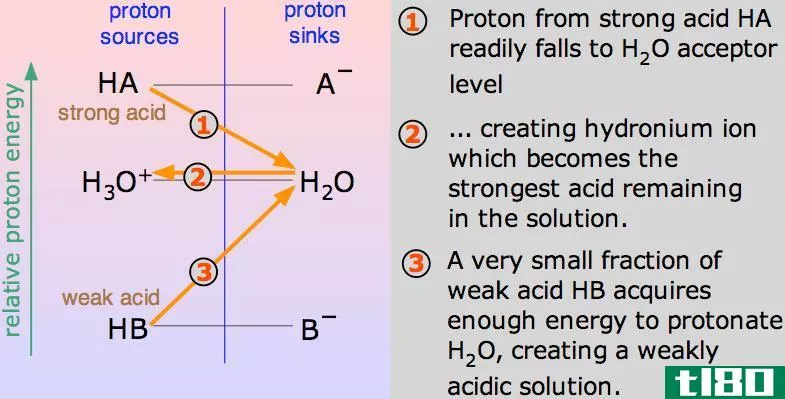
强酸是容易失去质子的酸。它们在水溶液中失去一个质子而电离。酸的强度由它电离的第一个质子决定。
为了比较酸的强度,他们捐赠质子的倾向是用混合的任何碱来检验的。这种强度是由pKA数决定的。强酸在水中完全分解。
氢质子是由酸释放的带电离子,如果氢离子的数目较多,则称酸为强酸。由于三个带电的强酸粒子被释放出来,它们也成为电的良导体。
少数强酸为硫酸、盐酸(HCI)、氢溴酸(HBr)、氢碘酸(HI)、高氯酸(HCLO4)、硝酸(HNO3)等。。这些酸更多地释放质子,并在碱(主要是水)中离解。
在强酸中反应速度较快。它们释放离子更快,使溶液变酸。强酸的PH值很低,可能在0或1左右。建议家庭不要使用强酸,应放在儿童接触不到的地方。
强酸容易腐蚀金属。一些强酸也用在日常生活中,例如汽车的电池,它用硫酸(它发电)硫酸是苛性的,盐酸的另一种形式是在水池中用来调节PH值。
即使是人体也含有强酸,即盐酸(HCI),它存在于胃中可能有助于消化,并且根据人的胃水平而存在。
当强酸在碱中释放质子时,反过来又从碱中提取电子。在物理性质上,酸是酸性的、腐蚀性的和有害的。强酸与任何碱混合都会产生盐和水。这个过程也被称为中和。中和产物的酸性比反应酸的酸性低。
什么是弱酸(weak acid)?
与强酸不同,弱酸在碱中不完全分解,因此它们在中和过程后部分溶解在碱中,形成中和产物。
它们获得电子和释放质子的能力较低,酸性强度较低,因此pKA较低。它们也是电的导体,但导电率极低。与强酸相比,它们的电流传递过程很慢。
从理论上讲,质子H+的浓度很低,因此它们的反应性较低。例如,草酸(C2H2O4)、乙酸(CH3COOH)、甲酸(HCOOH)、苯甲酸(C6H5COOH)、亚硝酸(HNO2)、氢氟酸(HF)等。。
弱酸反应需要时间,它们反应很慢。它们的PH值在5到7之间,比强酸低。他们甚至可以烧伤鼻孔时,气味和味道酸。
一些弱酸用于食品和饮料,如磷酸(用于软饮料、发酵粉,也可作为中和剂等)、柠檬酸(用于冰淇淋、水果饮料、乳制品等)、醋酸(用作防腐剂、蛋黄酱、烘焙制品等)。。
因此,很明显,弱酸是太弱,是正常人食用。它们没有腐蚀性,因此不会像在强酸的情况下伤害任何人。弱酸有时甚至被认为是有益于健康,以及当采取的限制。但是当超过限制或者某人对任何特定的酸(如乳酸)过敏时,会造成伤害。
Main Differences Between 强酸和弱酸
- 强酸反应更快,而弱酸与任何碱反应都需要时间。
- 强酸是电的良导体,相反,弱酸不太好作电的导体。
- 强酸通电更快,而弱酸是慢导体。
- 强酸不可食用,而弱酸可食用。
- 强酸的酸碱度值在0到3.之间,而弱酸的酸碱度值在5.到7.之间。
结论
强酸和弱酸都是不同类型的酸。质子的浓度不同,但所有酸的组成都是相同的。两者都是日常需要,目的可能不同。
参考文献
- https://www.sciencedirect.com/science/article/pii/0043135480902614
- https://www.sciencedirect.com/science/article/pii/0043135479902422
- 发表于 2021-07-10 00:46
- 阅读 ( 193 )
- 分类:科学
你可能感兴趣的文章
酸碱滴定法(acid-base titration)和氧化还原滴定(redox titration)的区别
...2CO3或Na2CO3。根据酸碱强度,酸碱滴定可分为以下几种。 强酸-强碱滴定 强酸弱碱滴定法 弱酸-强碱滴定 弱酸-弱碱滴定 在大多数酸碱滴定法中,指示剂用于确定反应终点。根据上述滴定类型使用不同的指示剂。 什么是氧化还...
- 发布于 2020-10-06 00:15
- 阅读 ( 660 )
弱酸(weak acid)和稀酸(dilute acid)的区别
...离子)的化合物。因此,酸的pH值低于7。根据酸的强度有强酸和弱酸两种类型。但根据酸的浓度,有浓酸和稀酸两种酸溶液。 目录 1. 概述和主要区别 2. 什么是弱酸 3. 什么是稀酸 4. 并列比较-弱酸与稀酸的表格形式 5. 摘要 什么...
- 发布于 2020-10-16 18:33
- 阅读 ( 567 )
氢氟酸(hydrofluoric acid)和盐酸(hydrochloric acid)的区别
... 氢氟酸和盐酸的关键区别在于氢氟酸是弱酸,而盐酸是强酸。此外,氢氟酸能够形成氢键,而盐酸不能形成氢键。 此外,氢氟酸和盐酸的另一个重要区别在于它们的分子结构。氢氟酸分子有氟离子,而盐酸分子有氯离子。此...
- 发布于 2020-10-18 08:39
- 阅读 ( 550 )
浓酸(concentrated acid)和强酸(strong acid)的区别
关键区别-浓酸与强酸 酸是一种化合物,它可以通过酸分子的离子化将氢离子(质子)释放到其所在的介质中。酸有两种主要类型,即强酸和弱酸。强酸是在水溶液中完全离解,释放H+离子的酸。强碱是在水溶液中完全离解形...
- 发布于 2020-10-19 14:49
- 阅读 ( 385 )
虚弱的(weak)和强酸(strong acid)的区别
弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。 酸的强度是它在水溶液中与水发生反应时电离或提供氢离子的能力。酸离子化得越多,它就越强,氢离子的生成越少,说明酸是弱酸。这就是强酸和弱酸...
- 发布于 2020-10-23 09:57
- 阅读 ( 349 )
酸的(acid)和酸的(acidic)的区别
...,酸的pH值小于7,而且有酸味。此外,还有三大类酸。即强酸、中强酸和弱酸。强酸完全电离,将所有可能的氢离子释放到水溶液中,而弱酸则部分电离。 此外,酸有两大类。也就是说,它们是Brønsted和Lewis酸。Brønsted酸是质子...
- 发布于 2020-11-05 21:23
- 阅读 ( 319 )
二元酸(binary acids)和多原子酸(polyatomic acids)的区别
...可能有一个或多个氢原子。 图01:氯化氢 二元酸可以是强酸、弱酸或中酸性。这种酸性强度取决于氢原子和非金属原子之间共价键的强度。因为所有的二元酸都含有氢原子,所以二元酸的名字以“hydro-”开头。 什么是多原子酸(...
- 发布于 2021-03-04 18:44
- 阅读 ( 254 )
酸的(acid)和基础(base)的区别
...的作用,而碱起质子受体的作用。 酸和碱可分为弱酸和强酸。在弱酸和弱碱的情况下,共轭结果很强,但弱酸或弱碱在水中不能很好地解离。然而,强酸和强碱在水中几乎完全解离,尽管它们的结合酸或结合碱很弱。 至于物理...
- 发布于 2021-06-22 10:49
- 阅读 ( 294 )
坚强的(strong)和弱酸(weak acid)的区别
...酸释放出的质子的数量实际上决定了酸的强度——无论是强酸还是弱酸。为了了解酸的强度,我们需要比较它们向类似的碱(主要是水)提供质子的倾向。强度由一个称为pKA的数字表示。 什么是强酸(a strong acid)? 如果一种...
- 发布于 2021-06-25 16:37
- 阅读 ( 417 )
硝酸盐(nitrate)和亚硝酸盐(nitrite)的区别
...分子几何结构。 与水反应 硝酸盐形成硝酸,硝酸是一种强酸。 亚硝酸盐形成亚硝酸,亚硝酸是一种弱酸。 氧化还原 硝酸盐可以被还原成亚硝酸盐。 Nitrites can be oxidized to form nitrates. 图片提供: “硝酸盐3D球”由Benjah-bmm27-自己...
- 发布于 2021-06-27 12:06
- 阅读 ( 438 )