原子和化合物的关键区别在于原子是所有物质的基本单位,而化合物是由两个或两个以上原子组成的化学物种。
单个元素在自然条件下很难稳定。它们在它们之间或与其他元素形成各种组合以存在。当这种情况发生时,单一元素的性质会发生变化,并产生新的混合物,如化合物。
目录
1. 概述和主要区别
2. 什么是原子
3. 什么是复合物
4. 并列比较-原子与化合物的表格形式
5. 摘要
什么是原子(atom)?
原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察。通常原子在埃范围内。此外,它们还含有一个原子核,它有质子和中子。除此之外,原子核中还有其他小的亚原子粒子。此外,还有电子在轨道上绕着原子核旋转。
然而,原子中的大部分空间是空的。带正电的原子核(质子带正电荷)和带负电的电子之间的吸引力维持着原子的形状。同类原子有相似的质子和电子。然而,同一类型的原子可能会因中子数的不同而有所不同,我们称之为同位素。
原子可以以各种方式与其他原子结合。因此,它们可以形成数千个分子。除诺贝尔气体外,所有元素都有一个双原子或多原子的排列方式变得稳定。根据它们的给电子或吸电子能力,它们可以形成共价键或离子键。有时,它们在原子间的吸引力很弱。
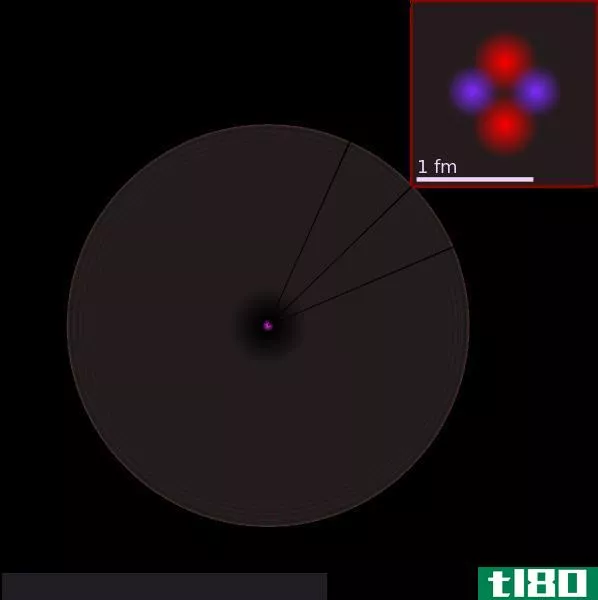
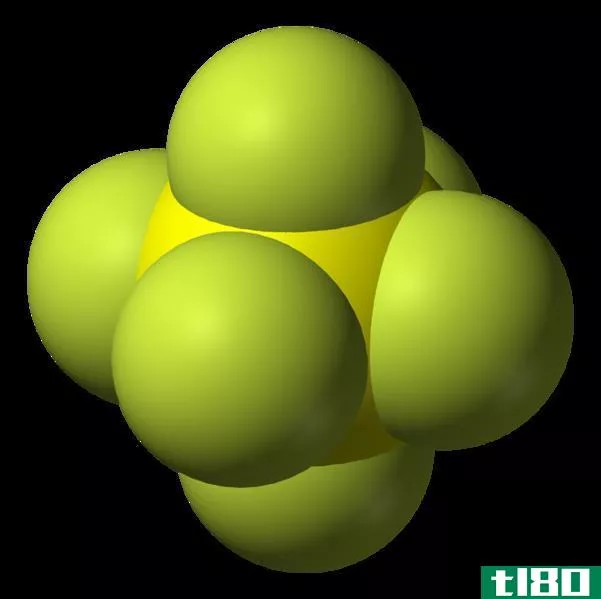
图01:假设原子的结构
此外,由不同科学家进行的一系列实验有助于确定原子的结构。根据道尔顿原子理论,
- 所有物质都是由原子构成的,我们不能进一步分解它们。
- 给定元素的所有原子都是相同的。
- 化合物是由两个或两个以上的原子结合而成的。
- 我们不能**或摧毁原子。化学反应是原子的重新排列。
然而,随着关于原子的更先进的发现,道尔顿理论有一些修改。
什么是复合(compound)?
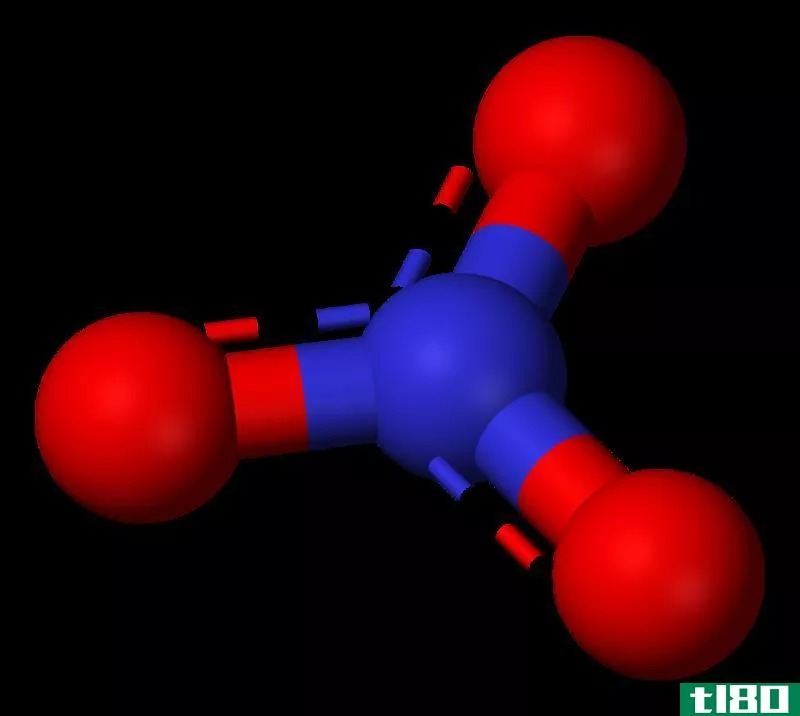
化合物是由两种或两种以上不同的化学元素组成的化学物质。我们可以把两种或两种以上相同化学元素的组合称为化合物。例如,像O2,H2,N2这样的双原子分子或者像P4这样的多原子分子不是化合物,它们是分子。NaCl、H2O、HNO3和C6H12O6是常见化合物的一些示例。因此,化合物是分子的一个子集。

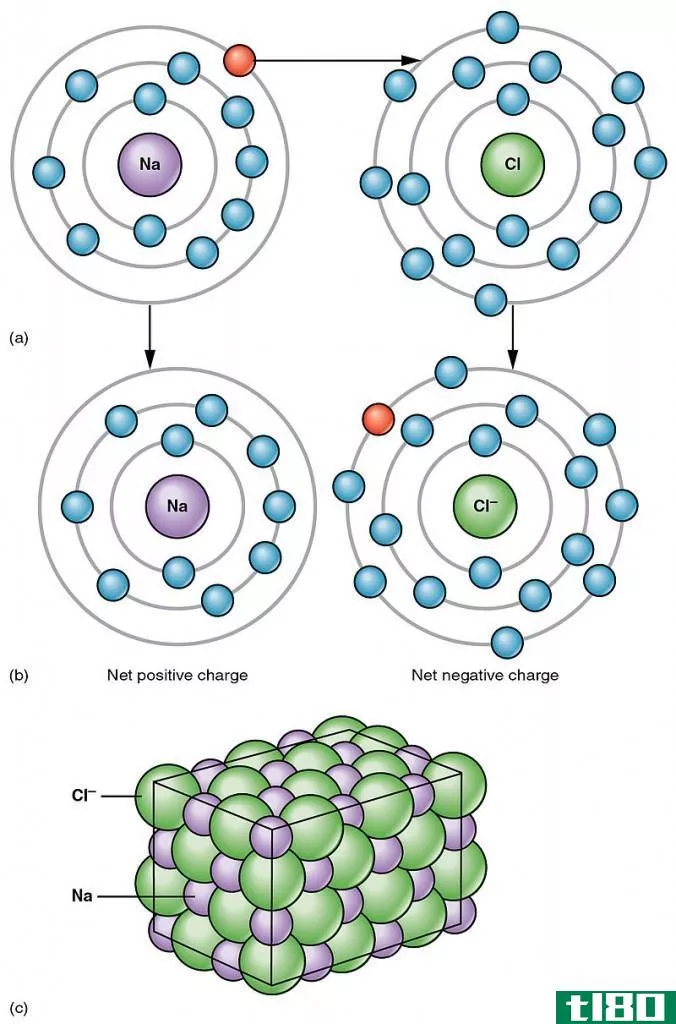
图02:水含有化合物H2O
此外,化合物中的元素通过共价键、离子键、金属键等连接在一起。这些化学物种的结构决定了化合物中原子的数量和它们的比例。在化合物中,元素以一定的比例存在。通过观察化合物的化学式,我们可以很容易地找到这些细节。此外,它们是稳定的,而且它们具有独特的形状、颜色、性质等。
原子(atom)和复合(compound)的区别
原子比化合物小得多。这是因为化合物是由两种或两种以上不同类型的原子组成的。因此,原子和化合物的关键区别在于原子是所有物质的基本单位,而化合物是由两个或两个以上原子组成的化学物种。
此外,化合物的化学和物理性质与所涉及的原子不同。除此之外,原子和化合物的另一个区别是,我们不能通过化学反应进一步分解一个原子,而不改变它的性质;在那里,我们只能把它们分解成亚原子粒子。然而,我们可以把化合物分解成分子或原子。
下图显示了原子和化合物的区别,作为一个并列的比较。

总结 - 原子(atom) vs. 复合(compound)
原子是所有物质中最小的单位。因此,它们很小。另一方面,化合物是原子的组合。原子和化合物的关键区别在于原子是所有物质的基本单位,而化合物是由两个或两个以上原子组成的化学物种。
引用
1“原子”,维基百科,维基媒体基金会,2018年12月6日。这里有2个。诺曼、理查德O.C.等人。“化合物”,《大英百科全书》,百科全书《大英百科全书》,2016年12月6日。可在此处查阅
2诺曼、理查德O.C.等人。“化合物”,《大英百科全书》,大英百科全书,2016年12月6日