极性与非极性
正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。这些原子趋向于相互反应以变得稳定。因此,每一个原子都可以实现稀有气体的电子组态。要使原子相互反应,就必须有吸引力。原子或分子中的电子运动使它们成为极性或非极性,这有助于它们的相互作用。
极地的
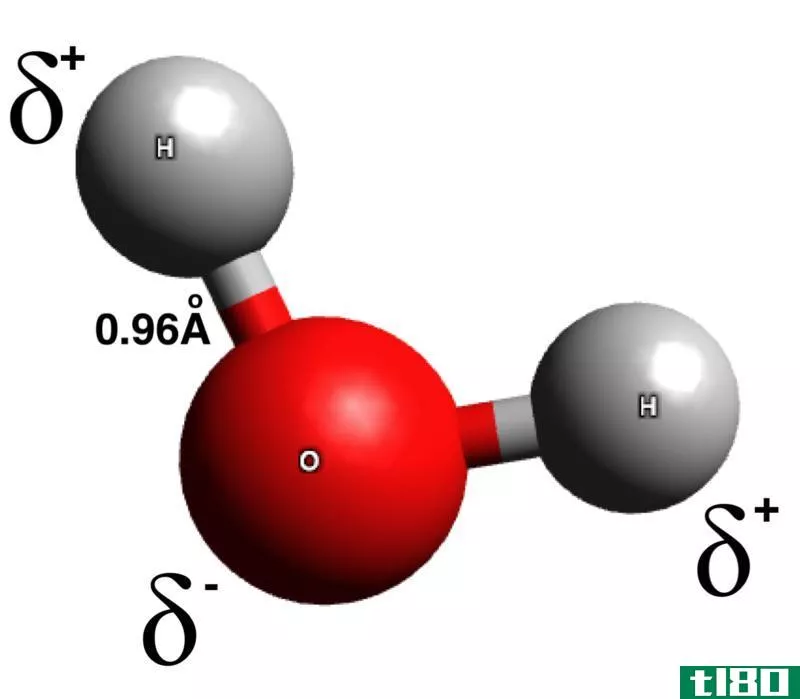
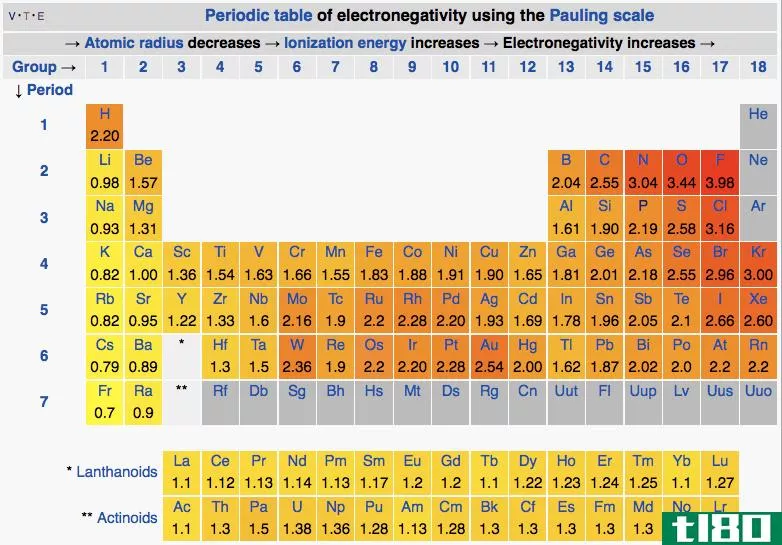
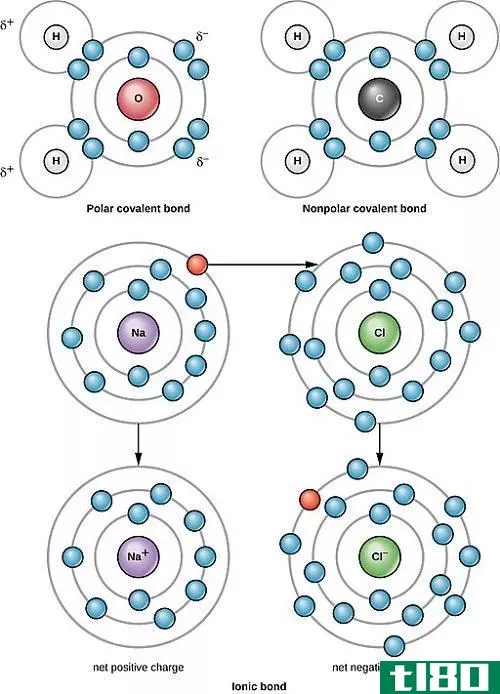
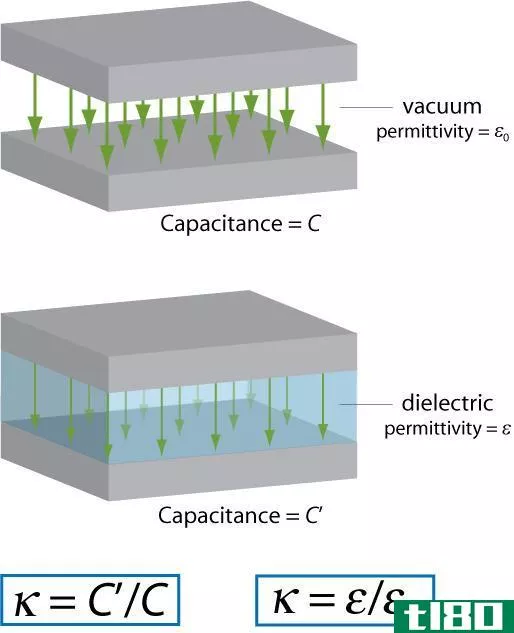
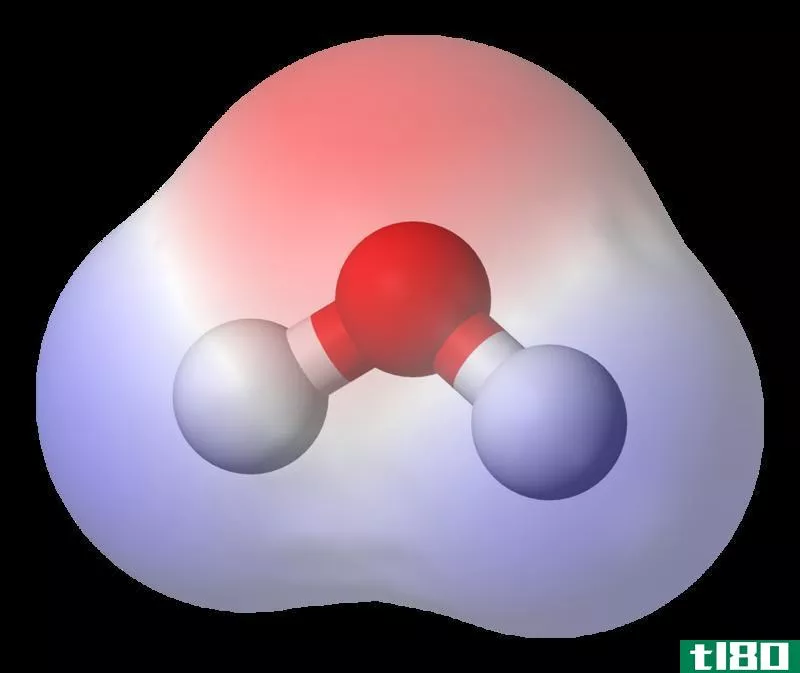
极性是由于电负性的不同而产生的。电负性是衡量原子在键中吸引电子的程度。通常用波林标度来表示电负性值。如果两个原子之间的电负性差非常大(超过1.7),那么键将是离子键。对于极性键,电负性差不应超过1.7。根据电负性差异的程度,极性可以改变。这种差异程度可能更高或更低。因此,键-电子对被一个原子拉大,而另一个原子参与形成键。这将导致两个原子之间的电子分布不均。由于电子的不均匀共享,一个原子带着轻微的负电荷,而另一个原子则带着轻微的正电荷。比如说,在这个例子中,我们得到了一个正电荷或负电荷。电负性高的原子带轻微的负电荷,电负性低的原子带轻微的正电荷。极性意味着电荷的分离。这些分子有偶极矩。偶极矩测量键的极性,通常用德比(它也有方向)来测量。
极性物质往往与其他极性物质相互作用。
非极性
当两个或两个具有相同电负性的原子在它们之间形成键时,这些原子以相似的方式拉动电子对。因此,它们倾向于共享电子,这种键被称为非极性共价键。例如,当同一个原子结合形成Cl2、H2或P4等分子时,每个原子通过非极性共价键与另一个原子结合。这些分子是非极性分子。
非极性物质喜欢与其他非极性物质相互作用。
| 极性和非极性的区别是什么?•极性分子有电偶极矩,而非极性分子没有偶极矩。•极性分子与非极性分子相比有电荷分离。•极性物质倾向于与其他极性物质相互作用;它们不喜欢与非极性物质相互作用。 |