惰性气体构型和电子构型之间的关键区别在于,惰性气体构型只有电子对,而电子构型可以有成对和非成对电子。
术语电子构型是指特定化学元素的原子中存在的电子序列或电子顺序。惰性气体电子组态一词表明所有的原子轨道都完全充满了电子。
目录
1. 概述和主要区别
2. 什么是惰性气体配置
3. 什么是电子构型
4. 并列比较-惰性气体组态与电子组态的表格形式
5. 摘要
什么是惰性气体配置(noble gas configuration)?
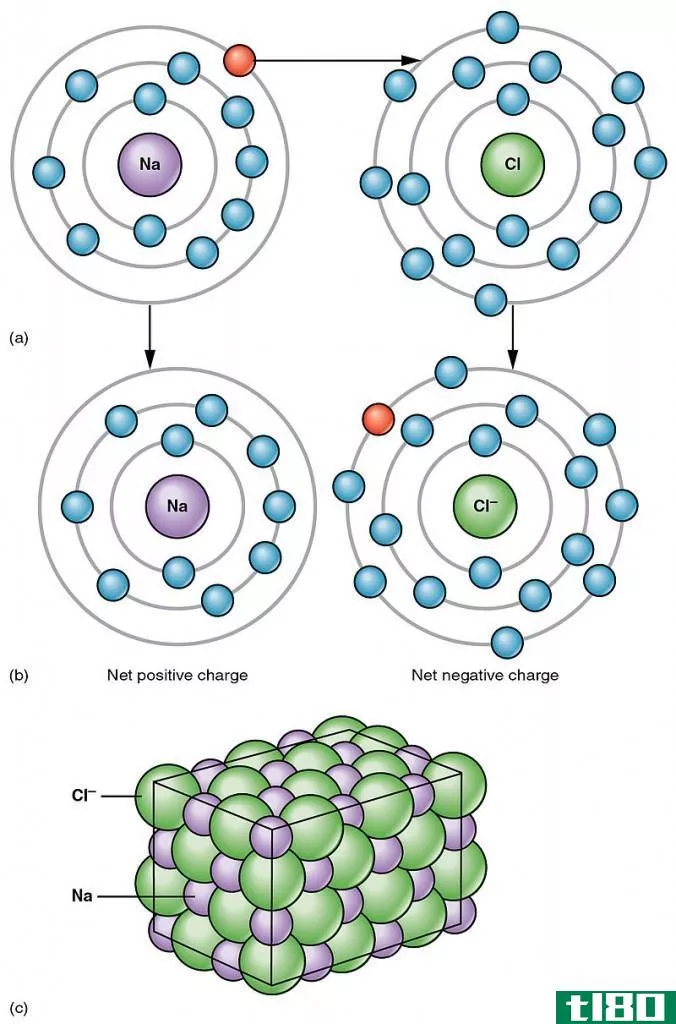
惰性气体构型是惰性气体原子的电子构型。惰性气体原子是周期表中第18组化学元素的原子。由于两个原因,第18组化学元素被称为惰性气体元素;第一,这些化学元素由于其完整的电子构型而大部分不反应;第二个原因是这些化学元素在自然界中以气态存在。

图01:不同的惰性气体
一个化学元素中有四种主要的原子轨道:s轨道、p轨道、d轨道和f轨道。s原子轨道最多包含两个电子,p轨道可以容纳六个电子,d轨道可以容纳十个电子,f轨道可以容纳十四个电子。在第18组化学元素中,我们可以观察到s2p6电子构型;在这里,s和p原子轨道完全充满了电子。因此,这些原子中没有未配对的电子。
什么是电子构型(electron configuration)?
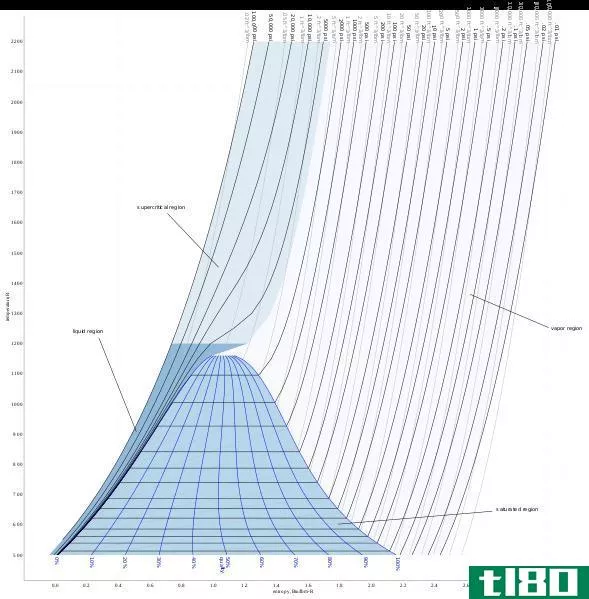
电子构型是一个原子的电子在其原子轨道上的分布。这个术语描述原子中的每个电子在一个轨道上独立地运动,在一个由所有其他轨道产生的平均场中。
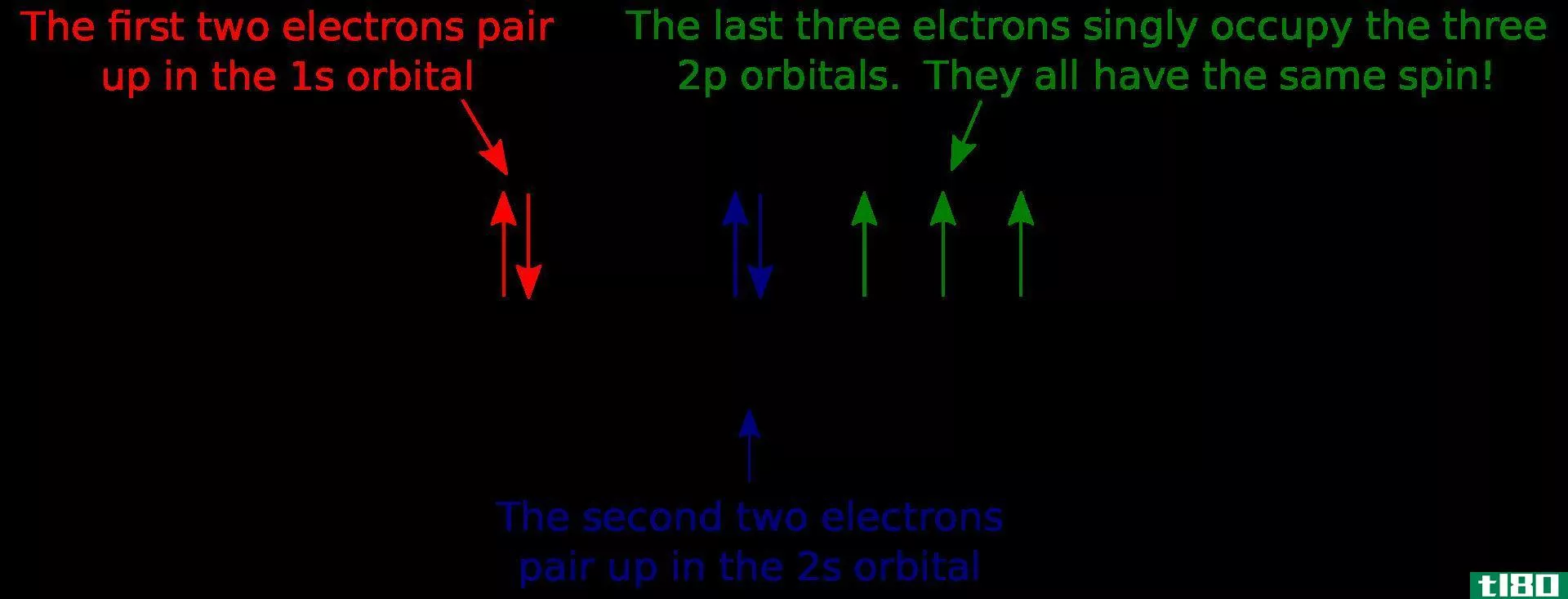
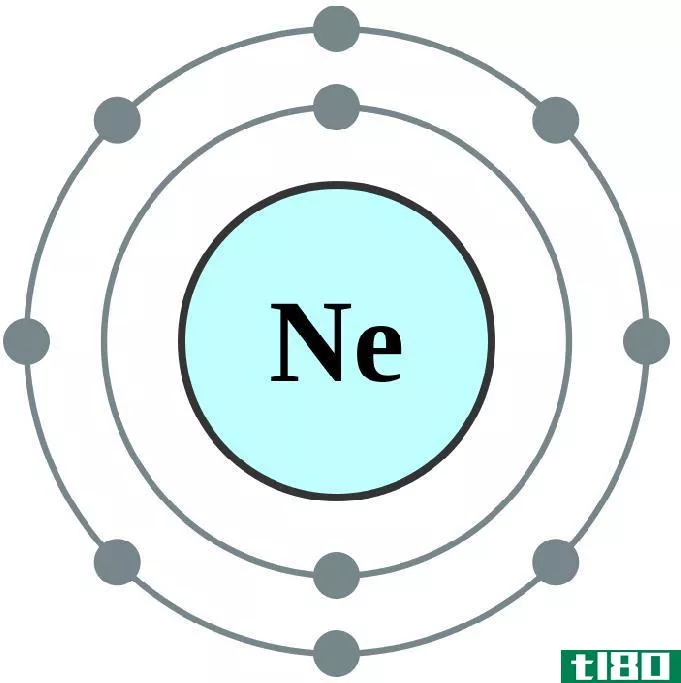
一个原子的电子构型可以表示为该原子中以分布形式存在于该原子的整个原子轨道上的电子序列。一些化学元素如惰性气体原子已经完成了原子轨道,并且没有未配对的电子;然而,我们知道的大多数化学元素的电子构型中都有未配对的电子。例如,惰性气体原子氖原子的电子构型为1s22s22p6。
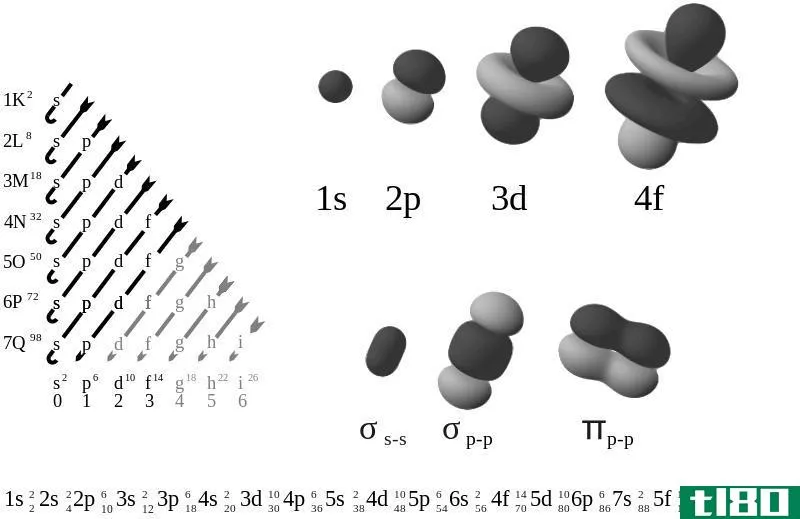
通过观察原子的电子构型,我们可以描述原子的反应性。一个完全充满的原子轨道表明它是一个不反应的性质,因为它不需要获得更多的电子来稳定自己。相反,在一个原子中,有未配对的电子往往倾向于高度反应,以稳定其电子组态。
惰性气体配置(noble gas configuration)和电子构型(electron configuration)的区别
惰性气体构型是一个惰性气体原子的电子构型;这意味着原子已经完全充满了原子轨道。惰性气体构型和电子构型之间的关键区别在于,惰性气体构型只有电子对,而电子构型可以有成对和非成对电子。也就是说,惰性气体构型有完全填充的原子轨道,而电子构型有完全填充或半填充的轨道。
下面的信息图表列出了惰性气体配置和电子配置之间的更多差异。
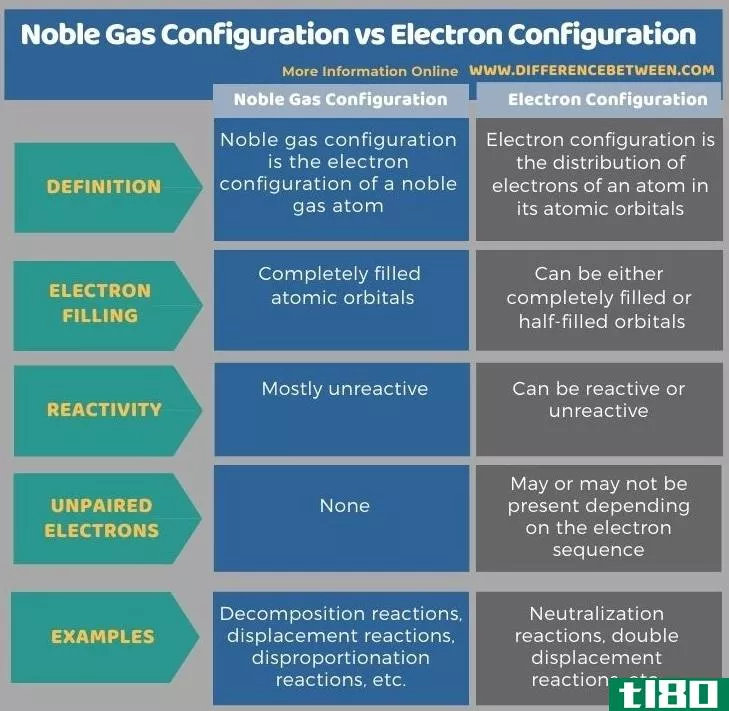
总结 - 惰性气体配置(noble gas configuration) vs. 电子构型(electron configuration)
电子构型是存在于原子中的电子序列。惰性气体构型和电子构型之间的关键区别在于,惰性气体构型只有电子对,而电子构型可以有成对和非成对电子。
引用
1“惰性气体”,《大英百科全书》,大英百科全书公司,2020年10月23日,可在此处查阅。