电负性(electronegativity)和电子亲和力(electron affinity)的区别
主差电负性(main difference electronegativity) vs. 电子亲和力(electron affinity)
电子是原子的亚原子粒子。电子无处不在,因为每种物质都是由原子组成的。然而,在某些化学反应中,电子是非常重要的,因为在这些反应中,电子的交换是反应物和产物之间的唯一区别。电负性和电子亲和力是解释元素由于电子的存在而产生的行为的两个术语。电负性和电子亲和性的主要区别在于,电负性是原子从外部吸引电子的能力,而电子亲和性是原子获得电子时释放的能量。
覆盖的关键领域
1.什么是电负性-定义、测量单位、与原子序数、键的关系2.什么是电子亲和性-定义、测量单位、与原子序数的关系3.电负性和电子亲和性之间的区别-主要区别的比较
关键词:原子,电子,电子亲和性,电负性,吸热反应,放热反应,鲍林标度

什么是电负性(electronegativity)?
电负性是原子从外部吸引电子的能力。这是原子的定性性质,为了比较每个元素中原子的电负性,使用了相对电负性值所在的标度。这个尺度被称为“鲍林尺度”,根据这个尺度,原子所能具有的最高电负性值是4.0。考虑到其他原子吸引电子的能力,给出了它们的电负性值。
电负性取决于原子序数和元素中原子的大小。当考虑周期表时,氟(F)的电负性为4.0,因为它是一个小原子,价电子位于原子核附近。因此,它可以很容易地从外部吸引电子。另外,氟的原子序数为9;它有一个空位轨道来容纳一个或多个电子,以便遵守八位元规则。因此,氟很容易从外面吸引电子。
电负性使两个原子之间的键极性。如果一个原子比另一个原子负性强,则电负性越高的原子就可以吸引键上的电子。这导致另一个原子由于周围缺少电子而产生部分正电荷。因此,电负性是将化学键分为极共价键、非极共价键和离子键的关键。离子键发生在两个原子之间,它们之间的电负性差别很大,而共价键发生在原子之间,原子之间的电负性略有不同。
元素的电负性是周期性变化的。元素周期表根据元素的电负性值对元素进行了更好的排列。

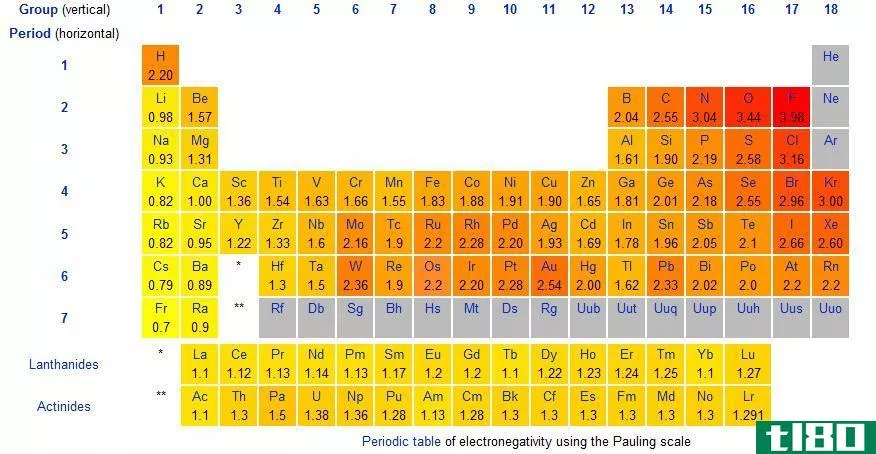
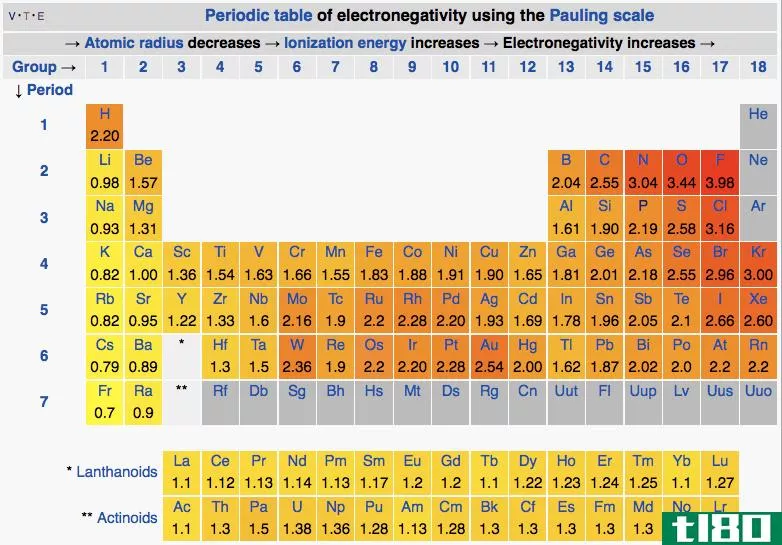
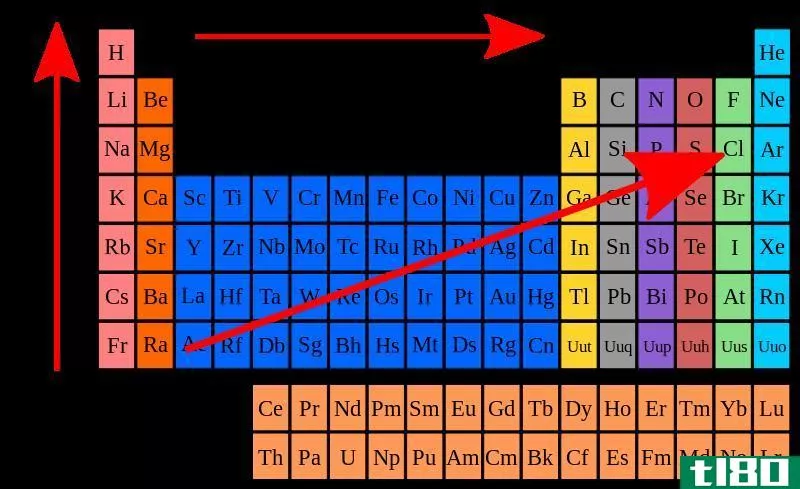
Figure 1: Periodic Table of Elements along with Electronegativity of Elements
当考虑周期表中的一个周期时,每个元素的原子大小从周期的左边到右边递减。这是因为价壳层中的电子数和原子核中的质子数都增加了,因此电子与原子核之间的吸引力逐渐增大。因此,电负性也会随着时间的推移而增加,因为来自原子核的吸引力会增加。这样原子就可以很容易地从外面吸引电子。

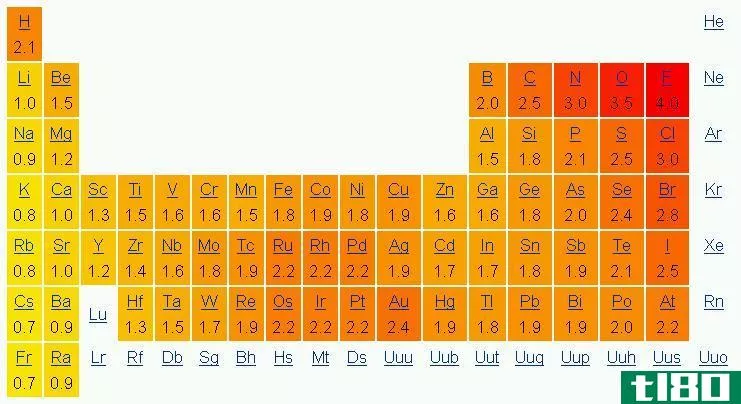
Figure 02: Electronegativity (XP) from top to bottom of each group
第17族每个周期的原子数最小,所以它的电负性最高。但是电负性随着轨道数的增加而减小,因为原子尺寸随着轨道数的增加而增大。
什么是电子亲和力(electron affinity)?
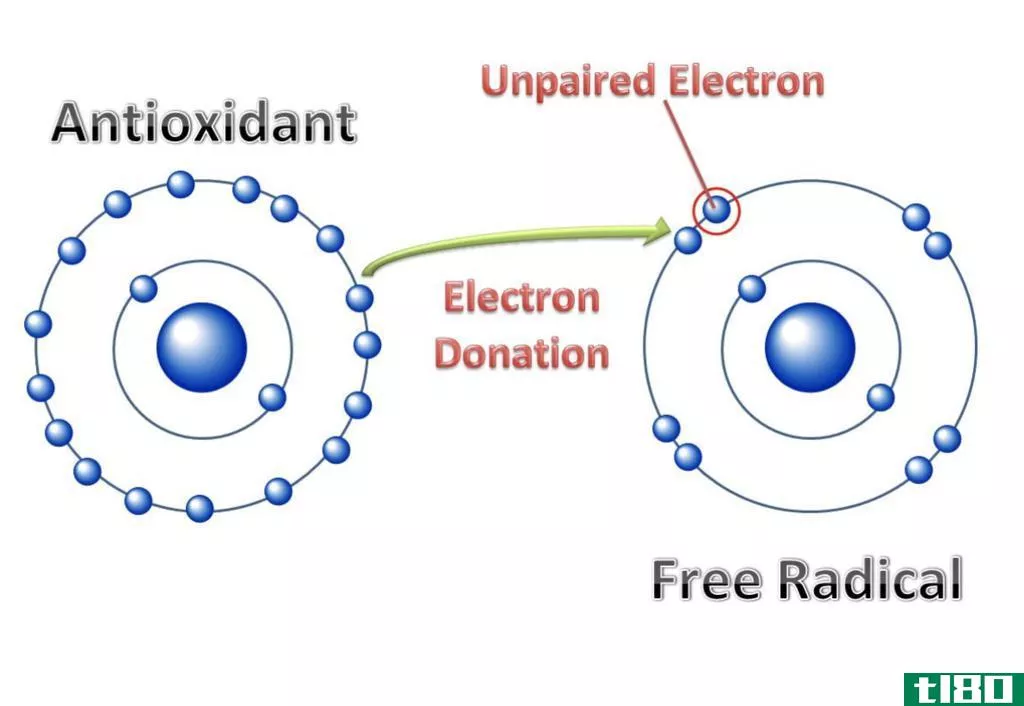
电子亲和力是中性原子或分子(在气相中)从外部获得电子时释放的能量。这个电子的加成导致一种带负电荷的化学物质的形成。这可以用如下符号表示。
X+e–→ X–+能量
把电子加到中性原子或分子上释放能量。这叫做放热反应。这个反应产生负离子。但是如果另一个电子要加入到这个负离子中,为了继续这个反应,应该给它能量。这是因为入射电子被其他电子排斥。这种现象称为吸热反应。
因此,同一物种的第一电子亲和性为负值,第二电子亲和性为正值。
第一电子亲和性:X(g)+e–→ X–(克)
第二电子亲和性:X–(g)+e–→ X-2(克)
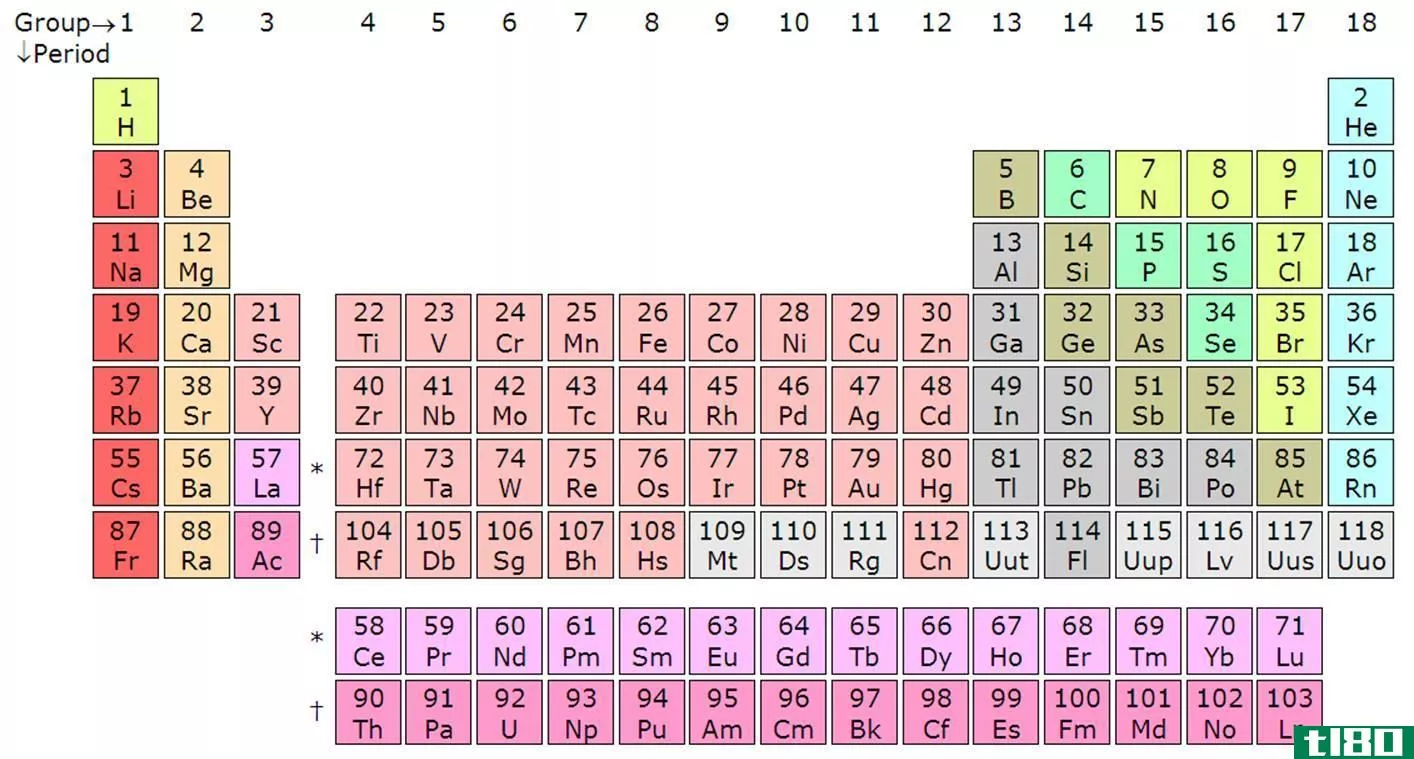
与电负性一样,电子亲和性在周期表中也表现出周期性变化。这是因为入射电子被加到原子的最外层轨道上。元素周期表的元素是按照原子序数的升序排列的。当原子序数增加时,它们最外层轨道上的电子数增加。

Figure 3: The General Pattern of Increasing the Electron Affinity along a Period
一般来说,电子亲和力应该沿着从左到右的周期增加,因为电子的数目沿着一个周期增加;因此,很难添加新的电子。当实验分析时,电子亲和势值显示出之字形图案而不是显示出逐渐增加的图案。

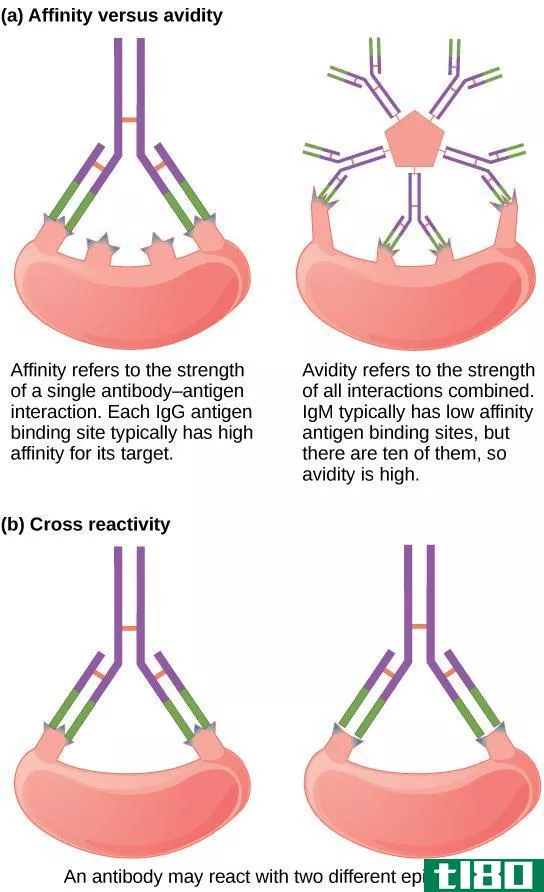
Figure 4: Variati*** of Electron Affinity of Elements
上图显示,从锂(Li)开始的周期显示出变化的模式,而不是电子亲和力的逐渐增加。在元素周期表中,铍(Be)排在锂(Li)之后,但铍的电子亲和力低于锂。这是因为进入的电子被带到锂的s轨道,那里已经有一个电子了。这个电子可以排斥进入的电子,从而产生高电子亲和力。但是在铍中,进入的电子被填充到一个自由p轨道,在那里不存在排斥。因此,电子亲和力的值稍小。
电负性(electronegativity)和电子亲和力(electron affinity)的区别
定义
电负性:电负性是原子从外部吸引电子的能力。
电子亲和性:电子亲和性是中性原子或分子(气相中)从外部获得电子时释放的能量。
自然
电负性:电负性是一种定性性质,用刻度来比较性质。
电子亲和力:电子亲和力是一种定量测量。
计量单位
电负性:电负性是用鲍林单位来测量的。
电子亲和力:电子亲和力由eV或kj/mol来测量。
应用
电负性:电负性适用于单个原子。
电子亲和性:电子亲和性可以应用于原子或分子。
结论
电负性和电子亲和性的主要区别在于,电负性是原子从外部吸引电子的能力,而电子亲和性是原子获得电子时释放的能量。
引用
1.“电子亲和性”,化学剧本。Libretexts,2016年12月11日,网络。这里有。2017年6月30日。 2.“电负性”,化学剧本。Libretexts,2016年11月13日。网络。这里有。2017年6月30日。 2.“电负性”,化学剧本。Libretexts,2016年11月13日。网络。
- 发表于 2021-06-28 19:57
- 阅读 ( 1176 )
- 分类:科学
你可能感兴趣的文章
电正性(electropositive)和电负性(electronegative)的区别
...因此,我们可以把它分为正负两种元素。 什么是电负性(electronegative)? 电负性是指化学元素获得电子的能力。从外部获得电子形成阴离子;阴离子是带负电的化学物质。电负性与电正性相反。这个现象的符号是χ。这个术语可能...
- 发布于 2020-10-15 13:07
- 阅读 ( 1161 )
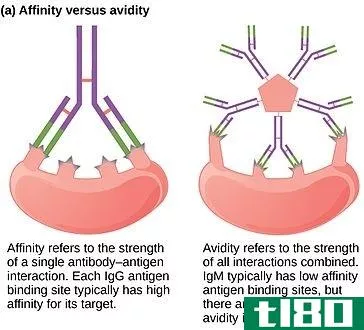
密切关系(affinity)和贪婪(avidity)的区别
关键区别–亲和力与热情 抗体-抗原相互作用是细胞内对抗感染的一种重要的相互作用。抗原是进入宿主细胞的外来粒子。它们主要由多糖或糖蛋白组成,形状独特。抗原和抗体之间的相互作用是通过氢键、范德华键等非共价...
- 发布于 2020-10-16 13:03
- 阅读 ( 219 )
酸度(acidity)和碱度(basicity)的区别
...氢氧化物离子的化学结构 影响化合物碱度的因素如下。 Electronegativity Atomic radius Formal charges 原子的电负性是指它对电子的亲和力。与低电负性原子相比,具有高电负性的原子可以吸引电子。电负性越高,碱度越低。为了释放氢...
- 发布于 2020-10-19 11:23
- 阅读 ( 386 )
密切关系(affinity)和离子交换色谱法(ion exchange chromatography)的区别
...以分离非靶生物分子,但目标分子必须对固定相有很高的亲和力才能成功分离。 什么是离子交换色谱法(ion exchange chromatography)? 离子色谱法是一种可以分析离子物质的液相色谱法。通常,我们用它来分析无机阴离子和阳离子(...
- 发布于 2020-10-22 02:59
- 阅读 ( 511 )
电负性(electronegativity)和极性(polarity)的区别
...列比较-电负性与极性的表格形式 5. 摘要 什么是电负性(electronegativity)? 电负性是一个原子吸引键中的电子朝向它的倾向。基本上,这显示了原子与电子的“相似性”。我们可以用鲍林标度来表示元素的电负性。 在周期表中,电...
- 发布于 2020-10-22 10:07
- 阅读 ( 896 )
电负性(electronegativity)和电离能(ionization energy)的区别
...比较-电负性与电离能的表格形式 5. 摘要 什么是电负性(electronegativity)? 电负性是一个原子吸引键中的电子朝向它的倾向。换句话说,这表明了原子对电子的吸引力。我们通常用鲍林标度来表示元素的电负性。 在周期表中,电负...
- 发布于 2020-11-04 14:49
- 阅读 ( 943 )
电子亲和力(electron affinity)和电子增益焓(electron gain enthalpy)的区别
电子亲和力和电子增益焓的关键区别在于,电子亲和力是指孤立原子获得电子的趋势,而电子增益焓是指孤立中性原子获得一个额外电子时释放的能量。 电子亲和力和电子增益焓是两个相关的术语,因为电子增益焓是关于电...
- 发布于 2021-03-04 15:37
- 阅读 ( 649 )
正电性(electropositive)和电负性自由基(electronegative radicals)的区别
...子(Na+)等。 图01:自由基的形成 什么是电负性自由基(electronegative radicals)? 电负性自由基是能够获得电子并携带负电荷的原子、离子或分子。电负性自由基是由于化学物种的高电负性而形成的,这意味着特定的化学物种有获...
- 发布于 2021-03-04 19:21
- 阅读 ( 995 )
亲和照片与photoshop:你应该选择哪一种?
...士无法想象没有Photoshop,但也许他们应该考虑其他选择。亲和力照片真的可以取代Photoshop吗?让我们试着回答这个问题。 ...
- 发布于 2021-03-26 17:48
- 阅读 ( 251 )
时期(periods)和组(groups)的区别
...变得相对难以去除电子。周期表中的核电荷增加。此外,电负性随着时间的推移从左向右移动而增加。随着电子的增加,电子亲和性也随之增加,从而增加了与原子核的强吸引力。 什么是组(groups)? 当您沿着列从上到下倒数...
- 发布于 2021-06-25 20:23
- 阅读 ( 518 )