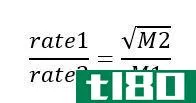亨利定律(henry’s law)和拉乌尔定律(raoult’s law)的区别
亨利定律的主要区别(main difference henry’s law) vs. 拉乌尔定律(raoult’s law)
亨利定律和拉乌尔特定律都是热力学中发现的两个定律,描述了一个解与其蒸汽之间的关系,它们之间是相互平衡的。亨利定律可以用来解释气体在液体溶剂(如水)中的溶解。拉乌尔特定律表明溶剂在一个与蒸汽压力平衡的溶液中的行为。然而,在实际解决方案中应用这些法律时,存在一定的局限性。亨利定律和拉乌尔特定律的主要区别在于亨利定律描述了溶液中溶质的行为,而拉乌尔特定律描述了溶液中溶剂的行为。
覆盖的关键领域
1.什么是亨利定律-举例说明定律,局限性2.什么是拉乌尔定律-举例说明定律,局限性3.亨利定律和拉乌尔定律的区别是什么-主要区别的比较
Key Terms: Henry’s Law, Raoult’s Law, Solute, Solution, Solvent
什么是亨利定律(henry’s law)?
亨利定律是一种气体定律,解释了气体在液体介质中的溶解。这条定律指出,溶解在液体中的气体的量与与液体平衡的气体的分压成正比。这可以用一个公式给出,如下所示。
[a(aq)]=kh.pa(g)
式中,[A(aq)]是溶解在溶液中的气体A的浓度,
kH是亨利定律常数
PA(g)是A(g)的分压
亨利定律常数是一个比例常数,它取决于溶剂、溶质和温度的类型。因此,对于一种特定的气体,亨利定律常数在不同的温度下可能不同。因此,在计算气体在水中的溶解度时,应得到该特定温度下亨利定律常数的值。
| 煤气 | 25℃时的亨利定律常数(mol/L atm) |
| 氧气 | 1.3 x 10-3英寸 |
| 氮气 | 6.1 x 10-4英寸 |
| 氢气 | 7.8 x 10-4英寸 |
| 二氧化碳 | 3.4 x 10-2英寸 |
表01:大气中不同气体在25℃时的亨利定律常数
此外,当对某一特定气体应用亨利定律时,应考虑该温度下水的蒸汽压来获得分压。让我们考虑下面的例子。
例子
问题:考虑一个处于正常大气条件下的湖泊。考虑到大气中水的蒸汽压为0.0313atm,在25℃温度和1atm大气压下测定O2(g)的溶解度。正常空气由21%的O2(g)组成。

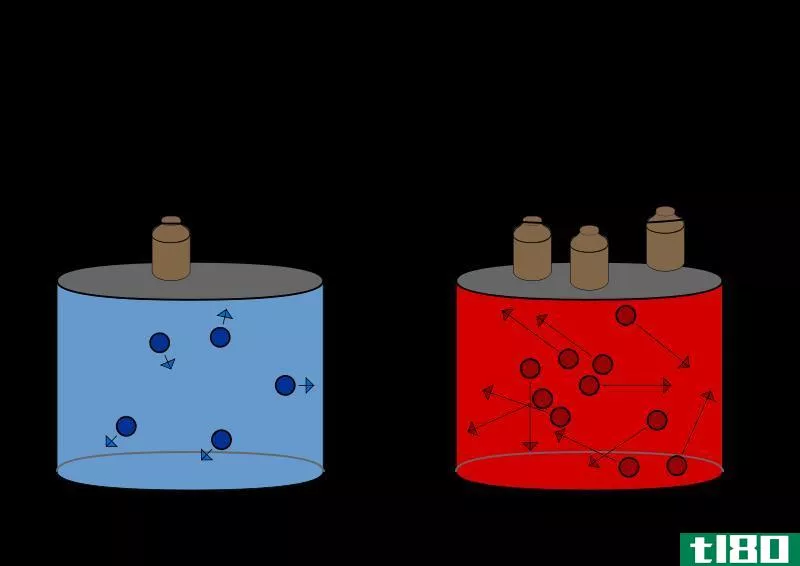
Figure 1: A water body is composed of water with gasses dissolved in different amounts according to the temperature of the water and at atmospheric pressure.
Answer:The partial 氧气在大气中的压力=(1-0.0313)atm x(21/100)=0.20 atmHenry定律常数,25℃时氧气=1.3 x 10-3mol/L atm
应用亨利定律;
[O2(aq)]=kH.PO2(g)=1.3 x 10-3 mol/L atm x 0.2 atm=2.6 x 10-4 mol/L
根据上述计算,在常温常压条件下,水体中的溶解氧含量很低。
局限性
只有当所考虑的分子处于平衡状态时,才能使用亨利定律。此外,这项法律不适用于高压条件。此外,如果溶解气体与溶剂发生化学反应,则该定律不能用于该体系。
什么是拉乌尔定律(raoult’s law)?
拉乌尔定律是一个热力学定律,它解释了溶液的蒸汽压和溶液中溶质的分压之间的关系。这个定律表明,溶液上方溶剂的蒸气压等于纯溶剂的蒸气压(在这个温度下)乘以溶剂的摩尔分数。这可以由下面的公式得出。
psolute=x绝对x绝对
式中,PA是混合物中A组分的分压,
xA是组分A的摩尔分数,
PoA是同一温度下纯组分的蒸气压。
例如,让我们考虑a和B的混合物。在这里,
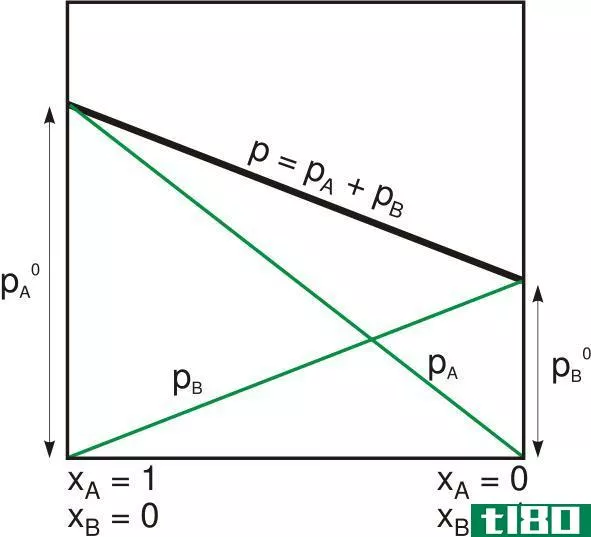
A的摩尔分数=nA/(nA+nB)A的分压={nA/(nA+nB)}p等于该体系的总蒸气压=PA+PB
然而,拉乌尔定律只适用于理想解。理想溶液是由溶质分子间相互作用等于溶剂分子间相互作用的溶质组成的。由于不存在可被视为理想气体的实际溶液,我们可以将此定律应用于溶质分子量较少的非常稀的溶液。

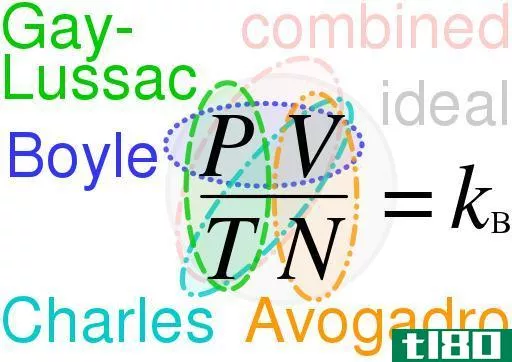
Figure 2: The application of Raoult’s law for a gaseous mixture composed of X and Y gases.
局限性
在计算溶质摩尔分数时,应考虑溶液中存在的粒子摩尔数,而不是添加的化合物的摩尔数。例如,当离子化合物溶解在水中时,在溶液中分离的每个离子应被视为一个粒子(例如:NaCl给出Na+和Cl-离子)。因此,所存在的颗粒量是添加NaCl量的两倍。)
亨利定律(henry’s law)和拉乌尔定律(raoult’s law)的区别
定义
亨利定律:亨利定律是解释气体在液体介质中溶解的热力学定律。
拉乌尔特定律:拉乌尔特定律是一个热力学定律,它解释了溶液的蒸汽压力和溶液中溶质的分压之间的关系。
概念
亨利定律:亨利定律指出,溶解在液体中的气体的量与与与液体平衡的气体的分压成正比。
拉乌尔定律:拉乌尔定律指出,溶液上方溶剂的蒸气压等于纯溶剂的蒸气压(在该温度下)乘以溶剂的摩尔分数。
比例常数
亨利定律:亨利定律中的比例常数称为亨利定律常数。
拉乌尔定律:拉乌尔定律不使用比例常数。
结论
亨利定律和拉乌尔定律表明了溶液与其蒸汽压接触时的化学行为。亨利定律和拉乌尔定律的区别在于,亨利定律解释了溶液中溶质的行为,而拉乌尔定律解释了溶液中溶剂的行为。
引用
1.“拉乌尔定律”,化学剧本,剧本,2017年3月3日,可在此查阅。查阅日期:2017年8月16日。无边无际。”亨利定律-无限开放教科书。“无限,2016年9月21日,可在这里获得。查阅日期:2017年8月16日。 2.无限。”《亨利定律——无限开放教科书》,《无限》,2016年9月21日,
- 发表于 2021-06-29 11:05
- 阅读 ( 908 )
- 分类:科学
你可能感兴趣的文章
格雷厄姆渗出定律(graham’s law of effusion)和扩散(diffusion)的区别
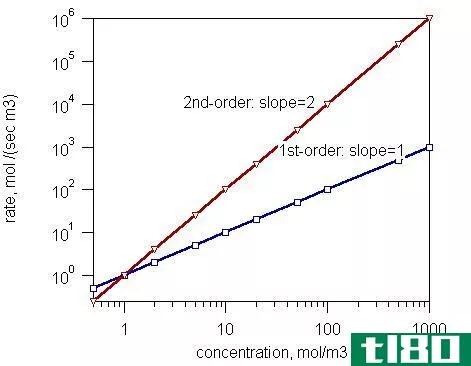
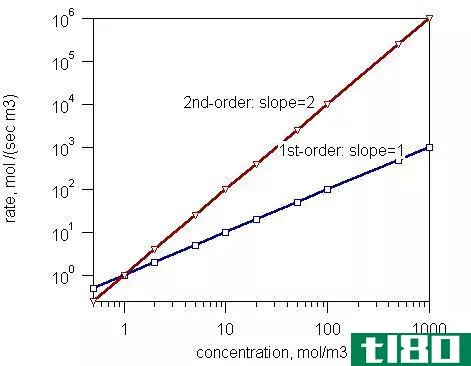
格雷厄姆渗出定律和扩散定律之间的关键区别在于,格雷厄姆的渗出定律适用于通过比气体颗粒小的开口的气体,而格雷厄姆扩散定律适用于在容器中分散的气体分子。 格雷厄姆定律指出,气体的扩散或渗出速率与其摩尔质...
- 发布于 2020-09-17 12:05
- 阅读 ( 635 )
利率法(rate law)和群众行动定律(law of mass action)的区别
关键区别-速率定律与质量作用定律 速率定律和质量作用定律的关键区别在于速率定律表示化学反应速率和反应物浓度之间的关系,而质量作用定律则表示化学反应的速率与反应物质的质量成正比。 速率定律是化学中用来解...
- 发布于 2020-10-05 12:19
- 阅读 ( 559 )
欧姆定律(ohm’s law)和基尔霍夫定律(kirchhoff’s law)的区别
主要区别——欧姆定律与基尔霍夫定律 在理解电学时,理解原始参数、电压和电流之间的关系是非常重要的。描述这种关系的基本原理是欧姆定律。另一方面,基尔霍夫定律是一种单独描述这些参数性质的理论。因此,欧姆...
- 发布于 2020-10-13 13:02
- 阅读 ( 547 )
微分速率定律(differential rate law)和综合费率法(integrated rate law)的区别
...微分速率律和综合速率律是速率律的两种形式。微分速率定律和积分速率定律的关键区别在于,微分速率定律给出了一个化学反应速率,它是一个特定时间段内一个或多个反应物浓度变化的函数,而积分速率定律给出的是化学反...
- 发布于 2020-10-16 09:23
- 阅读 ( 1220 )
拉乌尔定律(raoult law)和道尔顿定律(dalton law)的区别
拉乌尔定律和道尔顿定律的主要区别在于,拉乌尔定律处理固体或液体的蒸气压,而道尔顿定律处理的是非反应气体的分压。 劳尔定律和道尔顿定律是化学中解释气态分压的重要定律。拉乌尔定律描述了改变溶质浓度时溶液...
- 发布于 2020-10-16 16:00
- 阅读 ( 933 )
混合气体定律(combined gas law)和理想气体定律(ideal gas law)的区别
关键区别-组合气体定律与理想气体定律 在研究不同气体时,气体的体积、压力、温度和气体存在量之间的关系非常重要。这些关系由理想气体定律和组合气体定律给出。在解释这些定律时,通常使用“理想气体”一词。理想...
- 发布于 2020-10-19 04:51
- 阅读 ( 615 )
理想气体定律(ideal gas law)和真实气体定律(real gas law)的区别
理想气体定律和真实气体定律的关键区别在于,理想气体定律描述的是理论气体的行为,而真实气体定律描述的是宇宙中实际存在的气体的行为。 理想气体是一种理论气体,其随机运动的气体粒子之间没有其他相互作用,而...
- 发布于 2020-10-20 21:30
- 阅读 ( 857 )
孟德尔第一次(mendel’s first)和第二定律(second law)的区别
孟德尔第一定律和第二定律的关键区别在于,孟德尔第一定律描述了在配子发生过程中,某一特定基因座的等位基因分离为单独的配子体,而孟德尔第二定律描述的是基因等位基因独立地传递到子细胞中,而不受彼此的影响...
- 发布于 2020-10-24 06:25
- 阅读 ( 886 )
物质守恒定律(law of conservation of matter)和能量(energy)的区别
...量,反之亦然。这就是质量能量守恒的实际方式。这是由亨利·彭加勒和阿尔伯特·爱因斯坦首次提出的概念,被称为“狭义相对论”。质量和能量之间的关系如下所示: E=mc2 其中E是能量,m是质量,c是光速。然而,在经典力学...
- 发布于 2020-10-24 22:53
- 阅读 ( 695 )
牛顿第一定律(newton’s first law)和惯性(inertia)的区别
牛顿第一定律和惯性之间的关键区别在于,牛顿第一定律描述了物体的运动和作用在物体上的力之间的关系,而惯性一词是指物体对其速度变化的阻力。 一般来说,牛顿第一运动定律也被称为惯性定律。这是因为牛顿第一定...
- 发布于 2021-03-04 15:53
- 阅读 ( 723 )