主要区别
氯化物和氯酸盐的主要区别在于氯化物是单原子离子,如Cl-,而氯酸盐是多原子离子,如Cl-。
氯化物(chloride) vs. 氯酸盐(chlorate)
氯离子是HCl或其他氯化物化合物通过获得电子而离解得到的离子,而氯酸盐是由氯酸(HClO3)或其他含有氯酸盐的化合物离解而产生的多原子离子。氯化物在氯上具有负电荷的氧化态,在Cl-上为-1。氯酸盐的氧化态是氯的正电荷,就像氯离子上的+5。
氯化物是由一个单原子组成的单原子离子,而氯酸盐是由氯和三个氧原子组成的多原子离子。氯化物容易氧化,氯酸盐也会发生氧化还原反应(氧化和还原)。根据VSEPR(Valance-Shell-Electron-Pair)理论,氯酸盐具有三角-金字塔结构。
氯化物的摩尔质量为35.45gmol-1,而氯酸盐的摩尔质量为83.45gmol-1。氯化物在生物学上是最重要的,因为它们在维持内部细胞环境(稳态)中起着作用。主要含氯化合物是氯化钠(食盐),而氯酸盐化合物是氯酸镁、氯酸钾等。
比较图
什么是氯化物(chloride)?
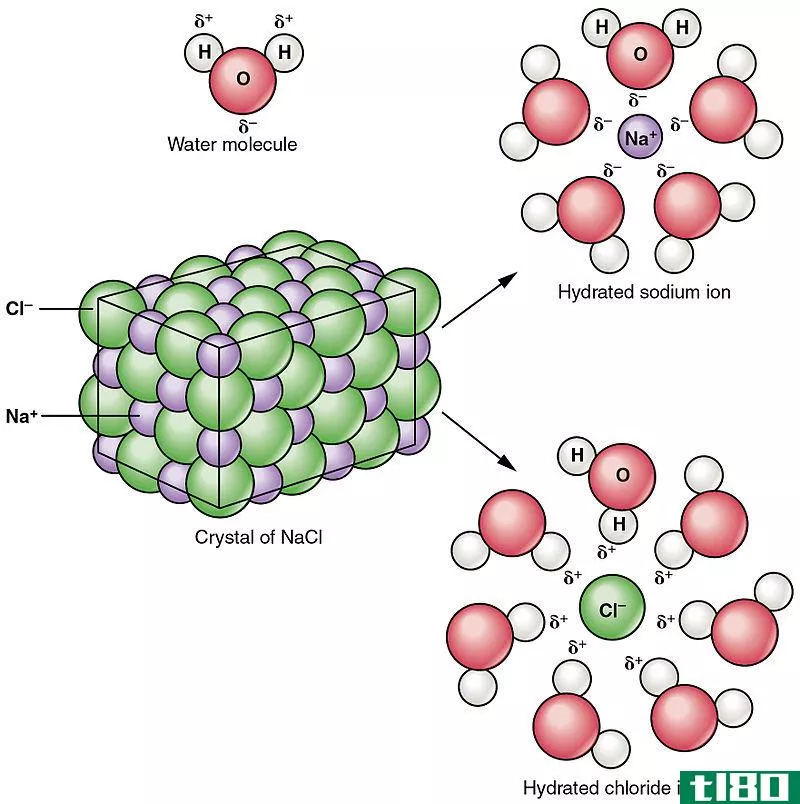
氯离子是一种阴离子,它是通过获得Cl-的电子而形成的。氯是一种单原子阴离子,它是由含有氯化物的化合物(如HCl)分解而成。氯原子比氯原子大得多,因为它的轨道上有一个额外的电子不稳定。氯化物是一种非常活泼的离子形式。氯化物只会氧化,因此氯化物的存在可能会导致大多数金属(如铝合金、不锈钢等)的严重腐蚀和小孔(点蚀)。
在生物学领域,Cl-离子作为细胞稳态的主要电解质。它们在神经元的动作电位(当膜电位迅速上升和下降时发生)的传递也起作用。人体内氯离子浓度的调节是通过肾脏进行的。它也是一些蛋白质的结构成分,如淀粉酶。
氯化物与金属形成盐,当它们溶解在水中时,它们形成氯化物,因为氯化物的盐是水溶性的。氯化物的一个例子是氯化钠(NaCl);它被认为是食盐中常见的氯化物,在水中极易溶解。作为一种电解质,它存在于维持酸碱平衡、体液调节和神经冲动传递的所有体液中。其他例子有NH4Cl(氯化铵)、MgCl2(氯化镁)、CaCl2(氯化钙)、Hg2Cl2(氯化亚汞)。
什么是氯酸盐(chlorate)?
氯酸盐也意味着任何氯氧阴离子如ClO3-。氯酸盐阴离子(ClO3-)是由氯酸(HClO3)和其他含有氯酸盐的化合物分解而来的氯酸盐。它可能以结晶、无色晶体或颗粒的形式出现。氯酸盐在氯上的氧化态为+5,是由氯和三个氧原子组成的多原子阴离子。它具有三角金字塔的几何形状,正如VSEPR理论所解释的那样。
氯酸盐天然存在于地球上干旱和超干旱地区,浓度相对较高。它们的特性是盐与有机溶剂、木屑等可燃化合物的混合物容易燃烧,这是通过传热燃烧的过程。氯酸盐,当暴露在易燃材料中时,由于氯酸盐离子在放热的氧气下分解而引起爆炸,从而加速燃烧过程。
氯酸盐被认为是由多个共振结构组成的杂化形式。氯酸盐也会发生氧化和还原反应,因为它们也是强大的氧化剂。
一些氯酸盐还与其他氧化态形成化合物,分别为次氯酸盐、亚氯酸盐、氯酸盐和高氯酸盐的+1、+3、+5、+7。
在工业规模上,可以用卤水(氯化钠水溶液)合成氯酸盐化合物氯酸钠(NaClO3)。它可以通过氯和氢氧化钠在50-70℃下的反应来实现。
示例
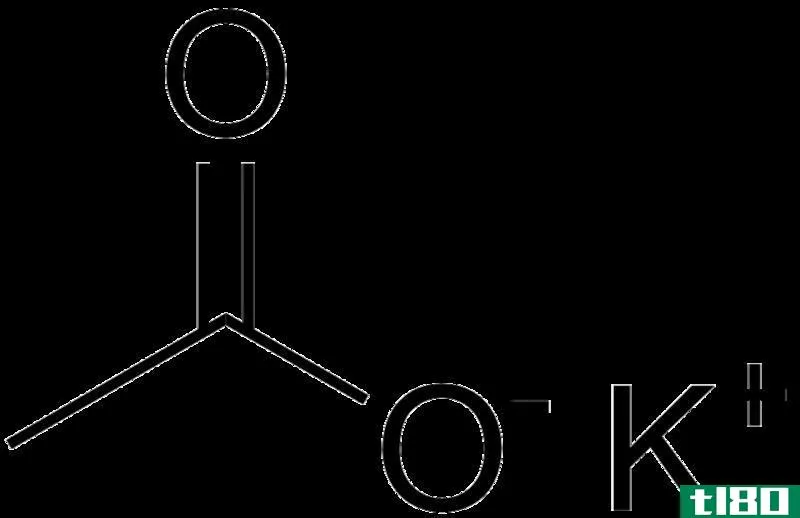
- 氯化钾:工业中最常见的氯酸盐
- 氯化钠制备的氯化钠在漂白纸中有着广泛的应用
- Mg(ClO3)2:白色水溶性化合物
主要区别
- 氯离子表示为Cl-,而氯酸根离子表示为Cl3-。
- 氯离子是HCl分解生成的阴离子,而氯酸根离子是HClO3产生的
- 氯是一种只有氯原子的单原子阴离子;另一方面,氯酸盐是一种含有氯和三个氧原子的多原子阴离子。
- 氯离子在氧化过程中只易被氧化,而氯酸根离子在氧化和还原的同时也会发生氧化还原反应。
- 氯化物的摩尔质量为35.45g/mol;氯酸盐的摩尔质量约为83.45g/mol。
- Cl–的氧化状态为-1;相反,ClO 3–的氧化状态为+5。
- 氯化物是单原子的;相反,氯酸盐是多原子的,具有三角金字塔的几何形状。
结论
氯化物是HCl解离产生的阴离子和其他氯化合物的-1氧化状态,而氯酸盐是氯酸离解产生的阴离子,具有+5氧化状态。