氯离子和氯酸盐的主要区别在于氯离子只含有一个原子,而氯酸盐阴离子含有四个原子。此外,氯在氯离子中的氧化态为-1,在氯酸根阴离子中为+5。
氯化物和氯酸盐都是氯的阴离子。氯是一种原子序数为17的化学元素。根据它的电子构型,在它最外层的p轨道上有一个不成对的电子。这种未配对的电子使氯具有高度的活性。它形成各种阴离子,包括氯化物和氯酸盐。让我们谈谈更多的细节。
目录
1. 概述和主要区别
2. 什么是氯化物
3. 什么是氯酸盐
4. 氯化物和氯酸盐的相似性
5. 并列比较-氯化物与氯酸盐的表格形式
6. 摘要
什么是氯化物(chloride)?
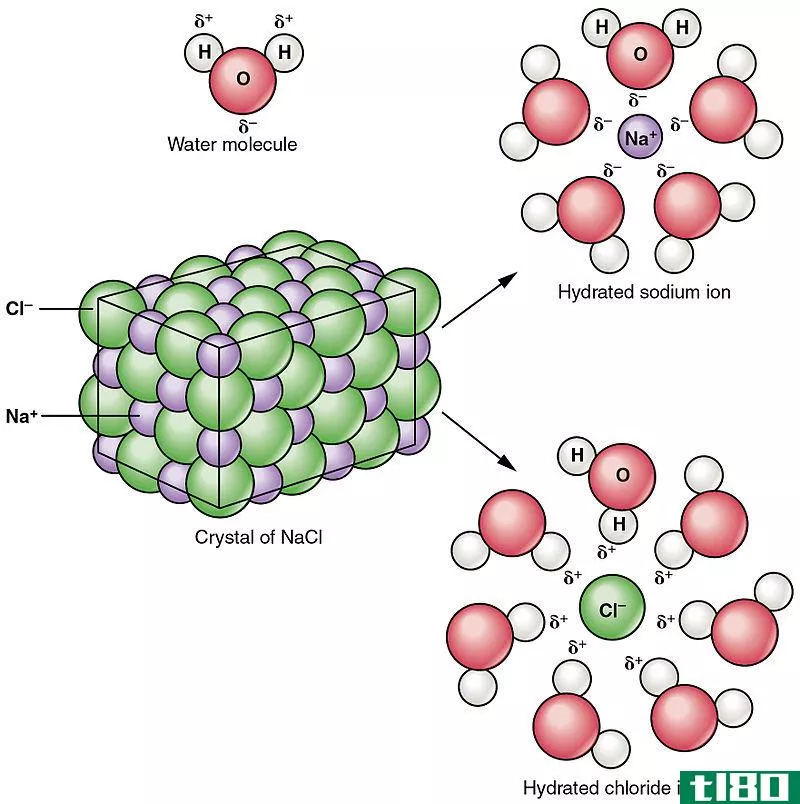
氯是氯的阴离子,具有化学式Cl-。根据氯原子的电子构型,它在最外层的p轨道上有一个未配对的电子。因此,它倾向于从外部获得一个电子,以完成其电子。这个进入的电子有负电荷。因此,它给氯原子额外负电荷,形成氯离子。
这个负离子的摩尔质量是35.5g/mol,它等于氯原子的摩尔质量,因为当我们把一个电子与中子和质子的质量比较时,它的质量可以忽略不计。然而,这个阴离子比氯原子大。而且,它是抗磁的。大多数含有这种阴离子的化合物都是高度水溶性的。考虑到这种阴离子的存在,海水中含有1.94%左右的氯离子。
什么是氯酸盐(chlorate)?
氯酸盐是氯的阴离子,化学式为ClO−3。这个阴离子有一个氯原子与三个氧原子结合;两个氯原子和一个氯氧键。除此之外,这个阴离子在氯原子上有一对孤电子。由于这种结构,这种阴离子具有多重共振结构。因此,氯原子在这里处于+5氧化状态。这个负离子的几何结构是三角金字塔几何。

图02:氯酸根离子的化学结构
这种化学物质起着强大的氧化剂的作用。这意味着它可以很容易地氧化其他物质,同时减少自身。我们可以在实验室里生产出含有这些离子的化合物。例如,氯气和热KOH之间的反应生成氯酸钾(KClO3)。然而,这些化合物的自然存在尚未得到证实。此外,含有这些阴离子的化合物具有相对毒性。
氯化物(chloride)和氯酸盐(chlorate)的共同点
- 它们都是阴离子
- 它们都带着净1电荷
- 氯化物和氯酸盐是氯的衍生物
氯化物(chloride)和氯酸盐(chlorate)的区别
氯是氯的阴离子,化学式为Cl-。它只有一个原子。该离子的摩尔质量为35.5g/mol,氯的氧化态为-1。氯酸盐是氯的阴离子,化学式为ClO−3。它有四个原子。这就是氯化物和氯酸盐之间的关键区别。此外,氯酸盐的摩尔质量为83.4g/mol,此外,该离子中氯的氧化态为+5。

总结 - 氯化物(chloride) vs. 氯酸盐(chlorate)
氯化物和氯酸盐都是氯的阴离子。氯离子和氯酸盐的区别在于氯离子只含有一个原子,而氯酸根离子含有四个原子。氯在氯离子中的氧化态为-1,在氯酸根阴离子中为+5。
引用
1“氯化物”,维基百科,维基媒体基金会,2018年7月23日。这里有2个。“氯酸盐”,维基百科,维基媒体基金会,2018年7月15日。此处提供
2“氯酸盐”,维基百科,维基媒体基金会,2018年7月15日。