主要区别
二氧化碳(CO2)和一氧化碳(CO)的主要区别在于,二氧化碳(CO2)含有两个共价键合的氧原子,而一氧化碳(CO)则含有一个共价键合的氧原子。
二氧化碳(co2)(carbon dioxide (co2)) vs. 一氧化碳(co)(carbon monoxide (co))
二氧化碳是大气中自然产生的气体,而一氧化碳不是天然的大气气体。1640年,让-巴蒂斯特·范·赫尔蒙特首次观测到二氧化碳,而亚里士多德首次观测到一氧化碳。二氧化碳在室温下是无毒气体;另一方面,一氧化碳对人和动物是有毒和致命的。二氧化碳含有两个由双键结合的氧原子;硬币的另一面,一氧化碳含有一个氧原子,氧原子与碳三重结合。
二氧化碳的偶极矩为零;另一方面,一氧化碳的偶极矩为0.122D。二氧化碳是动物呼吸系统的主要副产品,而一氧化碳则是化石燃料不完全燃烧、部分分解而产生的。二氧化碳的键长为116.3pm,而一氧化碳在碳和氧之间的键长为112.8pm。
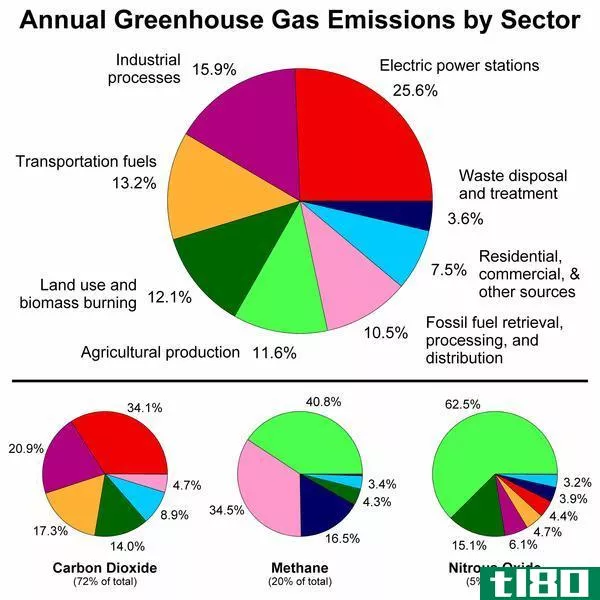
二氧化碳的摩尔质量为44g/mol,而一氧化碳的摩尔质量为28g/mol。二氧化碳是温室气体,而一氧化碳不是温室气体。碳在二氧化碳中带着+4的氧化状态;在另一方面,碳在一氧化碳中携带+2的氧化状态。
比较图
什么是二氧化碳(co2)(carbon dioxide (co2))?
1640年,Jan Baptist Van Helmont在密闭容器中进行木炭燃烧实验时首次观察到二氧化碳作为气体,当时他观察到一种气体从容器中演化出来。处于冰冻状态,称为干冰。二氧化碳是一种无味的气体,低浓度时无色,而高浓度时呈酸性,味道强烈。大气中二氧化碳的含量已上升到0.04%或412ppm的水平。在室温下是不易燃、无毒的气体。它溶解在水中形成碳酸,这也是海洋酸化的一个原因。
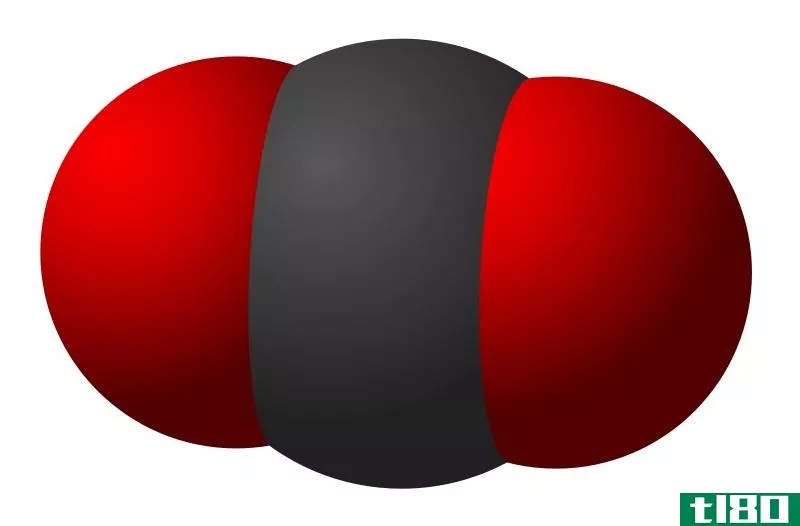
二氧化碳是一种无机化合物,因为气体中有两个氧原子通过双键共价结合到每个氧原子上,每个氧原子的摩尔质量为44g/mol。碳氧共价键的键长为116.3ppm。它的偶极矩为零,因为它是一个线性分子,两个氧原子位于中间碳的对侧。
二氧化碳是有氧生物和发酵的呼吸副产品。在大气中,二氧化碳的主要来源之一是化石燃料的燃烧,这导致二氧化碳演变为全球变暖的根源。它以温室气体的形式存在于大气中,因为它能将辐射捕获并排出大气层。动物呼出二氧化碳,植物进一步利用二氧化碳来维持自然界的平衡。
应用
二氧化碳可作为食品添加剂、碳酸饮料、葡萄酒工业中保存的干冰、灭火器、石油回收、制冷剂等。
什么是一氧化碳(co)(carbon monoxide (co))?
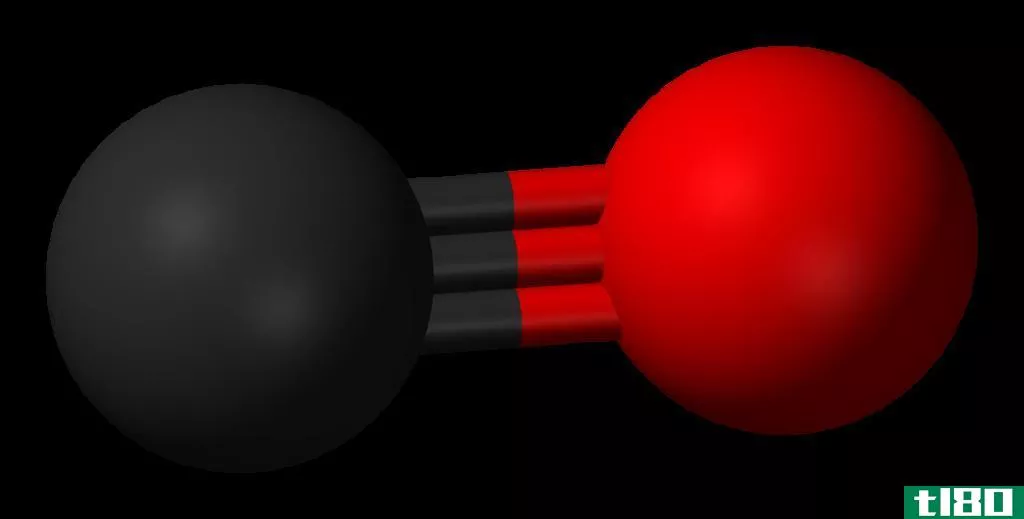
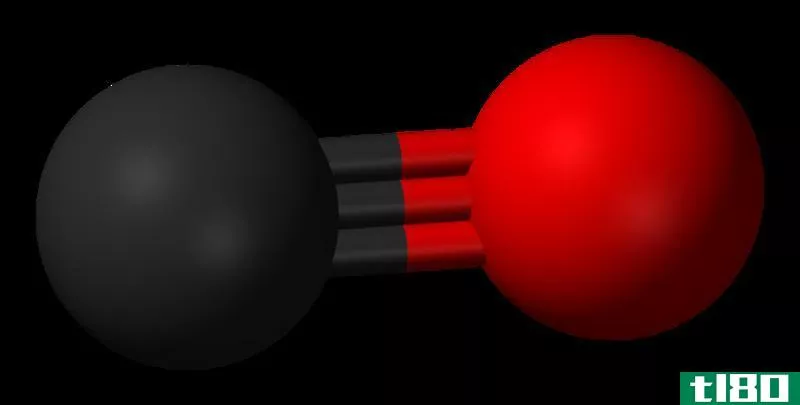
亚里士多德第一次观察到一氧化碳是在燃烧煤时产生有毒烟雾的。一氧化碳含有一个碳原子和一个氧原子,它们由一个σ和两个π键结合,偶极矩为0.122D,键长为112.8pm。因为分子量比空气轻,所以密度比空气稍低。在配位化学中,一氧化碳是配位体与金属离子结合的强配位体。
当氧气携带-2电荷时,碳在CO中的氧化状态为+2。一氧化碳是一种易燃、有毒、无色、无味的气体。它是由于化石燃料(包括煤、石油和天然气)不完全或部分燃烧(燃烧)而在大气中产生的。CO的最大天然来源是对流层,光化学反应每年产生约5×1012kg。
毒性
它是许多国家致命的空气中毒气体之一,因为**的正常耐受水平低于2.3%,但新生儿的耐受水平却高达约12%。低浓度的一氧化碳667ppm可能会导致人体50%的氧化血红蛋白转化为碳氧血红蛋白。一氧化碳与血红蛋白结合,血红蛋白是携带氧气的蛋白质,它掩盖了血液中的氧气含量。一氧化碳中毒的症状有头晕、头痛、恶心、呕吐、疲劳等。神经系统疾病也会出现定向障碍、视觉障碍、癫痫发作和意识混乱。
主要区别
- 二氧化碳最早是由让-巴蒂斯特·范·赫尔蒙特(Jean-Baptist Van Helmont)发现的,而一氧化碳则是亚里士多德(Aristotle)首次观测到的。
- 二氧化碳含有两个氧原子,而一氧化碳含有一个氧原子。
- 二氧化碳是双共价键;另一方面,一氧化碳是三重键。
- 二氧化碳在碳和氧之间的键长为116.3pm;在另一方面,一氧化碳在碳和氧之间的键长为112.8pm。
- 二氧化碳是有氧呼吸和发酵的呼吸副产品,而一氧化碳是由化石燃料的部分分解产生的。
- 二氧化碳是大气中自然产生的气体;另一方面,一氧化碳不是大气中的天然气。
- 二氧化碳是维持地球温度的温室气体,而一氧化碳对动物来说是有毒和致命的气体。
- 二氧化碳的偶极矩为零,因为它是一个线性分子;硬币的另一面,一氧化碳的偶极矩为0.122D。
- 二氧化碳在碳上的氧化状态为+4;另一方面,一氧化碳在碳上的氧化状态为+2。
- 二氧化碳不发生氧化反应,而一氧化碳则表现出氧化反应。
结论
二氧化碳是一种含有两个氧原子的天然呼吸副产品,而一氧化碳是含有一个氧原子的化石燃料部分分解的产物。