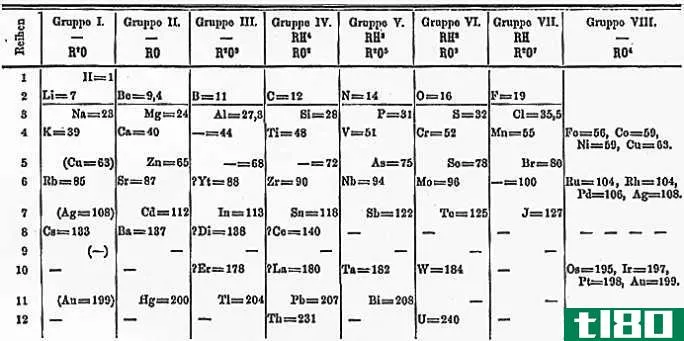
化学中的周期表定义
元素周期表是通过增加原子序数对化学元素进行的表格排列,显示元素,以便人们可以看到其性质的趋势。俄国科学家德米特里·门捷列夫(Dmitri Mendeleev)最常被认为是发明了元素周期表(1869年)。现代的元素周期表是从门捷列夫的元素周期表衍生出来的,但有一个显著的不同。门捷列夫的表格是根据原子量的增加而不是原子序数来排列元素的。然而,他的表格说明了元素属性的重复趋势或周期性。

又称:元素周期表、元素周期表、化学元素周期表
关键要点:周期表定义
- 元素周期表是一种化学元素的表格排列,它是根据重复出现的性质,通过增加原子序数和元素组来排列的。
- 周期表的七行称为周期。这些行的排列方式是,金属在桌子的左侧,非金属在桌子的右侧。
- 这些列称为组。组包含具有类似属性的元素。
组织
元素周期表的结构使人们能够一目了然地看到元素之间的关系,并预测不熟悉、新发现或未发现元素的性质。
时期
周期表有七行,称为周期。元素原子序数在一个周期内从左向右移动。周期左侧的元素是金属,右侧的元素是非金属。在桌子上向下移动一个周期会增加一个新的电子壳层。
组
元素的列称为组或族。组的编号从1(碱金属)到18(惰性气体)。具有基团的元素具有价电子构型。群中的元素显示出与原子半径、电负性和电离能有关的图案。随着连续元素获得电子能级,向下移动一个组时,原子半径增加。向下移动一个基团时,电负性降低,因为添加一个电子壳层会将价电子推离原子核更远。向下移动一组元素,元素的电离能会逐渐降低,因为它更容易从最外层移除电子。
阻碍
块是周期表中表示原子外层电子亚壳层的部分。s-段包括前两组(碱金属和碱土)、氢和氦。p-块包括组13至18。d-块包括第3组到第12组,它们是过渡金属。f区块由周期表主体下方的两个周期(镧系元素和锕系元素)组成。
金属、类金属、非金属
三大类元素是金属、类金属或半金属以及非金属。金属元素在周期表的左下角最高,而大多数非金属元素在右上角。
大多数化学元素是金属。金属往往有光泽(金属光泽)、坚硬、导电,并且能够形成合金。非金属倾向于柔软、有色、绝缘体,并且能够与金属形成化合物。类金属显示介于金属和非金属之间的性质。在元素周期表的右边,金属转变成非金属。从硼开始,经过硅、锗、砷、锑、碲和钋,有一个粗糙的阶梯状图案,确定了类金属。然而,化学家越来越多地将其他元素归类为类金属,包括碳、磷、镓等。
历史
德米特里·门捷列夫和朱利叶斯·洛萨·迈耶分别于1869年和1870年独立出版了周期表。然而,迈耶已经在1864年出版了一个早期版本。门捷列夫和迈耶都通过增加原子量来组织元素,并根据重复特征来组织元素。
还制作了其他几个早期表格。1789年,安托万·拉瓦锡将元素组织成金属、非金属和气体。1862年,Alexandre Emile Béguyer de Chancourtois发表了一个称为地球螺旋或螺旋的周期表。该表可能是第一个按周期性属性组织元素的表。
来源
- 张,R.(2002)。化学(第7版)。纽约:麦格劳·希尔高等教育。ISBN 978-0-19-284100-1。
- 埃姆斯利,J.(2011)。自然的积木:元素的A-Z指南。纽约:牛津大学出版社。ISBN 978-0-19-960563-7。
- 格雷,T.(2009)。元素:对宇宙中每一个已知原子的视觉探索。纽约:黑狗出版社。ISBN 978-1-57912-814-2。
- 格林伍德。;恩肖,A.(1984年)。元素的化学性质。牛津:佩加蒙出版社。ISBN 978-0-08-022057-4。
- 梅亚,法学;等人(2016年)。“2013年元素原子量(IUPAC技术报告)”。纯化学和应用化学。88 (3): 265–91. 内政部:10.1515/pac-2015-0305
- 发表于 2021-09-15 16:56
- 阅读 ( 419 )
- 分类:化学
你可能感兴趣的文章
门捷列夫(mendeleev)和现代周期表(modern periodic table)的区别
... 门捷列夫的主要区别(main difference mendeleev) vs. 现代周期表(modern periodic table) 元素周期表是化学元素按其化学和物理性质排列的表。现代元素周期表是在一系列不同版本的元素周期表之后产生的。俄罗斯化学家/教授德米特...
- 发布于 2021-06-27 12:49
- 阅读 ( 226 )
卤素(halogen)和氙(xenon)的区别
...别(main difference halogen) vs. 氙(xenon) 卤素和氙是分别包含在周期表第7组和第8组中的化学元素。卤素是非常活泼的元素。但氙气是一种反应性较弱的元素。卤素是周期表第7组中的化学元素,包括F、Cl、Br、I和At。它们具有不同的物...
- 发布于 2021-06-29 10:46
- 阅读 ( 448 )
锰(manganese)和镁(magnesium)的区别
...相同的原子。迄今为止发现的所有化学元素都被列入元素周期表。这个元素周期表根据原子核中质子数量的升序来显示化学元素。锰和镁就是这样的化学元素。锰的原子中有25个质子。镁的原子中有12个质子。锰和镁具有不同的...
- 发布于 2021-06-29 11:38
- 阅读 ( 483 )
原子半径(atomic radius)和离子半径(ionic radius)的区别
...原子的半径。 覆盖的关键领域 1.什么是原子半径-定义,周期表中的趋势2.什么是离子半径-定义,周期表中的趋势3.原子半径和离子半径之间的区别是什么-主要区别的比较 Key Terms: Atomic Radius, Atoms, Electron Shell, Ionic Radius, I*** 什么...
- 发布于 2021-06-29 14:30
- 阅读 ( 975 )
镁(magnesium)和氧化镁(magnesium oxide)的区别
...ium) vs. 氧化镁(magnesium oxide) 镁是一种碱土金属,属于元素周期表的第2族。它能形成许多基本化合物。镁通常通过形成镁二价阳离子形成离子化合物。氧化镁就是这样一种离子化合物。它是白色固体。镁和氧化镁的主要区别在于...
- 发布于 2021-06-29 20:15
- 阅读 ( 503 )
d(d)和f块元素(f block elements)的区别
...部分。所有化学元素都按原子序数递增的顺序排列在元素周期表中。周期表中还有四组元素:s块、p块、d块和f块。元素根据它们的电子构型被分为这些组。例如,s块元素的最外层电子在s轨道上。p块元素在p轨道上有最外层的电...
- 发布于 2021-06-29 23:23
- 阅读 ( 456 )
铑(rhodium)和银(silver)的区别
...主要区别(main difference rhodium) vs. 银(silver) 铑和银是元素周期表第5周期中的两种d块元素。铑是一种非常坚硬的金属,具有非常高的熔点和沸点。它的外观与银相似,但化学性质却截然不同。银是一种非常有光泽和贵重的金属,自...
- 发布于 2021-06-30 11:45
- 阅读 ( 916 )
反应性在化学中意味着什么?
...个定义是,它是对化学反应及其动力学的科学研究。 周期表中的反应性趋势 元素周期表上的元素组织允许对反应性进行预测。高电正性和高电负性元素都有强烈的反应倾向。这些元素位于周期表的右上角和左下角以及某些元...
- 发布于 2021-09-10 12:37
- 阅读 ( 328 )
化学101-主题介绍和索引
...接触化学。不知道从哪里开始?试试化学基础。 元素周期表 你需要一个可靠的元素周期表,几乎涵盖化学的所有方面!还有指向元素组特征的链接。 元素周期表 可打印周期表 元素组周期表 有用的资源 使用这些资源...
- 发布于 2021-09-15 11:49
- 阅读 ( 282 )
化学中的价定义
...为4,因为可以接受4个电子来填充2p轨道。 共价 元素周期表主族中的元素原子可能显示出介于1和7之间的价态(因为8是一个完整的八重态)。 第1组(I)-通常显示1的价态。示例:NaCl中的Na 第2组(II)-典型价态为2。示例:...
- 发布于 2021-09-15 16:52
- 阅读 ( 292 )