多原子离子和化合物之间的关键区别在于,多原子离子具有正电荷或负电荷,而化合物没有净电荷。
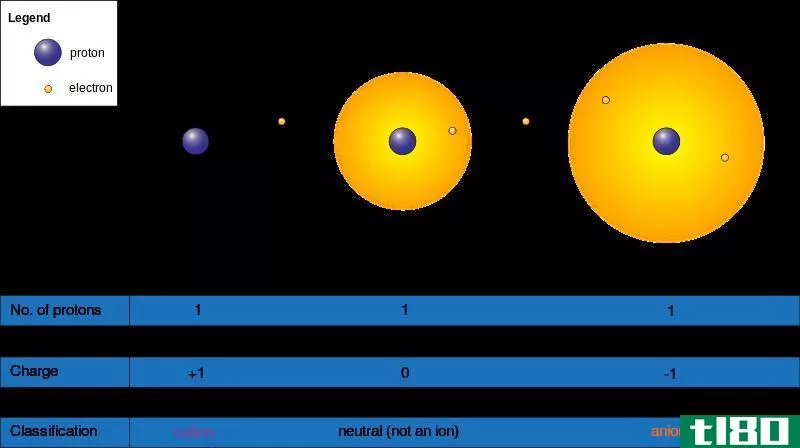
多原子离子是一个术语,我们用它来命名含有两个或两个以上带负电荷或正电荷的原子的化学物种。这个离子的电荷是由每个原子中的电子数决定的;如果原子中的电子数多于质子的总数,它就会得到净负电荷,反之亦然。另一方面,化合物是不带电荷的化学物质。它们有相等数量的电子和质子。
目录
1. 概述和主要区别
2. 什么是多原子离子
3. 什么是化合物
4. 并列比较-多原子离子与表格形式的化合物
5. 摘要
什么是多原子离子(polyatomic i***)?
多原子离子是具有两个或多个原子和一个净电荷的化学物种。这种电荷可以是正电荷,也可以是负电荷,这取决于化学物质中存在的电子和质子的数量。这个物种的同义词是“分子离子”。原子以共价方式相互结合。我们可以把一些金属配合物看作是多原子离子,如果它们作为一个单一的单元。相反,单原子离子是带电荷的单原子。我们可以在盐化合物、配位化合物和许多其他离子化合物中发现这些离子;作为化合物的一部分。
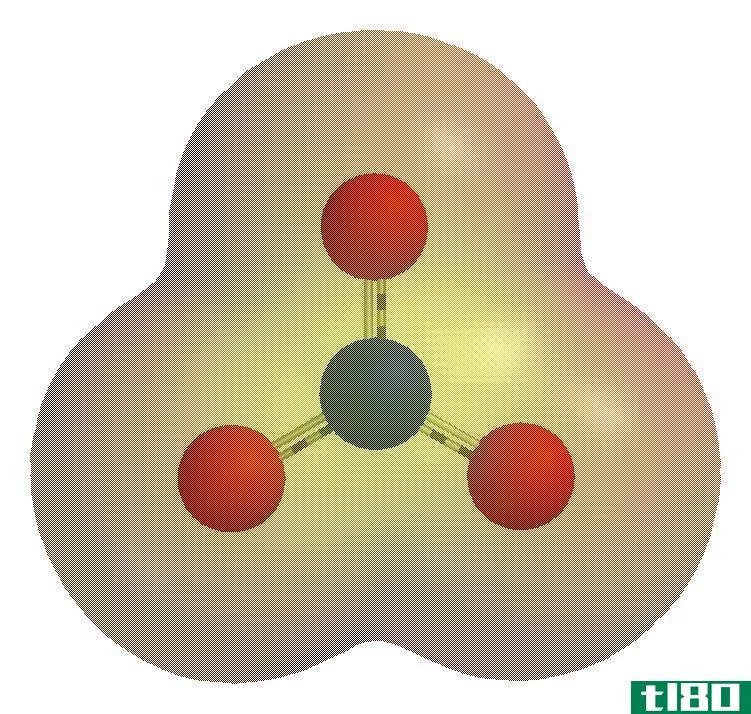
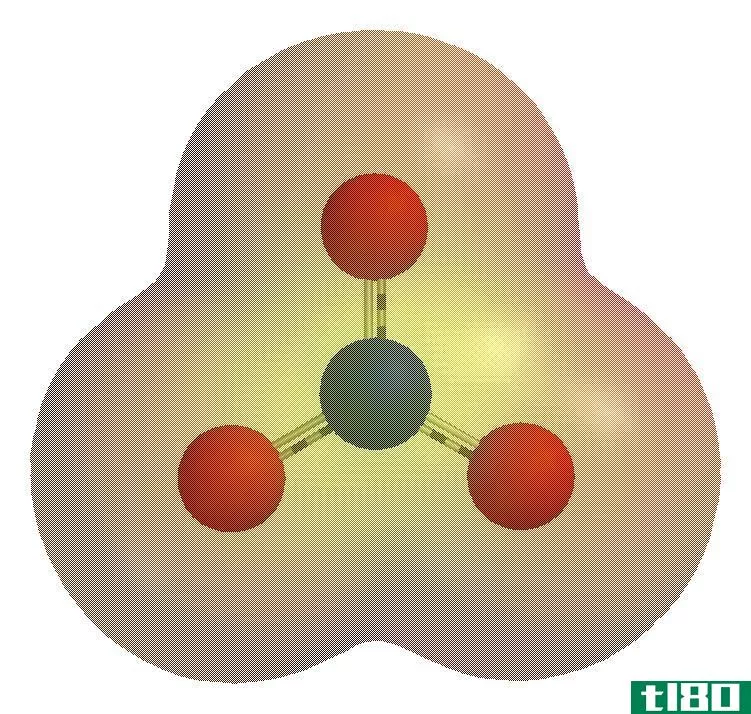
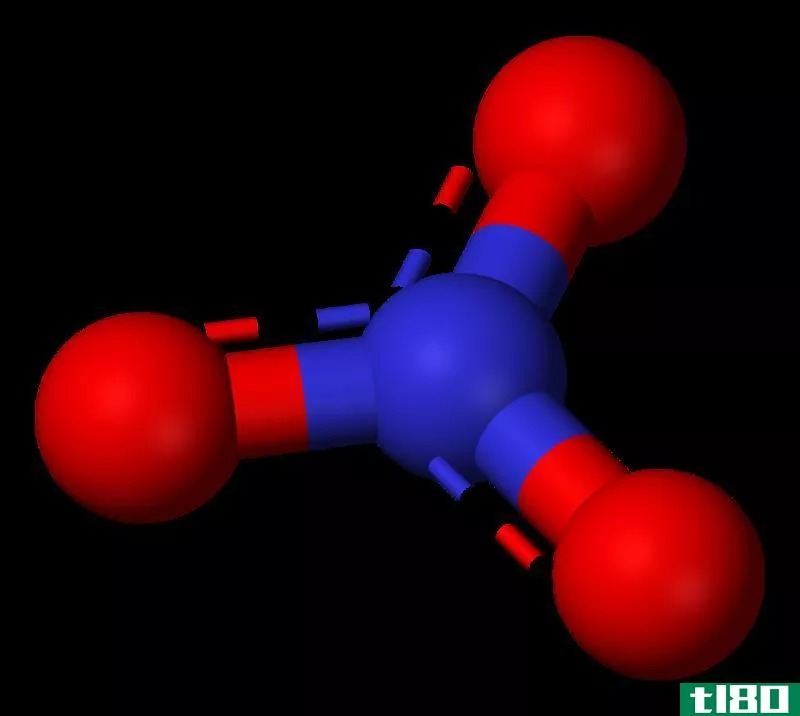
图01:硝酸根离子
多原子离子的一些例子:
- 乙酸离子(CH3COO-)
- 苯甲酸盐离子(C6H5COO-)
- 碳酸盐离子(CO32-)
- 氰化离子(CN-)
- 氢氧化物离子(OH-)
- 亚硝酸盐离子(NO2-)
- 铵离子(NH4+)
什么是化合物(compounds)?
化合物是由两个或两个以上化学元素的原子组成的含有相同分子的化学物种。因此,这些化学物质不携带净电荷。因此,它们是中性种。原子通过共价键、配位键或离子键相互结合。此外,如果一个分子含有两个或两个以上同一元素的原子,则它不是化合物,因为没有不同的元素。
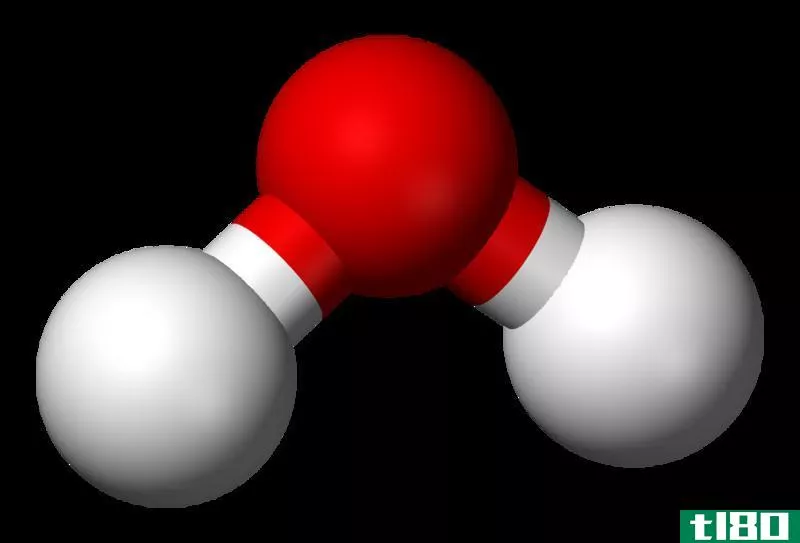
图02:水分子
此外,根据定义,有以下4种化合物:
- 具有不同化学元素组合的分子
- 离子化合物由离子键组成
- 具有金属键的金属间化合物
- 配位络合物由配位键组成
我们可以用一个化学式来表示化合物中的化学元素和它们之间的比例。例如,水分子的化学式是H2O,它有两个氢原子和一个氧原子,但分子没有净电荷,因此它是一种化合物。
多原子离子(polyatomic i***)和化合物(compounds)的区别
多原子离子是具有两个或多个原子和一个净电荷的化学物种。它们有正电荷或负电荷。化合物是由两个或两个以上化学元素的原子组成的含有相同分子的化学物种。它们没有净电荷。这就是多原子离子和化合物之间的关键区别。此外,多原子离子在原子间既有共价键,也有配位键。然而,化合物可以有共价键、离子键、金属键或原子间的配位键。
下面的信息图以表格形式展示了多原子离子和化合物之间的区别。

总结 - 多原子离子(polyatomic i***) vs. 化合物(compounds)
多原子离子与化合物的关键区别在于,多原子离子具有正负电荷,而化合物没有净电荷。这主要是因为多原子离子的电子和质子数量不平衡,而化合物的电子和质子数量相等。
引用
1Helmenstine,Anne Marie博士,“多原子离子的定义和示例”,ThoughtCo,2018年6月22日
2Noller,Carl R.等人。“化合物”,《大英百科全书》,大英百科全书,2016年12月6日。