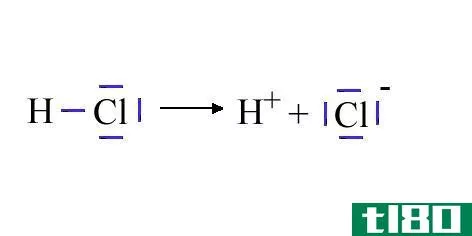自由基和离子的关键区别在于自由基有一个或多个不成对电子,而离子有成对电子。
我们可以从离子和自由基的基本性质来解释自由基和离子的区别。由于电子的损失或增加,离子可以作为带有电荷(正电荷或负电荷)的分子或原子出现。离子由于电子的增加而带负电荷,而由于失去电子而保持正电荷。离子可能以单电荷或多电荷化学物质的形式出现,这取决于获得或丢失的电子数。自由基是至少有一个不成对电子的分子或原子。本文介绍了自由基和离子的区别,包括它们的特点。
目录
1. 概述和主要区别
2. 什么是自由基
3. 什么是离子
4. 并列比较-自由基与离子的表格形式
5. 摘要
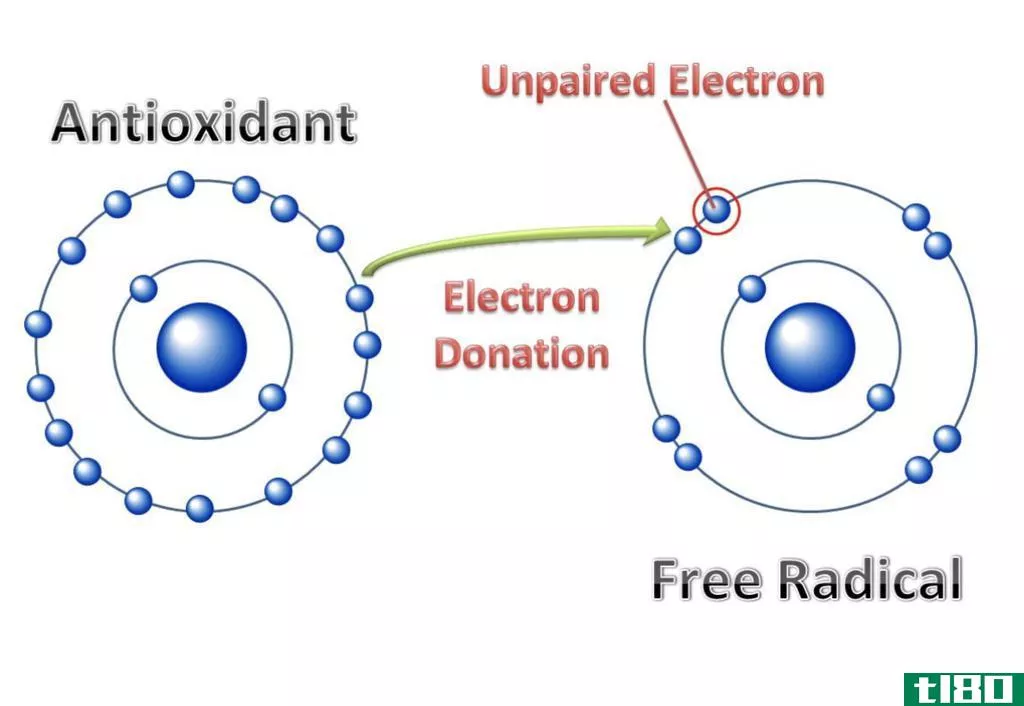
什么是自由基(free radical)?
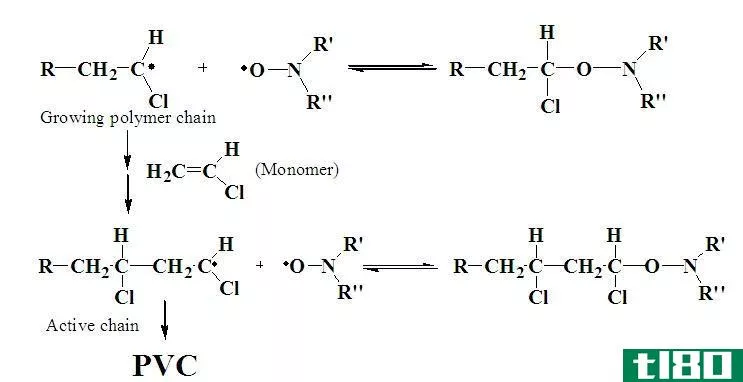
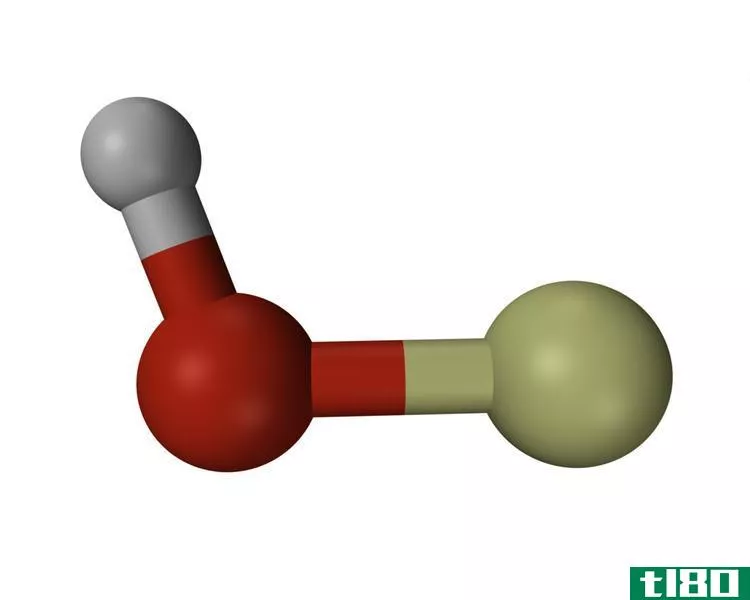
自由基是一个或一组含有一个或多个未成对电子的原子。由于存在不成对的电子,它们具有很高的反应性。自由基非常不稳定,试图通过接受所需的电子来获得稳定性。它们通过捕捉所需的电子与其他化合物发生反应。自由基是自然过程中重要的中间产物。我们可以用右边的一个上标点来表示自由基。例如,H.,Cl.,HO.,H3C。
图01:羟基自由基
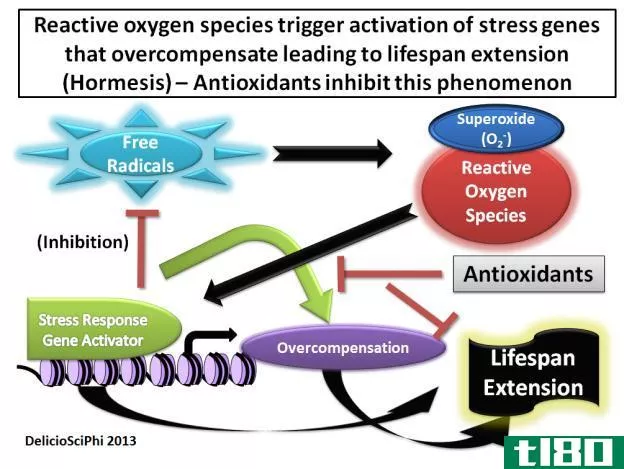
长寿命自由基分为三类:稳定自由基、持久自由基和双自由基。
- 稳定自由基:稳定自由基的主要例子是分子氧O2。含共轭π体系的有机自由基可以长寿。
- 持久性自由基:由于自由基中心周围的空间位阻拥挤,使它们很难与另一个分子发生反应,所以它们的寿命很长。
- 双自由基:有些分子有两个自由基中心,我们称之为二自由基。分子氧(大气中的氧)是以双向的形式存在的。
什么是离子(ion)?
当一种化学物质在化学反应中获得或失去电子时,就会形成离子;它们带有正电荷(+)或负(-)。它们通过接受电子而获得负电荷,通过向缺电子分子或元素提供电子而获得正电荷。接受或给予电子直接影响离子的大小;它会显著改变分子大小。我们把一个或一组没有正负电荷的原子称为“中性”;要成为中性原子或分子,质子的数量必须与电子的数量相同。
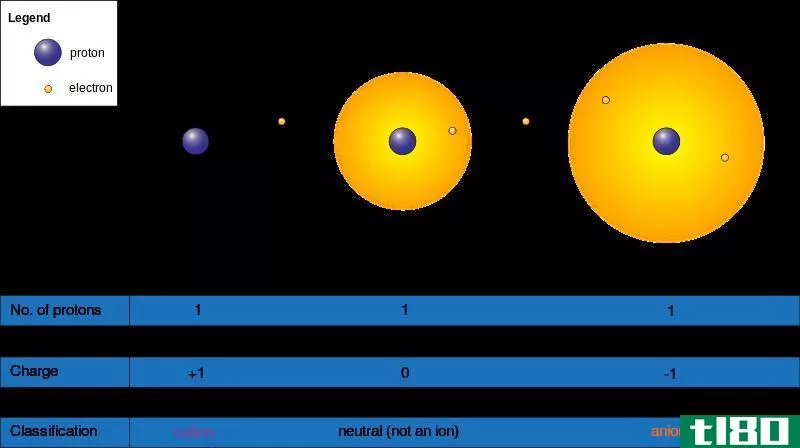
图02:阳离子和阴离子的形成
因此,有两种形式的离子如下。
- 阳离子或(+)离子-通常金属属于这一类,因为金属失去电子变成正(+)电荷(Na+、Ba2+、Ca2+、Al3+)
- 阴离子(-)离子-通常非金属属于这一类,因为非金属获得电子变成负(-)电荷(Cl-,S2-,O2-,Br-)
自由基(free radical)和离子(ion)的区别
自由基和离子的关键区别在于自由基有一个或多个不成对电子,而离子有成对电子。因此,自由基非常不稳定,而离子相对稳定。因此,这也是自由基和离子的显著区别。然而,当大多数离子与相反电荷的离子结合时,自由基可以自行存在。当更多地考虑它们的稳定性时,自由基通过接受电子而变得稳定,但是当离子与带相反电荷的化合物形成络合物时,它们是稳定的。
自由基和离子的另一个重要区别是,离子总是带电荷的,但是自由基不是带电的物种,即使它们有不成对的电子。这种差别的产生是因为,在离子中,电子的总数总是不等于原子核中的质子数,而在自由基中,电子数等于质子数。
下面的信息图提供了关于自由基和离子之间区别的更多细节。
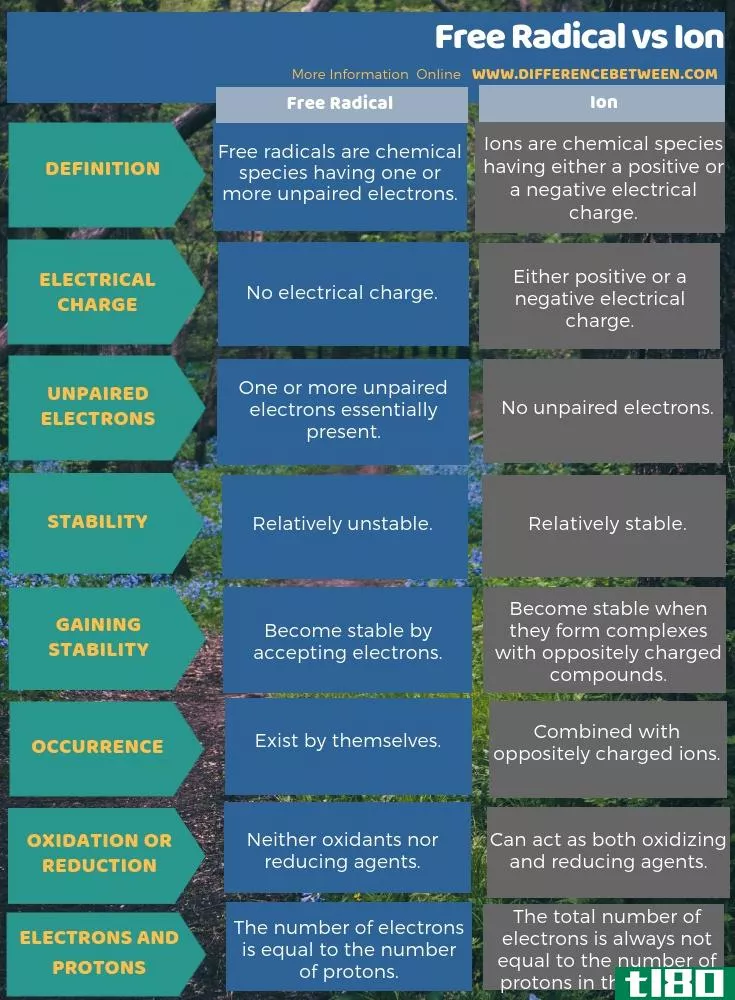
总结 - 自由基(free radical) vs. 离子(ion)
我们可以用属于某一物种的电子数来描述自由基和离子。这里,自由基和离子最显著的区别是自由基有不成对的电子,而离子有成对电子。因此,自由基更具反应性。另一方面,离子通过与带相反电荷的离子/分子形成化合物而变得化学稳定。
引用
1“激进(化学)。”维基百科,维基媒体基金会,2018年10月8日。这里有2个。“Ion.”维基百科,维基媒体基金会,2018年10月16日。可在此处查阅
2“离子”,维基百科,维基媒体基金会,2018年10月16日