离子与电子
电子和离子之间有许多不同之处,其中包括大小、电荷和性质。电子是带负电的微粒,而离子则是带负电或正电荷的分子或原子。电子的性质可以用“量子力学”来解释,但离子的性质可以用普通化学来解释。电子(符号:β-或℮-)是亚原子粒子,它没有子粒子或子结构。但是,离子可以有更复杂的结构和子成分。
什么是电子(an electron)?
电子第一次被J.J.Thompson发现是在1906年,当时他正在研究被称为电子束的阴极射线。他发现电子是带负电的微粒。他曾称它们为“微粒”,而且,他发现电子是原子的一个元素,它比氢原子小1000多倍。电子的大小大约是质子的1/1836。
根据玻尔的理论,电子绕着原子核运行。但后来,作为科学实验的结果,人们发现电子的行为更像电磁波,而不是绕轨道运行的粒子。
什么是离子(an ion)?
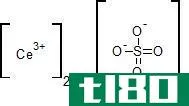
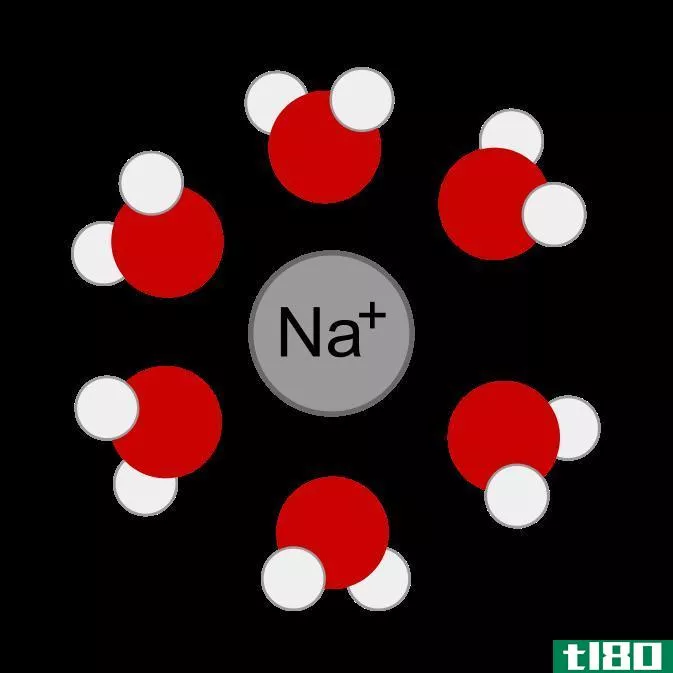
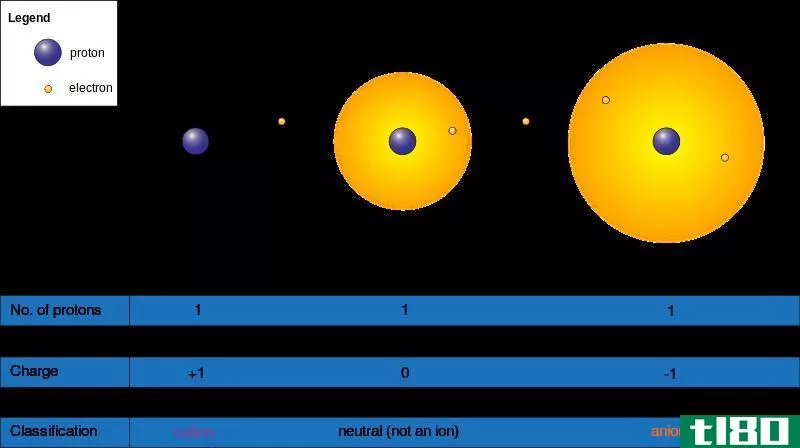
如前所述,离子不是带负电就是带正电的分子或原子。原子和分子都可以通过接受或除去电子而形成离子。它们通过去除电子获得正电荷(K+、Ca2+、Al3+),通过接受电子获得负电荷(Cl-、S2-、Al3-)。离子形成时,电子的数目不等于质子的数目。然而,它不会改变原子/分子中质子的数量。一个或多个电子的得失对母体原子/分子的物理和化学性质有着重要的影响。
电子(electr***)和离子(i***)的区别
•电荷:
•电子被认为是带负电荷的基本粒子,但可以是正的也可以是负的。
带正电荷的离子称为“正离子”,带负电荷的离子称为“负离子”。离子是通过接受或给予电子而形成的。
–正离子示例:Na+、Ca2+、Al3+、Pb4+、NH4+
-负离子示例:Cl-,S2-,AlO3–
•尺寸:
•与离子相比,电子是非常小的粒子。
•离子的大小取决于几个因素。
•电子的大小是一个固定值,大约是质子的1/1836。
•原子结构:
•电子不是多原子或单原子。电子不能相互结合形成化合物。
•离子可以是多原子或单原子;单原子离子只包含一个原子,而多原子离子包含多个原子。
–单原子离子:Na+、Ca2+、Al3+、Pb4+
–多原子离子:ClO 3–,SO43-
•颗粒物:
•电子是微粒,具有波粒特性(波粒二象性)。
•离子仅被视为粒子。
•要素:
•电子被认为是元素粒子。换句话说,电子不能被分成更小的组分或子结构。
•所有离子都有子成分。例如,多原子离子包含各种原子;原子可进一步细分为中子、质子、电子等。
•属性:
•所有电子都具有类似的波粒特性,这可以用量子力学来解释。
•离子的化学和物理性质因离子而异。换句话说,不同的离子有不同的化学和物理性质。
- Pair production by Davidhorman (CC BY-SA 3.0)
- An electrostatic potential map of the nitrate ion (NO3−) via Wikicomm*** (Public Domain)