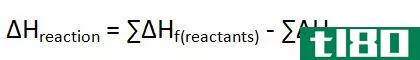主要区别
生成热和反应热的主要区别在于,生成热是一摩尔化合物形成过程中释放或吸收的能量变化的集合,而反应热是在任何化学反应过程中释放或吸收的能量变化的总和。
生成热(heat of formation) vs. 反应热(heat of reaction)
生成热是元素形成过程中能量值的变化,而反应热是反应过程中增加或释放的能量。焓的变化,通常发生在元素的发展过程中,是由生成热给出的,而化学反应中的总热量是由反应热来增加或释放的。
生成热在化学上写为Hreaction=Hf(反应物)–⅀Hf(产物);另一方面,反应热的化学形式为ΔH⊖rxn=∑ΔH⊖f{产物−∑ΔH⊖f{反应物}。
生成热的标准符号为∆Hf;相反,反应热的符号为∆Hr。
比较图
什么是生成热(heat of formation)?
形成热的概念被定义为当一个元素的一摩尔从其整体元素中产生时,焓的改变或变化称为生成热。换言之,它被定义为在25°C和77°F的温度下,在一个大气压下,当一摩尔化合物从其组成元素中产生,并且每种物质都以其正常物理状态存在时释放或吸收的热量。
当以标准速率生产各种物质时,这种热称为标准生成热,其条件为298.15开尔文温度和1 atm压力。
IUPAC给出的标准压力为105 Pa(1bar)。虽然目前还没有确定的标准温度,但这就是形成热的恒压可用的原因。生成热的单位是KJ/摩尔,因为我们只考虑一摩尔的生成。
生成热用∆Hf表示。这个符号可以用一个等式来计算。生成热的化学形式为Hreaction=Hf(反应物)–⅀Hf(产物)。这个方程意味着标准生成热通常等于产物的标准变化生成焓和反应物的标准变化生成焓之和的差值。
以石墨形成二氧化碳为例,石墨是碳的纯元素形式,氧源是一种特殊的双原子分子。当这种生成反应在标准规定的条件下发生,并且测量到焓的变化时,则该反应称为生成热。
什么是反应热(heat of reaction)?
反应热的概念定义为化学反应过程中吸收或释放的能量的总和,称为反应热。化学反应过程中的热焓变化是在恒定的压力下发生的,反应热在环境中被吸收或释放,以使反应物在化学反应过程中保持恒定的给定温度。
反应热一般是按某一特定物质的摩尔数来计量的,所以它的单位是千焦每摩尔。当反应热为标准速率时,这称为标准反应热或标准反应焓变。在1巴压力和适用温度下使用纯标准速率,以确定物质的纯标准速率。
反应热在化学上是这样写的,符号∑是希腊语的sigma,意思是“和”。标准反应热通常等于反应物的所有标准生成热的加成减去所有反应物的标准生成热的加成。
如果反应热为正值,则意味着热量从外部被吸收到反应中(吸热),但如果在反应热过程中出现负值,则意味着热量从反应到环境(放热)被给予外部。∆Hr是反应热的符号。
反应热或称为焓的变化,不直接由反应的特定通道决定,而只取决于反应物和产物的完整能级。
主要区别
- 在一摩尔化合物由其组成元素形成过程中能量值的变化称为生成热,而在化学反应过程中增加或释放的净能量称为反应热。
- 生成热给出了焓的变化的概念,这种变化通常发生在元素的发展过程中,而反应热给出了化学反应中释放或吸收的总热量的概念。
- Hreaction=Hf(反应物)–⅀Hf(产物)是生成热的通式;另一方面,反应热的通式是ΔH⊖rxn=∑ΔH⊖f{产物−∑ΔH⊖f{反应物}。
- ∆Hf是生成热的符号;相反,∆Hf是反应热的符号。
结论
上述讨论得出结论,生成热是化合物形成过程中释放或吸收的能量变化的总和,用∆Hf表示,而反应热通常是在任何化学反应过程中释放或吸收的能量变化的总和,用∆Hr表示。