平衡常数与生成常数的关键区别在于,平衡常数是平衡时产物浓度与反应物浓度之比,而生成常数是由其组分形成配位化合物的平衡常数。
平衡常数有助于解释不同平衡态的行为。形成常数是一种平衡常数,对配位化合物的形成有特殊作用;例如,络合离子。
目录
1. 概述和主要区别
2. 什么是平衡常数
3. 什么是形成常数
4. 并列比较-平衡常数与表格形式的形成常数
5. 摘要
什么是平衡常数(equilibrium c***tant)?
平衡常数是平衡时产物浓度与反应物浓度之比。这个术语只用于平衡的反应。对于处于平衡状态的反应,反应商和平衡常数是相同的。
平衡常数也作为浓度增加到化学计量系数的幂次而给出。由于温度影响组分的溶解度和体积膨胀,平衡常数取决于所考虑体系的温度。然而,平衡常数方程不包括反应物或产物中固体的任何细节。只考虑液相和气相的物质。
例如,让我们考虑碳酸和碳酸氢根离子之间的平衡。
H2CO3(水)↔ HCO3–(aq)+H+(aq)
上述反应的平衡常数如下所示。
平衡常数(K)=[HCO3–(aq)][H+(aq)]/[H2CO3(aq)]
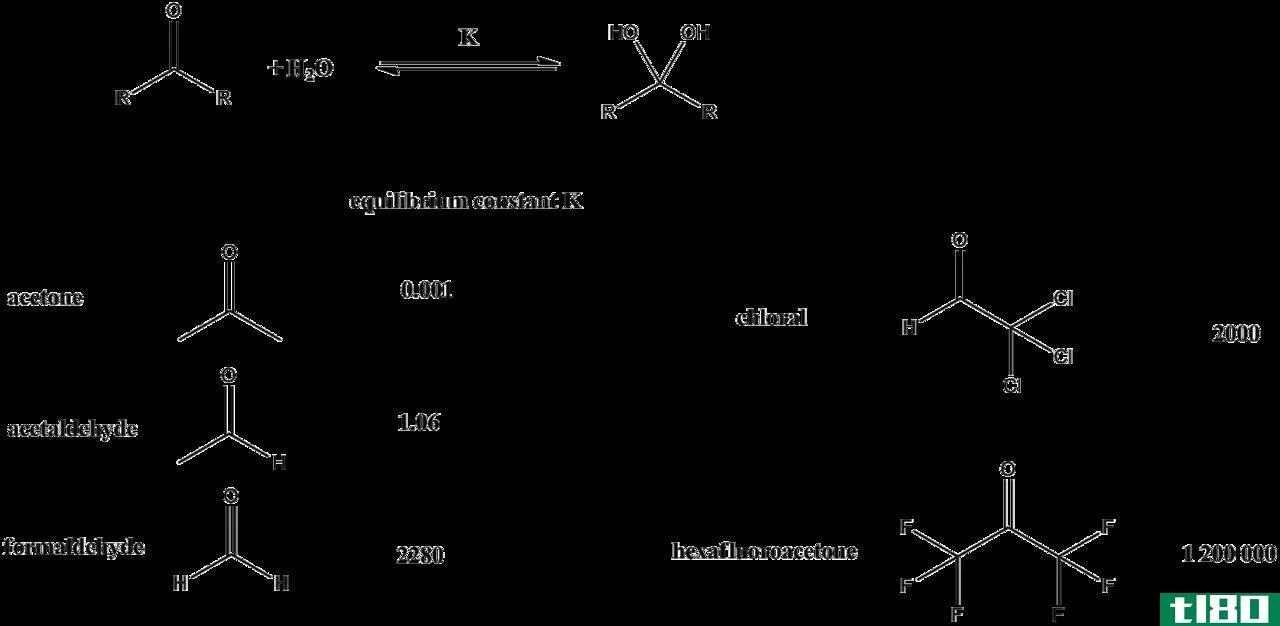
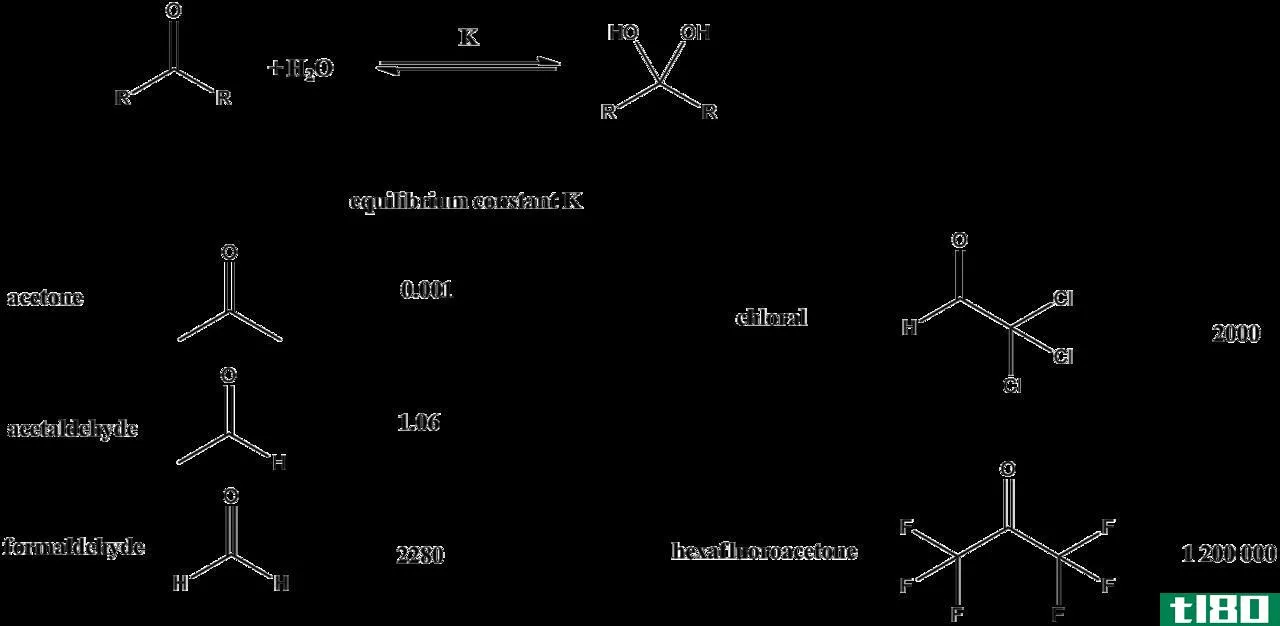
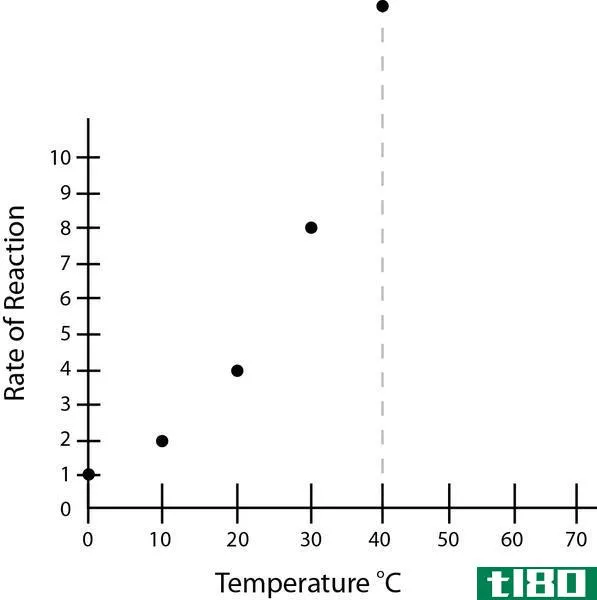
图01:不同化合物在水溶液中的平衡常数
什么是形成常数(formation c***tant)?
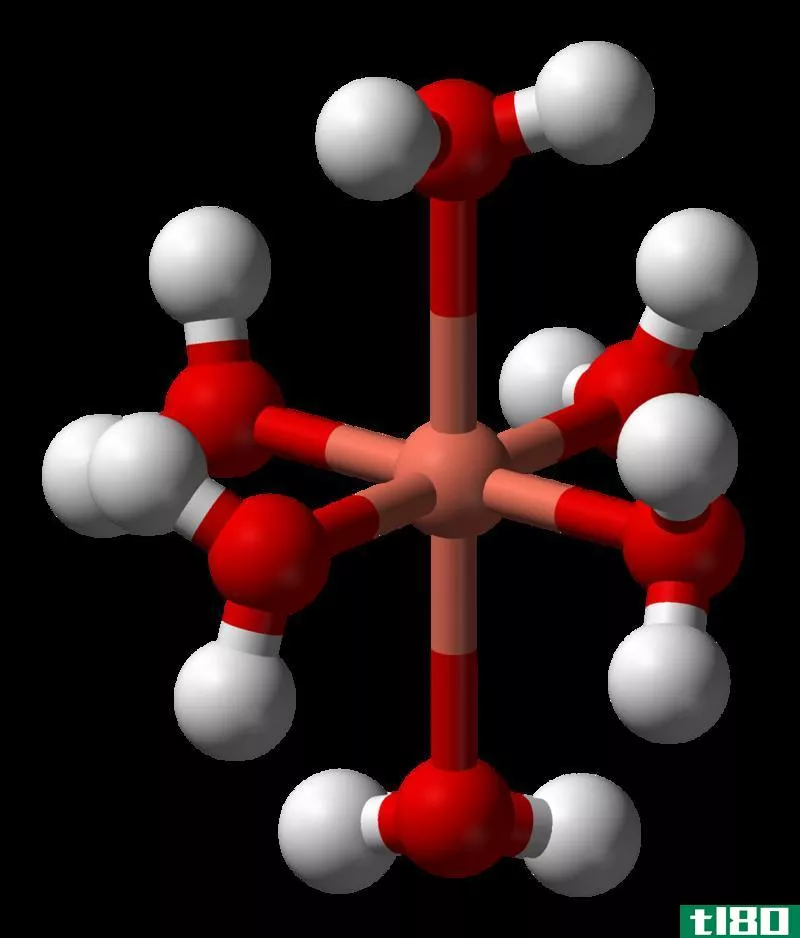
形成常数是从溶液中的组分形成配位络合物的平衡常数。我们可以用Kf来表示。这种平衡主要用于形成复合离子。形成复合离子所需的组分是金属离子和配体。
金属离子与配体的Lewis酸碱相互作用形成复合离子。金属离子总是带一个正电荷,它充当路易斯酸,而配体应该携带一个或多个孤电子对作为路易斯碱。小金属离子由于电荷密度高,极易形成复合离子。
一般来说,络合物离子的形成是一个逐步反应,它包括了配体加成的所有步骤,因此这些步骤也有各自的平衡常数。例如,铜铵络合物离子的形成有四个步骤。因此它有四个不同的平衡常数:K1、K2、K3和K4。那么,整个反应的形成常数如下:
Kf=K1K2K3K4
平衡常数(equilibrium c***tant)和形成常数(formation c***tant)的区别
平衡常数可以用来解释不同平衡态的行为,而形成常数是一种平衡常数。平衡常数与生成常数的关键区别在于,平衡常数是平衡时产物浓度与反应物浓度之比,而形成常数是由其组成成分形成配位化合物的平衡常数。
以下信息图总结了平衡常数和形成常数之间的差异。

总结 - 平衡常数(equilibrium c***tant) vs. 形成常数(formation c***tant)
平衡常数可以用来解释不同平衡态的行为,而形成常数是一种平衡常数。平衡常数与生成常数的关键区别在于,平衡常数是平衡时产物浓度与反应物浓度之比,而形成常数是由其组成成分形成配位化合物的平衡常数。
引用
1“17.3:复合离子的形成。”化学剧本,剧本,2019年6月17日,可在这里查阅。