关键区别-平衡常数与平衡位置
平衡常数是表示反应混合物在其平衡状态下的产物和反应物数量之间关系的数字,而平衡位置是平衡的正向反应等于反向反应的时刻。这是平衡常数和平衡位置的关键区别。
平衡是一个系统同时存在一个正向和反向反应的状态。这意味着,存在着相互平衡的对立反应。平衡常数定量地解释了系统的平衡状态,而平衡位置则定性地解释了平衡状态。
目录
1. 概述和主要区别
2. 什么是平衡常数
3.什么是平衡位置
4. 并列比较-平衡常数与平衡位置的表格形式
5. 摘要
什么是平衡常数(equilibrium c***tant)?
平衡常数是给出反应混合物在其平衡状态下的产物量和反应物数量之间关系的数字。反应混合物的平衡状态是指反应物或产物不再发生变化的系统所接近的状态。平衡常数是产物浓度与反应物浓度之比。

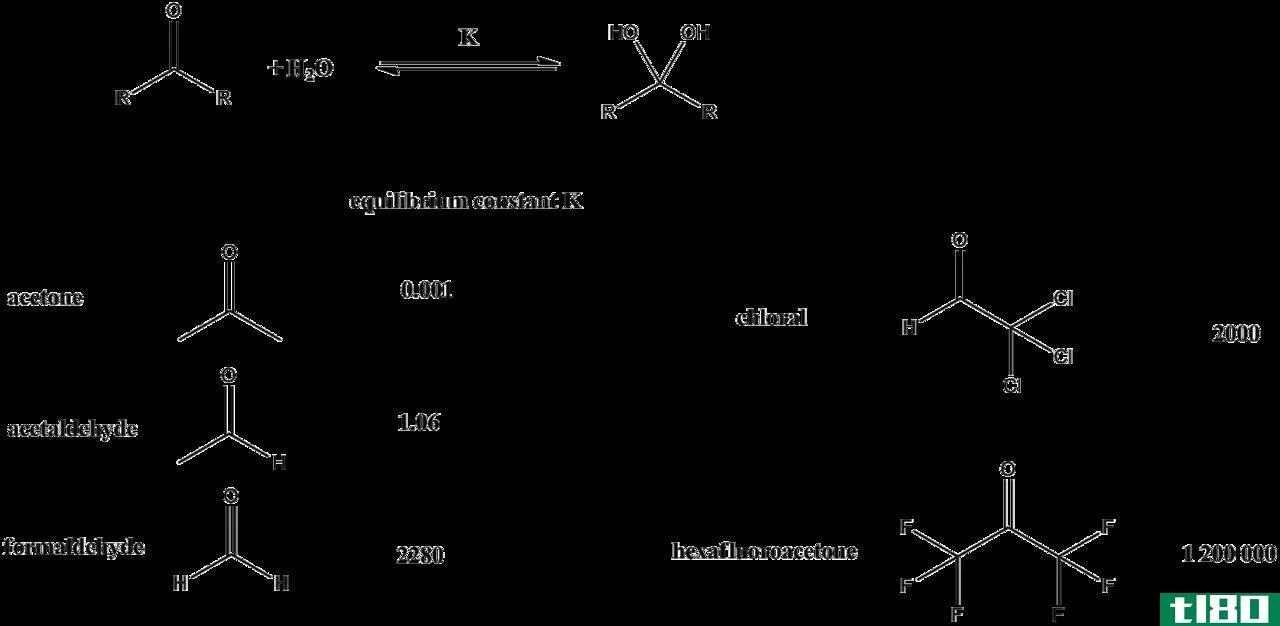
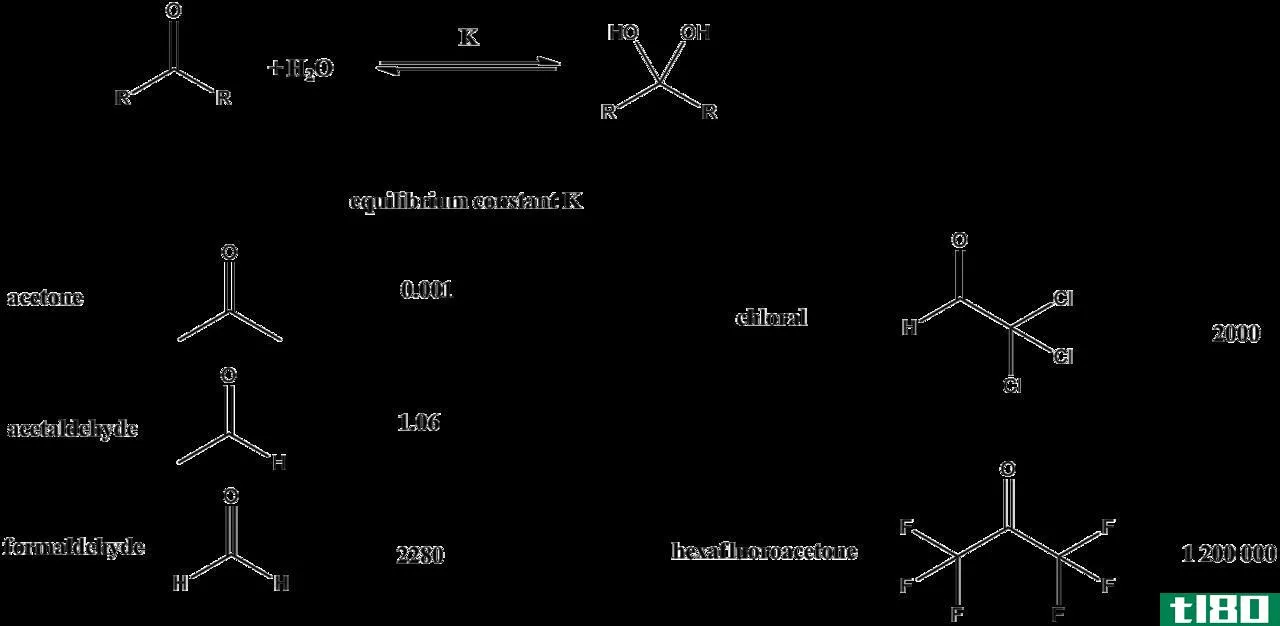
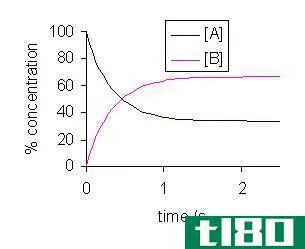
图01:用来表示平衡的符号
平衡常数与反应物的初始浓度无关。影响平衡常数值的因素有温度、溶剂性质、反应混合物中离子的离子强度等。平衡常数用“K”表示。
平衡常数方程
A+B组↔ C
对于上述反应,平衡常数如下所示。
K=[C]/[A][B]
这也被称为浓度的平衡常数,因为反应物和产物的浓度是用来写表达式的。用Kc表示。如果K值大于1,则平衡有利于产物。但当K值小于1时,平衡有利于反应物。在写平衡常数的表达式时,应考虑方程的化学计量值。
aA+bB型↔ 复写的副本
上述方程的K值如下。
K=[C]C/[A]A[B]B
对于气态化合物之间的反应,平衡常数是压力的平衡常数。用Kp表示。其中考虑了气体的压力,平衡常数的单位由压力单位给出。
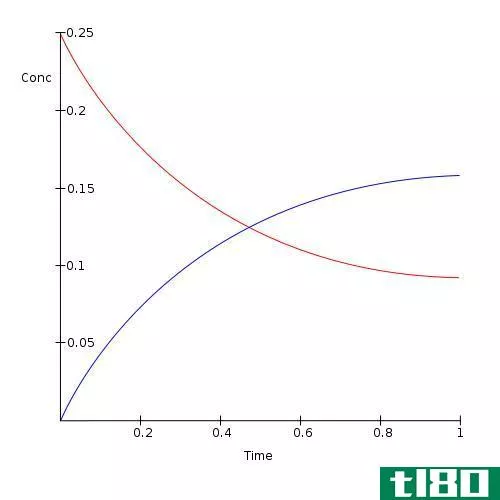
什么是平衡位置(equilibrium position)?
平衡位置是平衡的正向反作用力等于反向反作用力的时刻。系统在平衡位置没有明显的变化。没有净量的反应物是损失,或没有产物形成。如果产物形成,它们被转化回反应物,反之亦然。
平衡常数(equilibrium c***tant)和平衡位置(equilibrium position)的区别
| 平衡常数与平衡位置 | |
| 平衡常数是表示反应混合物在其平衡状态下的产物量和反应物数量之间关系的数字。 | 平衡位置是平衡的正向反作用力等于反向反作用力的时刻。 |
| 自然 | |
| 平衡常数是一个给出平衡状态的数字。 | 平衡位置是用来解释平衡系统状态的概念。 |
| 外部因素的影响 | |
| 平衡常数随温度、离子强度等参数的变化而变化。 | 平衡位置不会因系统的任何变化而改变。 |
总结 - 平衡常数(equilibrium c***tant) vs. 平衡位置(equilibrium position)
平衡常数是对系统平衡状态的定量解释,而平衡位置是平衡系统的定性解释。平衡常数和平衡位置的区别在于,平衡常数是给出反应混合物在其平衡时的产物和反应物数量之间关系的数字,而平衡位置是平衡的正向反应等于反向反应的时刻。
引用
1.歌词。“平衡常数”,化学歌词,歌词,2018年3月23日。这里有2,“平衡常数”,韦氏,韦氏。此处提供
2.“平衡常数”,韦氏,韦氏。