一级动力学同位素效应与二级动力学同位素效应的关键区别在于,一级同位素效应描述了断裂键处的同位素替代,而次级同位素效应则描述了断裂键附近的同位素替代。
动力学同位素效应(KIE)是指同位素取代后化学反应速率的变化。在这里,反应物中的一个原子被它的同位素取代,所以反应速率与初始速率不同。然后我们可以用轻同位素取代反应物的反应速率常数除以重同位素取代反应物的反应速率常数来确定KIE的值。因此,KIE大于1被认为是正常的动力学同位素效应,而KIE小于1则被认为是逆动力学同位素效应。
目录
1. 概述和主要区别
2. 什么是初级动力学同位素效应
3. 什么是次级动力学同位素效应
4. 并列比较-表格形式的一级和二级动力学同位素效应
5. 摘要
什么是初级动力学同位素效应(primary kinetic isotope effect)?
初始动力学同位素效应是指在键断裂处由于同位素取代而引起反应速率的变化。在这里,这种取代反应处于反应速率决定步骤的键断裂阶段。因此,这种同位素效应表明在速率限制步骤,同位素的键断裂或成键。
对于亲核取代反应,主动力学同位素效应适用于发生取代反应的基团、亲核分子和α碳。这种动力学效应不如理想的KIE敏感。这是由于非振动因素的贡献。
什么是次级动力学同位素效应(secondary kinetic isotope effect)?
次级动力学同位素效应是指在键断裂位置以外的一个位置,由于同位素置换而引起的反应速率的变化。换言之,它表明同位素标记的原子没有断裂或形成键。与主要动力学效应一样,这也发生在速率决定步骤中。有三种次级动力学效应,称为α、β和γ效应。
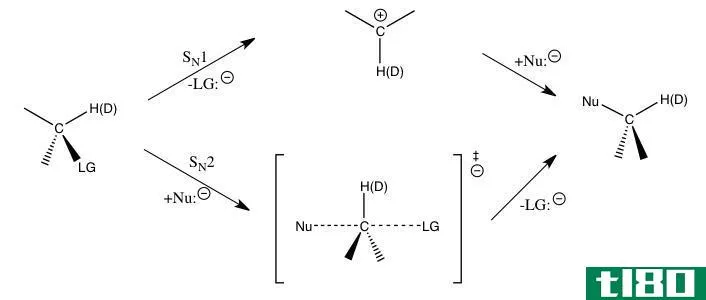
图01:氢被氘取代的分子的亲核取代
与初级KIE不同,次级KIE往往要小得多。然而,这种类型的KIE在阐明反应机理方面仍然非常有用,因为每个氘原子的次级KIE相当大。除此之外,次级动力学同位素效应的大小是由振动因素决定的。
初级的(primary)和次级动力学同位素效应(secondary kinetic isotope effect)的区别
动力学同位素效应(KIE)是指同位素取代后化学反应速率的变化。一级动力学同位素效应与二级动力学同位素效应的关键区别在于,一级同位素效应描述了断裂键处的同位素替代,而次级同位素效应则描述了断裂键附近的同位素替代。此外,与主要KIE不同,次要KIE往往更小。
此外,二次动力学同位素效应的大小取决于振动因素,而初级动力同位素效应则因非振动因素而不那么敏感。
下面的信息图总结了初级和次级动力学同位素效应之间的区别。

总结 - 初级的(primary) vs. 次级动力学同位素效应(secondary kinetic isotope effect)
动力学同位素效应(KIE)是指同位素取代后化学反应速率的变化。一级动力学同位素效应与二级动力学同位素效应的关键区别在于,一级同位素效应描述了断裂键处的同位素替代,而次级同位素效应则描述了断裂键附近的同位素替代。
引用
1“动力学同位素效应”,维基百科,维基媒体基金会,2019年11月8日,可在这里查阅。“动力学同位素效应”,化学剧本,剧本,2019年6月5日,可在这里查阅。
2“动力学同位素效应”,化学剧本,歌词,2019年6月5日,