什么是极性键?(a polar bond?)

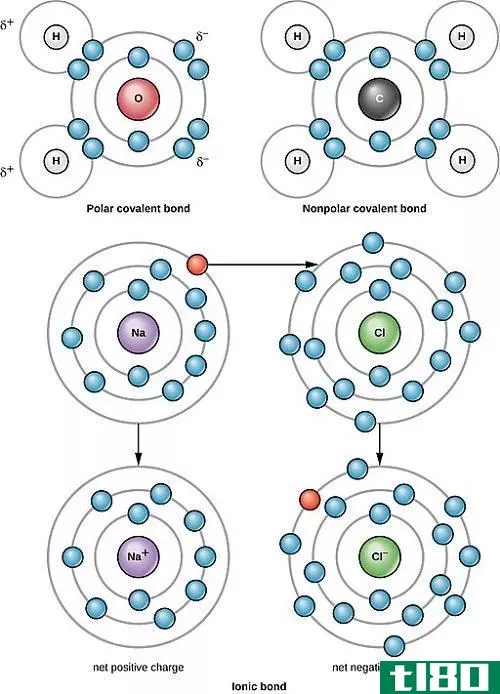
极性键是一种共价化学键,分子的电磁电荷在两端分开;i、 例如,分子的一端带有总的正电荷,另一端带有总的负电荷。不同分子中正负电荷的连接使它们能够相互结合。原子形成极性键的可能性取决于价电子与另一个原子相互作用时的行为。价电子是原子上能与其他原子形成键的电子。这些类型的键对复杂分子结构的形成至关重要;带电分子充当更复杂化合物的连接点 .

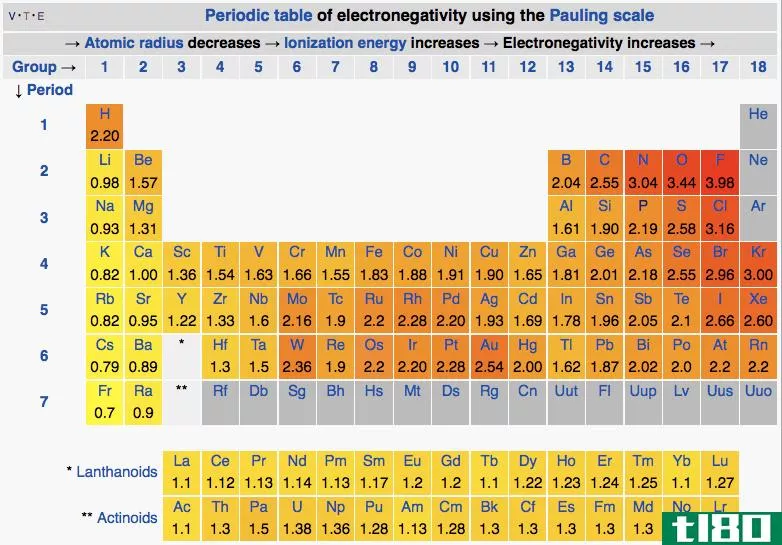
当两个原子相遇并具有相似的电负性时,就会形成共价键。电负性是电子通过原子核被吸引到价壳层,从而积累负净电荷的趋势。价壳层或电子壳层是原子的外壳。电负性的性质部分取决于价层中的电子数,以及电子与原子核的距离。价壳层中的电子数越多,原子量越大,而与原子核的距离越小。氟是电负性最强的元素。。
当两个原子相遇,其中一个原子的电负性较高时,电子会移动到电负性较低的原子的价壳层,并在那里停留大部分时间,尽管它们可能会短暂地围绕原始原子运行。两个原子成为一个分子的一部分,平均而言,分子中包含最多电子的一端带负电,而另一端带正电。
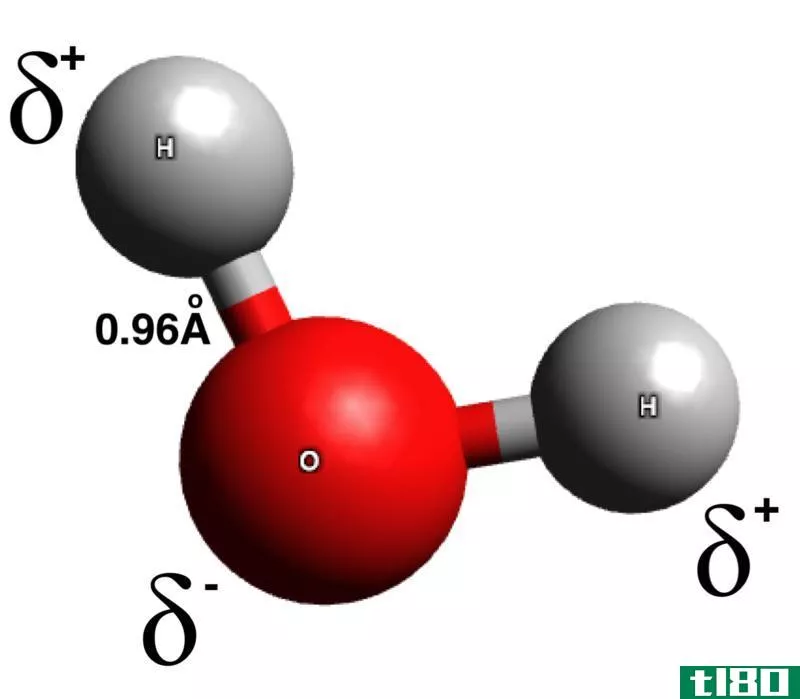
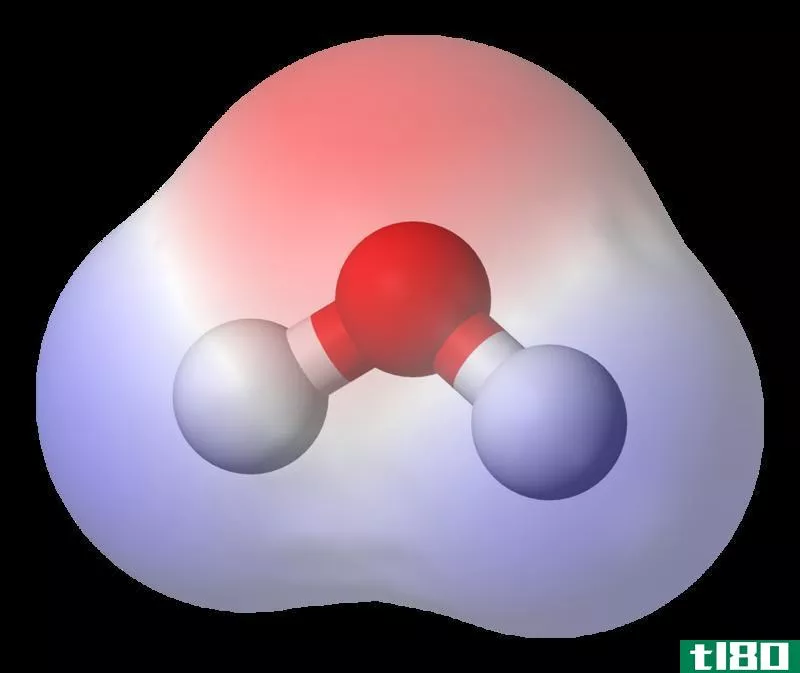
极性键最简单的例子是水分子,它由一个原子和两个氢组成,与一个原子和一个氧结合。氢原子由一个质子和一个电子组成,但由于第一个价壳层可以容纳两个电子,氢原子通常成对成键并生成二氢。虽然这两个氢原子结合在一起,但它们仍然可以接收另一个电子。同时,氧包含八个质子和八个中子;前两个电子占据最里面的电子轨道壳,在价壳层中留下六个电子,有两个空位可用。氢原子和氧原子在它们之间共享一对电子,而氧原子在大多数情况下占据电子 .
水中的极性键之所以存在,是因为氢的电负性较低,这直接受到它在共价键中倾向于吸引到自身的电子数的影响:一对氧的二。电子绕着氧原子运行,因此在分子的一端给它带负电荷。总的来说,由极性键产生的分子是电中性的,但它们的电荷集中在相反的一侧。这就是所谓的偶极子。
- 发表于 2022-02-10 22:37
- 阅读 ( 64 )
- 分类:科学
你可能感兴趣的文章
极地的(polar)和偶极分子(dipolar molecules)的区别
...中电子分布的不同而产生的。 目录 1. 概述和主要区别 2. 什么是极性分子 3. 什么是偶极分子 4. 并列比较-极性与偶极分子的表格形式 5. 摘要 什么是极性分子(polar molecules)? 极性分子是具有极性键的化学物质。这些极性键的偶极...
- 发布于 2020-09-24 05:10
- 阅读 ( 559 )
键偶极子(bond dipole)和分子偶极子(molecular dipole)的区别
...存在极性不同的两端的状态。 目录 1. 概述和关键区别 2. 什么是键偶极子 3. 什么是分子偶极子 4. 并列比较——键偶极子与分子偶极子的表格形式 5. 摘要 什么是键偶极子(a bond dipole)? 键偶极子是指在同一化学键中存在两个相反...
- 发布于 2020-10-01 16:53
- 阅读 ( 1031 )
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
...生部分正电荷和部分负电荷。 目录 1. 概述和主要区别 2. 什么是极性溶剂 3. 什么是非极性溶剂 4. 并列比较-极性和非极性溶剂的表格形式 5. 摘要 什么是极性溶剂(polar solvents)? 极性溶剂是具有大偶极矩的液体。这些是能溶解极...
- 发布于 2020-10-12 14:40
- 阅读 ( 504 )
盐桥(salt bridge)和氢键(hydrogen bond)的区别
...之间的连接,从而形成氢键。 目录 1. 概述和主要区别 2. 什么是盐桥 3. 什么是氢键 4. 并列比较-盐桥与氢键的表格形式 5. 摘要 什么是盐桥(a salt bridge)? Salt bridge is a tube that contains an electrolyte (typically in the form of a gel), providing elec...
- 发布于 2020-10-14 03:27
- 阅读 ( 988 )
共价键(covalent bond)和与格键(dative bond)的区别
...格键为共价键,这是正确的。 目录 1.概述和主要区别 2. 什么是共价键 3. 什么是与格键 4. 并列比较-共价键与与格键的表格形式 5. 摘要 什么是共价键(covalent bond)? 共价键是两个原子共用一对电子时形成的化学键。我们称之为“...
- 发布于 2020-10-17 17:57
- 阅读 ( 863 )
电负性(electronegativity)和极性(polarity)的区别
...述的是分子水平上的吸引力。 目录 1. 概述和主要区别 2. 什么是电负性 3. 什么是极性 4. 并列比较-电负性与极性的表格形式 5. 摘要 什么是电负性(electronegativity)? 电负性是一个原子吸引键中的电子朝向它的倾向。基本上,这显...
- 发布于 2020-10-22 10:07
- 阅读 ( 902 )
非极性(non-polar)和极性共价键(polar covalent bonds)的区别
非极性与极性共价键 非极性和极性共价键既属于极性的三类,也属于共价键的两类。所有这三种类型(离子、极性和非极性)都被归类为化学键,其中有一种力(电负性)允许两种特定元素的原子相互吸引。可能的共价键的数...
- 发布于 2021-06-24 05:05
- 阅读 ( 620 )
介电常数(dielectric constant)和极性(polarity)的区别
什么是介电常数(dielectric c***tant)? 介电常数是某种材料在电场作用下储存电势能的能力。它也被称为介电常数。 介电磁导率是一种物理性质,描述电场如何影响介电环境,以及电场如何因这种相互作用而改变自身。 介电磁导...
- 发布于 2021-06-26 04:32
- 阅读 ( 755 )
极地的(polar)和非极性键(nonpolar bonds)的区别
...之间,而非极性键发生在具有相同电负性的元素之间。 什么是极性键(polar bonds)? 极性键是一种共价键,当两种元素的电负性不同时,它们之间会发生共价键。电负性是指对电子的亲和性。电负性高的原子比电负性低的原子更容...
- 发布于 2021-06-27 10:16
- 阅读 ( 416 )
极地的(polar)和非极性分子(nonpolar molecules)的区别
...极矩,而在非极性分子上不形成。 这篇文章解释道, 1.什么是极性分子-定义、形成、性质、示例 2.什么是非极性分子-定义、形成、性质、示例 3. What is the difference between Polar and Nonpolar Molecules 什么是极性分子(polar molecules)? 极...
- 发布于 2021-06-28 12:20
- 阅读 ( 1826 )