键偶极子和分子偶极子的关键区别在于,键偶极子是指在一个特定的化学键中产生两个极性端。而分子偶极子是指在一种特定化合物中产生两个极性末端。
键偶极子和分子偶极子是决定化合物的化学和物理性质的重要术语。偶极子是指在同一化学键或化合物中存在极性不同的两端的状态。
目录
1. 概述和关键区别
2. 什么是键偶极子
3. 什么是分子偶极子
4. 并列比较——键偶极子与分子偶极子的表格形式
5. 摘要
什么是键偶极子(a bond dipole)?
键偶极子是指在同一化学键中存在两个相反带电端。键偶极矩是一个电偶极矩,在同一化学键中有正电荷和负电荷。这种电荷分离是由于化学键的极性引起的。我们可以把键偶极子表示为“”。我们可以给出键偶极子作为键的部分电荷的函数,由δ给出,以及“d”给出的带电端之间的距离如下:
=δd
键偶极子是一个与键轴平行的向量,它的点从负(负电荷)到正电荷(正电荷)。然而,在化学中,我们通常画一个从正到负的向量来表示电子的物理运动。
测量键偶极子的国际单位制是库仑米。实际上,这个单位不适合,因为它给出的值太大了。因此,我们可以使用带符号“D”的单位德拜,它使用(10-10 x)静态库仑的电荷和以埃为单位的距离。
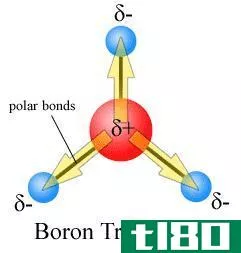
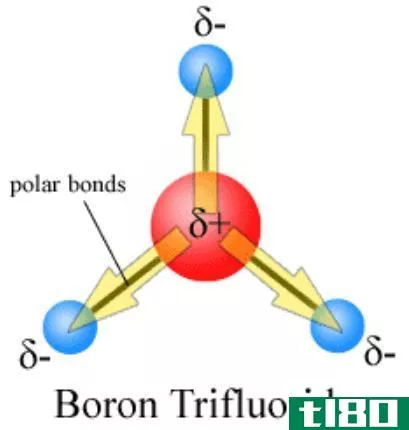
图01:表示具有三个化学键的分子中的键偶极子
对于多原子分子,键偶极子是分子内特定化学键的特征。对于双原子分子,两个原子之间只有一个键,因此,键偶极子和分子偶极子是相同的。
什么是分子偶极子(molecular dipole)?
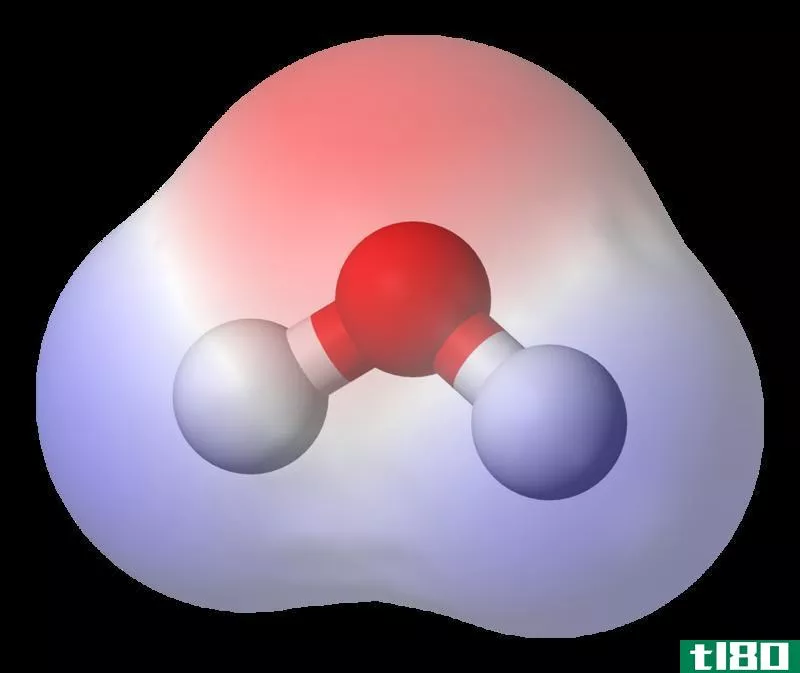
分子偶极子是指同一分子中存在两个相反的带电端。这种偶极矩是由于分子的净极性而产生的。分子的净极性或整体极性取决于分子的形状和每个化学键的极性。

图02:二氧化碳分子的结构
有时,具有极性化学键的分子可能没有净极性,因为其形状使净极性平衡为零。例如,具有两个极性键的线性分子。在这里,两个键的偶极矩向量抵消了。E、 g.二氧化碳。
键偶极子(bond dipole)和分子偶极子(molecular dipole)的区别
键偶极子和分子偶极子的关键区别在于,键偶极子一词是指在特定化学键中产生两个极性端,而术语分子偶极子是指在特定化合物中产生两个极性端。换言之,对于分子内的特定键,给出了键偶极子,而对于特定化合物,给出了分子偶极子。
下面的信息图总结了键偶极子和分子偶极子之间的区别。
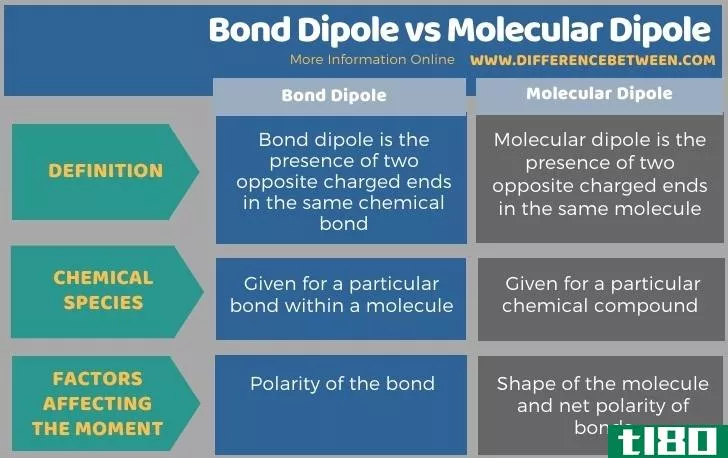
总结 - 键偶极子(bond dipole) vs. 分子偶极子(molecular dipole)
键偶极子和分子偶极子是确定化学物质的化学和物理性质的两个重要术语。键偶极子和分子偶极子的关键区别在于,键偶极子是指在特定化学键中形成两个极性端,而分子偶极子是指在特定化合物中形成两个极性端。
引用
1“偶极矩”,化学剧本,歌词,2019年9月30日,可在这里查阅。“邦德偶极矩”,维基百科,维基媒体基金会,2019年12月17日,可在这里查阅。
2“邦德偶极矩”,维基百科,维基媒体基金会,2019年12月17日,