水溶液和非水溶液的关键区别在于水溶液的溶剂是水,而在非水溶液中,溶剂是水以外的任何物质。
溶液含有溶剂和溶质。溶质溶解在溶剂中。在这里,溶质和溶剂应该具有相同的极性。而且,如果溶剂是极性的,而溶质是非极性的,反之亦然,溶质就不会溶解在溶剂中,我们就不能得到溶液。
目录
1. 概述和主要区别
2. 什么是水溶液
3. 什么是非水溶液
4. 并列比较-表格形式的水溶液和非水溶液
5. 摘要
什么是水溶液(an aqueous solution)?
水溶液是以水为溶剂的任何溶液。在这里,溶质必须是亲水的和极性的,才能溶解在水中形成水溶液。虽然我们称水为万能溶剂,但我们不能溶解几乎所有的东西。例如,我们不能将脂肪溶解在水里,所以任何地方都没有脂肪水溶液。
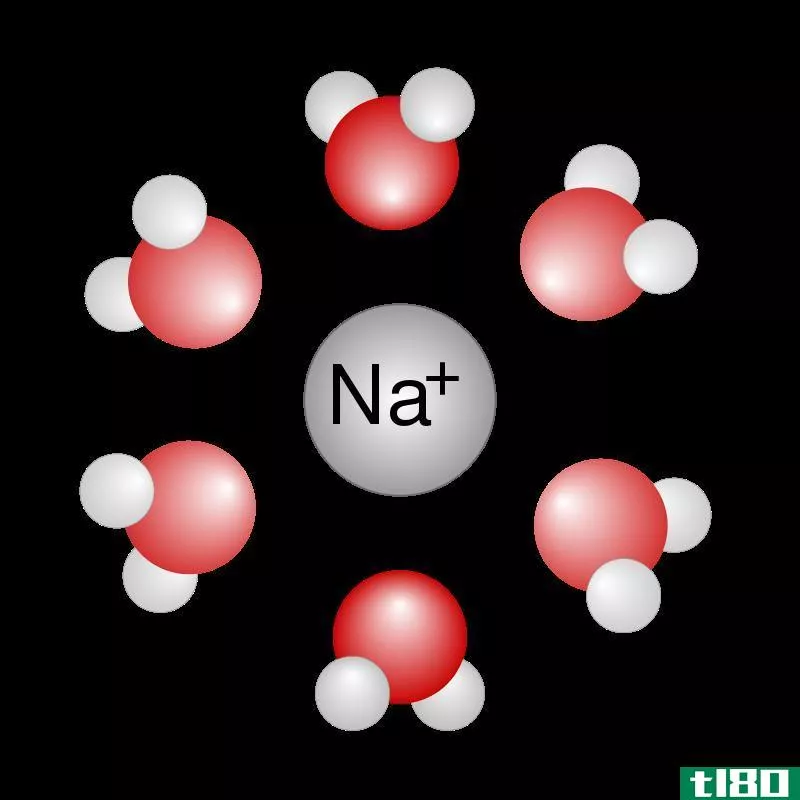
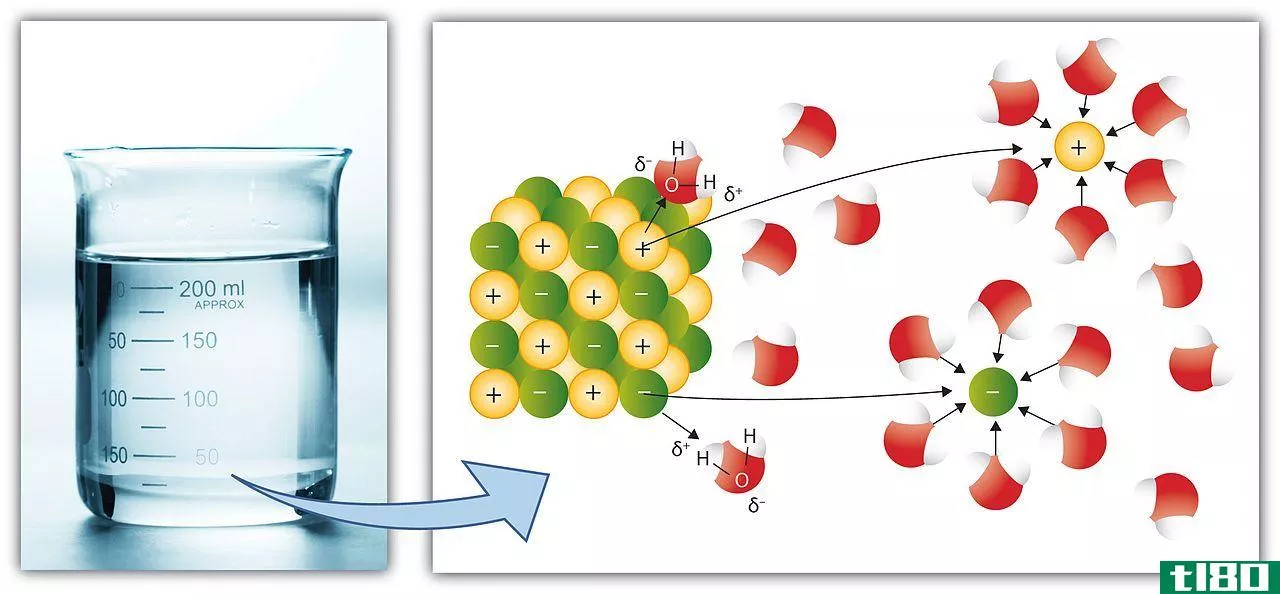
图01:水中钠离子
在写化学方程式时,我们用符号(aq)作为下标来表示物质在水溶液中。如果溶质溶解在水里能分解成离子,我们说水溶液是导电的,因为它能通过溶液导电,因为离子的存在。
什么是非水溶液(nonaqueous solution)?
非水溶液是我们将溶质溶解在除水以外的任何溶剂中而得到的溶液。溶剂可以是丙酮、甲苯、醚、醇、苯等有机化合物。

图02:酒精中的碘
溶剂可以是极性的,也可以是非极性的,这取决于溶质在溶剂中溶解时的极性。碘在酒精中的溶液和碘在四氯化碳中的溶液是非水溶液的例子。
水的(aqueous)和非水溶液(nonaqueous solution)的区别
根据溶剂的不同,我们可以把溶液分为两类:水溶液和非水溶液。水溶液和非水溶液的关键区别在于水溶液的溶剂是水,而在非水溶液中,溶剂是水以外的任何物质。氯化钠、氨水等的水溶液是水溶液的例子,而碘在酒精中的溶液、碘在四氯化碳中的溶液等是非水溶液。

总结 - 水的(aqueous) vs. 非水溶液(nonaqueous solution)
基本上,根据溶剂的不同,我们可以把溶液分为两类:水溶液和非水溶液。水溶液和非水溶液的关键区别在于水溶液的溶剂是水,而在非水溶液中,溶剂是水以外的任何物质。
引用
1赫尔曼斯汀,安妮·玛丽。“水溶液在化学中的定义”,ThoughtCo,2019年1月13日,可在此处查阅。