溶剂和溶质的关键区别在于溶质是被溶解的,而溶质是溶解它的责任。
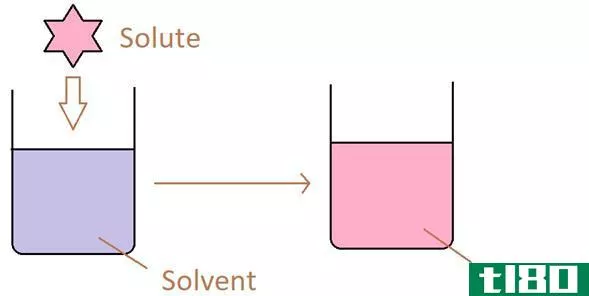
溶液是两种或两种以上物质的均匀混合物。我们称之为均质混合物,因为在整个溶液中成分是均匀的。此外,溶液的组分主要由溶质和溶剂两种类型组成。溶剂溶解溶质,形成一个统一的溶液。所以,通常溶剂量高于溶质量。
目录
1. 概述和主要区别
2. 什么是溶剂
3. 什么是溶质
4. 并列比较-溶剂与溶质的表格形式
5. 摘要
什么是溶剂(solvent)?
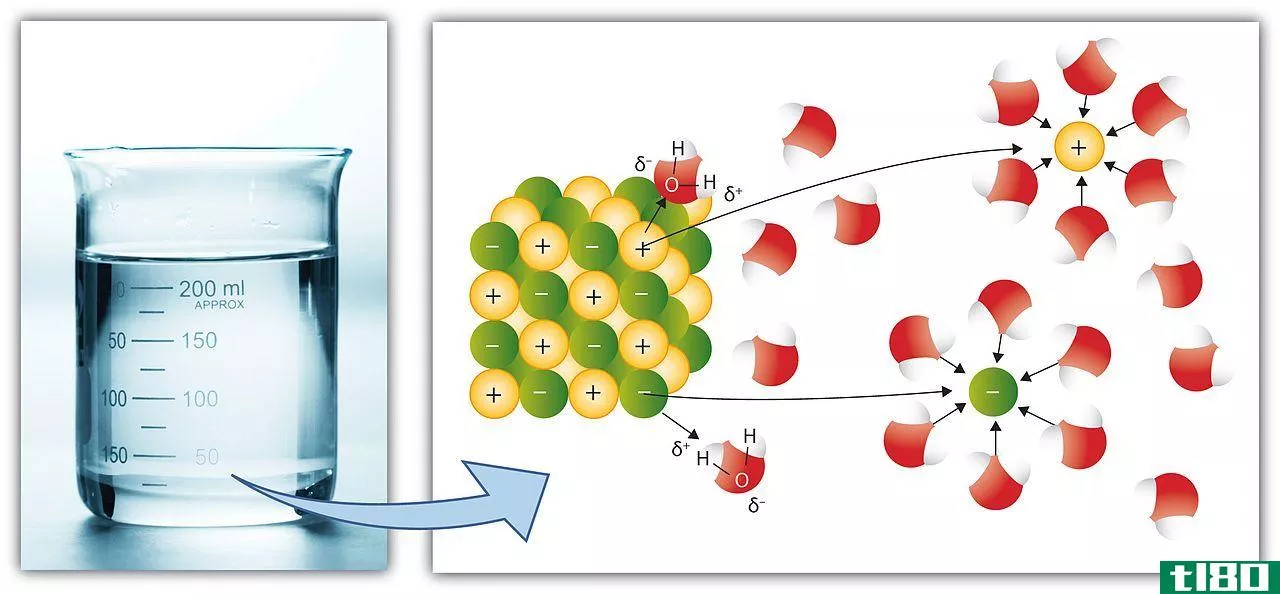
溶剂是一种具有溶解能力的物质。因此,它可以溶解另一种物质。此外,溶剂可以是液态、气态或固态。然而,最常见的是,我们使用液体作为溶剂。此外,在液体中,水是一种普遍的溶剂,因为它比任何其他溶剂都能溶解许多物质。此外,我们可以在液体溶剂中溶解气体、固体或任何其他液体溶质。但是,在气体溶剂中,只有气体溶质会溶解。

图01:乙酸可用作有机溶剂
此外,我们可以添加到一定量溶剂中的溶质量是有限制的。我们说如果我们在溶剂中加入了最大量的溶质,溶液就饱和了。溶剂分为有机溶剂和无机溶剂两种。例如,乙醚、己烷和二氯甲烷是有机溶剂,而水是无机溶剂。
极性和非极性溶剂
溶剂分为极性溶剂和非极性溶剂两大类。
极性溶剂分子具有电荷分离,因此能够溶解极性溶质。在溶解过程中,可能发生偶极-偶极相互作用或偶极诱导偶极相互作用。我们可以进一步将极性溶剂分为极性质子溶剂和极性非质子溶剂。极性质子溶剂能与溶质形成氢键。因此,它们通过氢键溶剂化阴离子。水和甲醇是极性质子溶剂。极性非质子溶剂不能形成氢键。然而,它们具有较大的偶极矩,因此与离子溶质形成偶极-偶极相互作用,使它们溶剂化。丙酮是一种极性非质子溶剂。
非极性溶剂溶解非极性溶质。己烷、苯和甲苯是一些常见的非极性溶剂。
除上述分类溶剂外,还有一些溶剂具有中间极性和非极性。根据“类溶似溶”现象,溶剂溶解与其相匹配的溶质。
属性
当我们在实验室使用溶剂时,必须知道溶剂的性质。例如,了解溶剂的沸点有助于我们确定如何使用蒸馏方法来分离它们。另外,溶剂的密度在溶剂萃取技术中很重要。挥发性、毒性和易燃性是我们在处理不同溶剂时必须关注的一些其他参数。
什么是溶质(solute)?
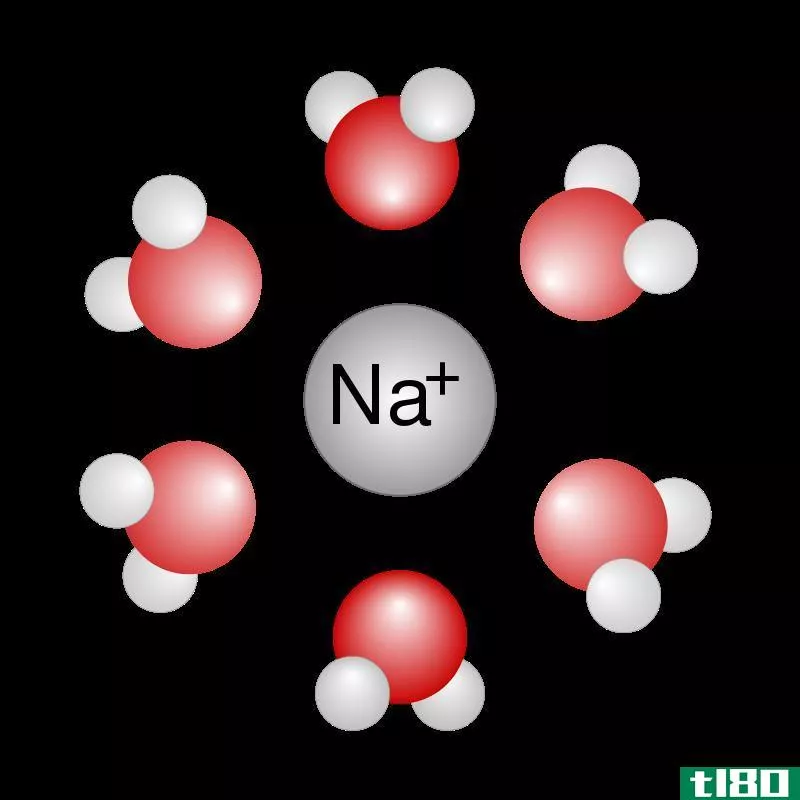
溶质是溶解在溶剂中形成溶液的物质。溶质可以是液相、气相或固相。通常,在溶液中,溶质的含量比溶剂少。

图02:盐水含有盐作为溶质
当一个溶液有它能溶解的最大数量的溶质时,我们称之为溶液饱和。溶质在溶剂中的溶解会改变溶剂的性质。
溶剂(solvent)和溶质(solute)的区别
溶剂是一种具有溶解能力的物质,因此可以溶解另一种物质,而溶质则是溶解在溶剂中形成溶液的物质。这是溶剂和溶质的关键区别。此外,溶剂和溶质在物理状态、溶解度和沸点等方面还存在一些差异。例如,考虑到沸点,溶质的沸点通常高于溶剂的沸点。
下面的信息图显示了溶剂和溶质之间差异的更多细节。

总结 - 溶剂(solvent) vs. 溶质(solute)
溶质是溶解在溶剂中形成溶液的物质。因此,溶剂和溶质的区别在于,溶质是被溶解的物质,溶剂负责溶解它。
引用
1“有偿付能力”,维基百科,维基媒体基金会,2018年9月6日。这里有2个。“解决方案”,维基百科,维基媒体基金会,2018年9月21日。可在这里查阅
2“解决方案”,维基百科,维基媒体基金会,2018年9月21日